广西南宁市宾阳中学2025-2026学年高一年级春季学期期中考试 化学试题
2026-05-15
|
4份
|
17页
|
49人阅读
|
1人下载
资源信息
| 学段 | 高中 |
|---|---|
| 学科 | 化学 |
| 教材版本 | - |
| 年级 | 高一 |
| 章节 | - |
| 类型 | 试卷 |
| 知识点 | - |
| 使用场景 | 同步教学-期中 |
| 学年 | 2026-2027 |
| 地区(省份) | 广西壮族自治区 |
| 地区(市) | 南宁市 |
| 地区(区县) | 宾阳县 |
| 文件格式 | ZIP |
| 文件大小 | 1.45 MB |
| 发布时间 | 2026-05-15 |
| 更新时间 | 2026-05-15 |
| 作者 | 匿名 |
| 品牌系列 | - |
| 审核时间 | 2026-05-15 |
| 下载链接 | https://m.zxxk.com/soft/57883025.html |
| 价格 | 1.00储值(1储值=1元) |
| 来源 | 学科网 |
内容正文:
宾阳中学高一年级2026年春季学期期中考试
化学
命题:林思影蒋莹审题:黎华琼
(全卷满分:100分,考试用时:75分钟)
可能用到的相对原子质量:H1C12N14016Mn55Fe56Cu64
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.有机高分子材料在生活和生产的各个领域中都有极为广泛的应用。下列有关说法错误的是()
A.棉花、羊毛和塑料均属于天然有机高分子材料
B.聚乙烯具有耐化学腐蚀等性能,常被用作食品、药物的包装材料
C.以石油、天然气和煤等为原料制成有机小分子单体,再经聚合反应生产合成纤维
D.硫化橡胶具有更好的强度、韧性、弹性和化学稳定性,橡胶硫化的过程发生了化学变化
2.下列化学用语中正确的是()
A.乙烯的结构简式:CHCH
CI
B.CCl4的电子式:Cl:C:Cl
CI
C.CH4分子的空间填充模型:
CH3
D.CH一CH2一C一CH一CH3用系统命名法命名:3,3.二甲基.4.乙基戎烷
CH3 C2Hs
3.化学在科技发展中起到了重要的作用,与生产、生活和社会发展密切相关,下列叙述错误的是()
A.军事装备系统中常用La-i储氢合金,可在室温下快速吸放氢
B.用于北京冬奥会礼仪服智能发热的石墨烯属于无机非金属化合物
C.宇树机器人的触觉传感器材料压电陶瓷,属于新型无机非金属材料
D.含铅的原料制造的光学玻璃透光性好、折射率高,可用来制造眼镜、照相机的透镜
第1页共8页
4下列反应的离子方程式书写正确的是()
A.Fe(OH)3溶于氢碘酸:Fe(OHD3+3H=Fe3++3HO
B.实验室用氯化铵和熟石灰共热制氨气:NH+OHNL,个+H,O
C.用稀硝酸洗涤试管内壁的银镜:Ag+2Ht+NO?=Ag*+NO↑+H0
D.水玻璃露置在空气中变浑浊:SiO+CO2+H,O=H,SiO3↓+CO
5.设N为阿伏加德罗常数的值,下列说法正确的是()
A.标准状况下,11.2LHC1气体中含有的H数目为0.5NA
B.1mol甲基(-CH)含有的电子数为9NA
C.10mL1mol.L1的KoH水溶液中含有氧原子数为0.01N
D.一定条件下,1nolN2与4molH,反应生成的NH分子数为2NA
6.下列说法正确的是()
CH,
H,一CH-CH
A.CHo与C6H14一定互为同系物
B
和
CH,-CH-CH,-CH,CH,-CH,
是同分异构体
C.1H2与2H2互为同位素
CH的一溴代物有4种
7.下列实验操作正确且能达到实验目的的是(
铜丝
浓硝酸
木炭与
浸NaOH
NH.CI
溶液的
棉花
浓H,SO.
棉团
澄清
石灰水目
Fe
Cu
A.
可通过拉动铜丝控
B.比较Fe和Cu的金
C.制备、收集氨气
D.检验CO2
制反应的发生和停止
属活动性
8.下列有关有机物的叙述中正确的是(
A.沸点:新戊烷>异戊烷>正戊烷
B.在光照条件下,烷烃易与溴水发生取代反应
C.CHCL,只有一种空间结构
D.用酸性KMnO,溶液可以除去甲烷中混有的乙烯
第2页共8页
9.某有机物的结构简式如图所示,下列说法错误的是()
A.该物质中含有两种官能团
CH,CHOH
B.该物质能发生加成、氧化、取代反应
CH:
C.lmol该物质与足量金属钠反应生成1molH,
D.该物质完全加氢后的分子式为CHisO
10.反应NO2(g)+CO(g)=NO(g)+CO,(g)的能量变化如图所示,下列说法正确的是()
↑能量
b
CO
a
NO+CO2
c
反应过程
A.图中a→b为放热过程
B.因该反应放热,故升高温度,反应速率减慢
C.该反应中,断裂反应物化学键的能量变化大于形成生成物化学键的能量变化
D.理论上可以借助原电池装置使该反应以电能的形式释放的能量
11.2-氯-1,3-丁二烯是化工生产中一种非常重要的单体,其工业生产方法如下。
7080C
Cu2C2,20~50℃
2HC≡CH
CH2=CH-C≡CH
①Cu2Cl2,NH4C
②HCI
(原子利用率-目标产物中日标原子的总数×100%)
反应物中该类原子的总数
下列说法错误的是()
A.乙炔分子的球棍模型:O
B.反应①为加成反应,反应②为取代反应
C.反应①的产物乙烯基乙炔CH2=CH-C三CH中所有原子处于同一平面
D.该工业生产方法的原子利用率理论上为100%
第3页共8页
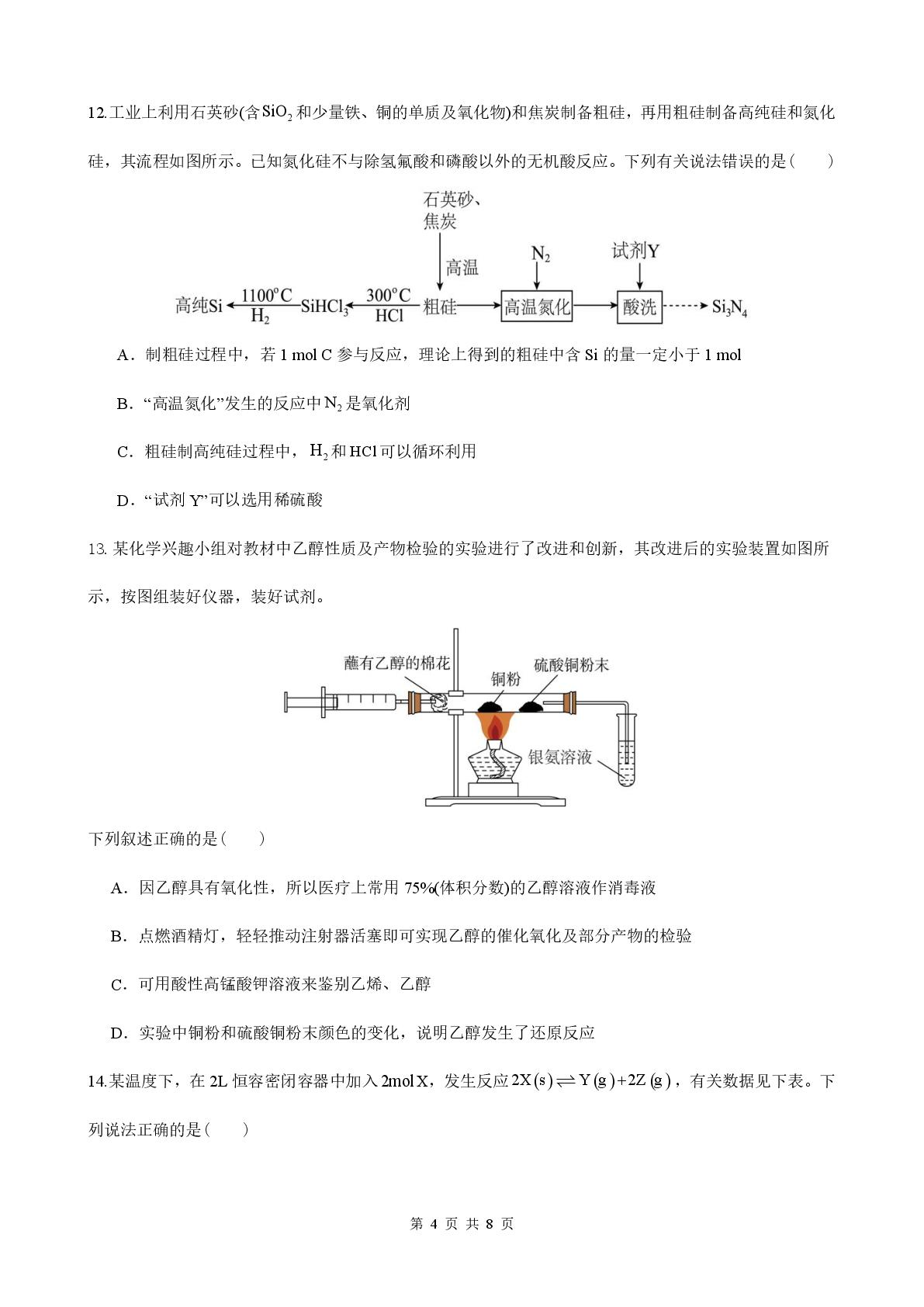
12.工业上利用石英砂(含SO,和少量铁、铜的单质及氧化物)和焦炭制备粗硅,再用粗硅制备高纯硅和氨化
硅,其流程如图所示。已知氨化硅不与除氢氟酸和磷酸以外的无机酸反应。下列有关说法错误的是()
石英砂、
焦炭
N2
试剂Y
高温
高纯si←100 C SiHCI5300C
H2
HC1粗硅
高温氮化
酸洗
…→Si,N4
A.制粗硅过程中,若1molC参与反应,理论上得到的粗硅中含Si的量一定小于1mol
B.“高温氮化”发生的反应中N2是氧化剂
C.粗硅制高纯硅过程中,H,和HC1可以循环利用
D.“试剂Y可以选用稀硫酸
13.某化学兴趣小组对教材中乙醇性质及产物检验的实验进行了改进和创新,其改进后的实验装置如图所
示,按图组装好仪器,装好试剂。
蘸有乙醇的棉花
硫酸铜粉末
铜粉
银氨溶液
下列叙述正确的是()
A.因乙醇具有氧化性,所以医疗上常用75%(体积分数)的乙醇溶液作消毒液
B.点燃酒精灯,轻轻推动注射器活塞即可实现乙醇的催化氧化及部分产物的检验
C.可用酸性高锰酸钾溶液来鉴别乙烯、乙醇
D.实验中铜粉和硫酸铜粉末颜色的变化,说明乙醇发生了还原反应
14.某温度下,在2L恒容密闭容器中加入2molX,发生反应2X(s)一Y(g)+2Zg),有关数据见下表。下
列说法正确的是()
第4页共8页
时间段
0~10s
020s
0-30s
v(Z)/(mol-L-1.g-1)
0.05
0.03
0.02
A.5s时,Y的浓度等于0.125mol.L1
B.020s内,用X表示的平均速率为0.03nol.L1.s1
C.反应到20s时,已经达到化学平衡状态
D.容器内气体Y的体积分数不再变化时,达到化学反应的限度
二、非选择题:本题共4小题,共58分。(除标注外,每空2分)
15.(14分)C1C1为白色固体,常用作催化剂、杀菌剂、媒染剂等,实验室一般将$0,通入新制氢氧化铜
中制备CuC1,实验装置(加热和夹持装置略去)如图所示。己知:CuC1难溶于水和乙醇,能溶于浓盐酸,
在潮湿的环境中易被氧气氧化为碱式氯化铜。
70%浓硫酸
NaOH
溶液
Na.SO.
固体
aOH
溶液
溶液
B
(1)仪器b的名称为
(2)长导气管a的作用是
,B中的试剂X应选择下列
试剂(填序号)。
①饱和NaHSO3溶液
②饱和Na2SO3溶液
③饱和Na2SO4溶液
(3)实验过程中先向C中加入一定量的CCl溶液,滴加适量的NaOH溶液,再启动A中的反应,一段时间
后C中产生白色固体,产生白色固体的离子方程式为
当
(填实验现象)时,CuCl的制备结束,然后
(填实验操作)。
(4)将C中混合物采用抽滤法快速过滤,再分别用水、乙醇洗涤,最后在真空干燥机内干燥得到C1C1产品。
用乙醇洗涤的目的是
第5页共8页
16.(16分)回答下列问题。
I.合成尿素[CO(NH,)2]:一种合成尿素反应的机理及能量(单位:kJ.mol-)变化如图,Ts表示过渡
态。
TS3
TS2
+NH3+3H2O
TSI
(87.5)
COz(g)+2NH;(g)
+NH+2H,0
o(g)
+2H20(g)
+3H,0(g)
(0.00)
反应①
(36.8)
反应②
反应③
(I)合成尿素总反应2NH,(g)+C0,(g)=CO(NH,),(g)+H,O(g)是
反应(填“吸热”或“放热)
(已知△E,=66.5 kJ.mol,△E2=241.0 kJ.mol)。
(2)若向某恒温恒容的密闭容器中加入等物质的量的NH,和CO2,发生(1)中反应,下列叙述能说明反应
已经达到平衡状态的是
(填标号)。
a.2vE(NH3)=v(CO2)
b.化学平衡常数K不变
c.CO,的体积分数不再变化
d.体系中气体的密度不变
(3)如图甲为使用不同催化剂①、②、③时,反应至相同时间,容器中尿素的物质的量随温度变化的曲线,
A点
(填“是或不是")平衡状态,T),C以上曲线②n[CO(NH,)2]下降的原因可能是
(答出一点即可)。
负载
(HNO3]
3
N
一空气
电
电
极
KOH
溶液
N,H
T
T
TIC
图甲
图乙
Ⅱ.肼一空气燃料电池是一种新型电池,无污染,能量高,有广泛的应用前景,工作原理如图乙所示。
(4)该燃料电池中正极通入的物质是
,该燃料电池工作时,溶液中OH向电极移动(填“a”或),
负极的电极反应式为
电池工作时电路对外提供了1mol电子,a电极
生成气体的体积为一L(折算成标准状况下)。
第6页共8页
17.(13分)以软锰矿(主要成分是MnO2、含有少量的FO4、AlO3、SiO2)为主要原料制备高纯碳
酸锰的工艺流程如图所示:
稀硫酸S0,
MnO.
MnCO.
NH,HCO,溶液
软锰矿
浸取
过滤→氧化→除杂→过滤→沉锰
过滤
…→高纯MnCO
滤渣1
滤渣
已知:①MnC03难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解;
②Mn(OHD2开始沉淀时pH为7.7,则:
(1)浸取时S02发生
(填“氧化”或“还原”)反应(1分),“浸取”反应中往往有副产物MnS,O。生
成,温度对浸取反应的影响如图所示:
100
百
90
分
80
■代表温度对锰浸出率的影响
70
◆代表浸锰温度与MnS,O6
(%)
60
生成率的关系
50
0
30
201
10
0
153045607590105120135一
温度/℃
为减少MS,O。的生成,“浸取的适宜温度是
(2)滤渣I主要成分是
(填化学式)。
(3)氧化”操作的离子方程式为
(4)沉锰时,加入NH4HCO3溶液调节溶液pHK7.7,充分反应直到不再有气泡产生;若溶液p7.7,会导
致产品中混有
(填化学式)
(⑤)生成的碳酸锰产品需要充分洗涤,检验碳酸锰产品已完全洗净的方法是
(6)取g碳酸锰样品,加适量硫酸加热溶解后,用c mol.L1的MnO4溶液滴定,至滴定终点(高锰酸钾
恰好反应完即为滴定终点)时,消耗KMnO4溶液的体积为VmL。(已知:反应产物为MnO2,杂质不参
与反应),则样品中MnCO3质量分数的计算式为
(用质量分数表示,无需化简)。
第7页共8页
18.(15分)A是一种重要的有机化工原料,其产量通常用来衡量一个国家的石油化学工业发展水平,通过
一系列化学反应,可以制得成千上万种有用的物质。结合下图物质间转化关系回答问题。
Y
X
CH.OHCH.OH
CH,BrCH,Br
乙二醇
③
1,2-二溴乙烷
CH,CHO
H,0/催化剂
A
催化剂、△
E
①
CH,=CHCOOCH,CH,
02
②
G
CH,=CHCH,
D
丙烯酸乙酯
丙烯
催化剂
(1)A的电子式为
(2)①的反应类型为
Y中的官能团名称是
(3)高分子化合物G是一种常见的合成纤维一丙纶,其结构简式为
(4)B→X的化学方程式为
(⑤)关于Y的说法正确的是
①Y和乙醇互为同系物
②Y可以与水任意比互溶
③相同物质的量的A和Y充分燃烧后,耗氧量相同
(6)某醇与乙醇互为同系物,且相对分子质量比乙醇大42,则该醇的同分异构体共有
种,写出其中
不能与氧气在铜催化下反应的同分异构体的结构简式
第8页共8页宾阳中学高一年级2026年春学期
期中考试化学答题卡
姓名:
班级:
考场/座位号:
正确填涂
考号
注意事项
1.
答题前请将姓名、
班级、考场、准考证
[0]
[o]
[o]
[o]
[0]
[0]
[o]
缺考标记
号填写清楚。
[1]
[1]
[1]
[1]
[1]
[1]
[1]
口
2.客观题答题,必须
[2]
[2]
[2]
[2]
[2]
[2]
[2]
使用2B铅笔填涂,修
[3]
[3]
[3]
[3]
[3]
[3]
[3]
[4]
[4]
[4]
[4]
改时用橡皮擦干净。
[4]
[4]
[4]
3.必须在题号对应的
[5]
[5]
[5]
[5]
[5)
[5]
[5]
答题区域内作答,超
[6]
[6]
[6]
[6]
[6]
[6]
[6]
出答题区域书写无
[7]
[7]
[7]
[7]
[7]
[7]
[7]
[8
效。
[8]
[8]
[8]
[8]
[8]
[8]
[9]
[9]
[9]
[9]
[9]
[9]
[9]
、
选择题(共14小题,每小题3分,
共42分)
1[A][B][C][D]
6[A][B][C][D]
11[A][B][C][D]
2[A][B][C][D]
T[A][B][C][D]
12[A][B][C][D]
3[A][B][C][D]
8[A][B][C][D]
13[A][B][C][D]
4[A][B][C][D]
9[A][B][C][D]
14[A][B][C][D]
5[A][B][C][D]
10[A][B][C][D]
二、
非选择题(共58分)
15.
(每空2分,共14分)
(1)
(2)
(3)
(4
16.(每空2分,共16分)
(1)
(2)
(3)
(4)
17.(除标记外,每空2分,共13分)
(1)
(1分)
(2)
(3)
(4)
(5)
(6)
18.(除标记外,每空2分,共15分)
(1)
(2)
(1分)
(3)
(4)
(5)
(6)
■宾阳中学高一年级2026年春季学期期中考试化学评分细则
-、
选择题:本题共14小题,每小题3分,共42分。
2
3
4
5
6
7
8
9
10
11
12
13
14
A
C
B
D
B
A
A
C
D
B
D
B
二、非选择题:本题共4小题,共58分。(除标注外,每空2分)
15.【答案】
(1)球形干燥管
(2)平衡气压,防堵塞,保证实验安全
①
(3)2CI+SO +2Cu(OH)=2CuCI+SO-+2H,O
三颈烧瓶中溶液蓝色刚好消失
关闭A、C中分液漏斗活塞
(4)使晶体迅速干燥,防止CuC1被氧化
16.【答案】
(1)放热
(2)c
(3)不是
随着温度升高,催化剂活性降低(或发生副反应)
(4)空气
N,H,+40H.4e=N,+4H,0
5.6
17.【答案】
(1)氧化(1分)
90°C
(2)SiO,
(3)MnO,+2Fe2++4H+=2Fe3++Mm2++2H,0
(4)Mn(OH2
(⑤)取最后一次洗涤液,先加入盐酸酸化,后加几滴BaCl2溶液,若无沉淀,则已洗净
O55+12+48)cp×3
100%(其它答案合理也可)
2000m
18.【答案】
HH
H.C:C:H
(1)
(2)加成反应
羟基(1分)
七CH2-CHn
(3)
(④2CH,CH,OH+O2→2CH,CHO+2H,O
CH,
(5)②
(6)8 (CH)C(OHCH,CH宾阳中学高一年级2026年春季学期期中考试化学详细答案
1.【答案】A
【详解】A.塑料是合成有机高分子材料,A错误:
B.聚乙烯具有耐化学腐蚀等性能,常用作食品、药物的包装材料,B正确:
C.以石油、天然气、煤为原料制小分子单体再经聚合得到合成纤维,C正确:
D.橡胶疏化过程中硫原子与橡胶分子反应,将线型结构交联为网状体型结构,有新物质生成属于化学变
化,硫化后橡胶的强度、韧性、弹性和化学稳定性均显著提升,D正确:
故选A。
2.【答案】C
【详解】
A.乙烯分子中含有碳碳双键,结构简式应体现双键,正确的结构简式为:CH=CH2,A错误;
:Cl:
B.电子式书写时要将原子最外层的电子都表示出来,CCl4的电子式::C:C:C1:,B错误;
:Cl:
C.CH4分子为正四面体形,空间填充模型为:
C正确:
CH;
D.CH3一CH2-C一CH—CH3
主链有6个碳原子,3号碳原子上连有2个甲基、4号碳原子上连
CH;C2Hs
有1个甲基,用系统命名法给命名为3,3,4-三甲基己烷,D错误:
故选C。
3.【答案】B
【详解】A.L-Ni储氢合金是性能成熟的储氢材料,可在室温下快速完成吸氢、放氢过程,可应用于军
事装备领域,A正确:
B.石墨烯是碳元素组成的单质,不属于无机非金属化合物,B错误:
C.压电陶瓷是具有电声转换等特殊功能的陶瓷材料,属于新型无机非金属材料,C正确;
D.含铅光学玻璃具备透光性好、折射率高的特点,符合眼镜、照相机透镜等光学元件的性能要求,可用
于这类产品的制造,D正确;
故答案选B。
4.【答案】D
【详解】A.氢碘酸(Ⅱ)具有还原性,Fe3+会被I还原为F+,并生成I2,该离子方程式忽略了氧化还原
反应,正确的方程式为:2Fe(OHD3计6H+2I=2Fe2+I+6H0,A错误;
B.氯化铵和熟石灰共热制氨气是固体间的加热反应,不是水溶液中的离子反应,不能用离子方程式表示,
B错误;
C.稀硝酸与银反应的正确离子方程式为3Ag+4H+NO=3Ag+NO↑+2HO,选项中原子不守恒(左
侧O原子数为3,右侧为2),C错误:
D.水玻璃为Na2SiO3的水溶液,由于HCO3酸性比HSiO3强,且H2SiO3难溶于水,故露置在空气中变浑
浊时发生反应:SiO+CO2+HO=H,SiO3↓+CO,D正确。
第1页共7页
故选D。
5.【答案】B
【详解】A.HC1为共价化合物,气体中不含有H,A错误:
B.1mol甲基(-CH)中含有9mol电子,则电子数为NA,B正确;
C.10mL1mol·L的K0H水溶液中nKOH)=0.1mol·L1×0.1L0.01mol,含有溶质氢氧化钾和溶剂水,
O原子数目为二者O原子数目的总和,大于0.01NA,C错误:
D.N2与H2合成H的反应为可逆反应,反应物不能完全转化,生成H的分子数小于2NA,D错误:
故选B。
6.【答案】A
【详解】
A.C4H1o与CH4都符合烷烃通式CH2+2,均为饱和链烃,结构相似,分子组成相差2个CH2原子团,
一定互为同系物,A正确:
CH,
CH,一CH-CH3
分子式相同、结构相同,是同一种物质,故B错误:
CH,一CH-CH一CH,CH,-CH
C.同位素的研究对象是原子,H2、2H2是单质分子,不互为同位素,C错误:
D.图示为甲基环己烷,根据分子对称性,该有机物共有5种等效氢,因此一溴代物有5种,D错误:
故选A。
7.【答案】A
【详解】A.铜和浓硫酸加热反应生成$O?,通过拉动铜丝,可以控制铜丝与浓硫酸的接触与分离,从而
控制反应的发生和停止;A正确:
B.常温下,浓硝酸会使铁发生钝化,而铜能与浓硝酸反应,因此不能通过该实验现象比较二者的金属活
动性大小,B错误:
C.氯化铵受热易分解生成氯化氢和氨气,两种气体在试管口又化合生成H4C1,所以不能用此装置和药
品制取氨气,C错误;
D.木炭与浓硫酸反应生成二氧化碳和二氧化硫,两者都能使澄清石灰水变浑浊,D错误:
故答案选A。
8.【答案】C
【详解】A.相同碳原子数的烷烃支链越多,沸点越低,正戊烷无支链,沸点最高,新戊烷支链最多,沸
点最低,则沸点顺序为正戊烷>异戊烷>新戊烷,A错误:
B.光照条件下,烷烃易与卤素单质发生取代反应,与溴水不反应,B错误;
C.CH,C12只有一种空间结构,C正确;
D.酸性KnO4氧化乙烯会生成CO2,引入新杂质,无法提纯甲烷,D错误:
故选C。
9.【答案】C
【详解】A.该物质中含有碳碳双键、羟基两种官能团,A正确:
B.该物质含有碳碳双键能发生加成、氧化反应;含有羟基能发生取代反应,该羟基也能发生氧化反应,B
正确:
C.羟基中的H可以和钠反应,1mol该物质与足量金属钠反应生成0.5molH2,C错误:
第2页共7页
D.结合物质结构,碳碳双键可以和氢气发生加成反应,该物质完全加氢后的分子式为C,H1O,D正确:
故选C
10.【答案】D
【详解】A.图中a→b为化学键断裂的过程,b状态具有的总能量高于a状态,故为吸热过程,A错误;
B.升高温度,化学反应速率加快,B错误;
C.由图可知,该反应是一个放热反应,故该反应中,断裂反应物化学键的能量变化小于形成生成物化学
键的能量变化,C错误;
D.反应NO2(g)+CO(g)≥NO(g)+CO2(g)为释放能量的氧化还原反应,一定条件下可以自发进行,理
论上反应释放的能量可以借助原电池装置转化为电能,D正确:
故选D。
11.【答案】B
【详解】A.乙炔的结构简式为HC=CH,原子半径C>H,因此乙炔分子的球棍模型为O
A正确:
B.反应①为2个乙炔分子发生加成反应生成乙烯基乙炔,反应②为乙烯基乙炔与HC1发生加成反应转化
为2-氯-1,3-丁二烯,B错误:
C.乙烯为平面型分子,分子中6个原子共面,乙炔为直线型分子,分子中4个原子共线,则乙烯基乙炔
中所有原子处于同一平面,C正确:
D.该工业生产方法中,原料的原子全部转化为生成物,原子利用率理论上为100%,D正确:
故选B。
12.【答案】D
【分析】SiO2和C在高温下反应生成Si和CO而得到粗硅,粗硅和HC1在300C下反应生成SHCl3和氢
气,SHC13和氢气在1100C下反应生成高纯硅和HC1:粗硅与氨气在高温条件下反应生成氨化硅,再经稀
酸酸洗得到氮化硅,据此解答。
【详解】A.制粗硅过程中发生反应:Si0,+2cSi计2C0个,则由反应式可知,若1molC参与反应,理
论上得到的粗硅中含Si的量(0.5mol)一定小于1mol,A正确;
B.粗硅与氮气在高温条件下反应生成氮化硅,氮元素化合价降低,则高温氮化”发生的反应中N2是氧化
剂,B正确:
C.粗硅和HC1在300C下反应生成SiHCl3和氢气,SiHCI3和氢气在1100C下反应生成高纯硅和HC1,
则粗硅制高纯硅过程中,H和HC1可以循环利用,C正确:
D.稀硫酸无法除去氮化硅中可能含有的铜、硅、二氧化硅等杂质,因此“试剂Y'不能选用稀硫酸,D错
误:
故选D。
13.【答案】B
【详解】A.因为乙醇可以进入蛋白质分子的肽链环节,从而使得蛋白质变性,乙醇的渗透作用是比较强
的,可以渗透到细菌当中,从而破坏了细菌的结构,达到了消毒杀菌的作用,所以医疗上常用75%(体积
分数)的乙醇溶液作消毒液,故A错误:
B,点燃酒精灯,轻轻推动注射器活塞,乙醇进入硬质玻璃管中在铜催化条件下反应生成乙醛与水,可观
察到硫酸铜粉末变蓝,银氨溶液中生成银单质,实现乙醇的催化氧化及部分产物的检验,故B正确:
C.酸性高锰酸钾溶液遇乙烯、乙醇均褪色,不能鉴别二者,故C错误;
D.实验中银氨溶液的变化和硫酸铜粉末变蓝,说明乙醇发生了氧化反应,故D错误。
答案为:B。
第3页共7页
14.【答案】C
【详解】A.由v(Y)=二v(Z)可知,0-10s内Y的平均速率为0.025nol.L1.g1,但5g时的瞬时速率更高,
故5s时Y的浓度应大于0.025mol.L1.s1×5s=0.125mol.L1,A错误;
B.X为固体,其浓度不参与速率计算,无法用X表示反应速率,B错误;
C.20s时Z的浓度为c(Z)=-20×20s=0.03molL1.s1×20s=0.6mol·L1;30s时Z的浓度为
c(Z)=-30×30s=0.02mol.L1.s×30s=0.6molL1。因20s后Z的浓度不再变化,故反应在20s时已达到
平衡,C正确;
D.Y和Z的物质的量比始终为1:2,体积分数恒定,无法作为平衡标志,D错误;
故选C。
15.【答案】
(1)球形干燥管
(2)平衡气压,防堵塞,保证实验安全
①
(3)2C1+SO,+2Cu(OH),=2CC1↓+S0+2H,0
三颈烧瓶中溶液蓝色刚好消失
关闭A、C中分液漏斗活塞
(4)使晶体迅速干燥,防止CuCl被氧化
【分析】该实验是利用亚硫酸钠与70%浓硫酸在装置A中反应生成二氧化硫,经装置B(饱和NHSO3溶
液)后,通入装置C中与新制氢氧化铜反应生成氯化亚铜;装置D中氢氧化钠溶液用于吸收未反应的二氧
化硫,防止污染环境;同时需注意氯化亚铜难溶于水、乙醇,易被氧气氧化,实验过程应避免其接触潮湿
空气。
【详解】(1)根据图示,仪器b是球形干燥管;
(2)长导气管ā的作用是平衡气压,防堵塞,保证实验安全;由实验装置图可知,制备SO2过程中会产生
酸雾,饱和NaHSO3溶液可除去SO,中混有的硫酸酸雾,同时抑制SO2溶解,减少其损失,保证后续反应
顺利进行:饱和NaSO3溶液吸收SO2生成NaHSO3,造成目标气体损失,无法用于隔离或收集SO2;使用
饱和NSO4溶液会使得SO2大量溶于水,损耗严重,达不到保护或收集的目的:
(3)二氧化硫通入C中新制氢氧化铜,硫元素被氧化化合价升高生成硫酸根离子,C1元素被还原化合价
降低,生成CuC1沉淀,离子方程式为2C1+SO+2Cu(OH),=2CC1↓+SO+2H,0:当三颈烧瓶中溶
液蓝色刚好消失时,表明+2价Cu全部被还原为CuCl,CuCI的制备结束,然后关闭A、C中分液漏斗活
塞
(4)CCI难溶于水、乙醇,在潮湿的环境中易被氧气氧化为碱式氯化铜,而乙醇易挥发,用水洗涤可以
去除氯化亚铜表面的可溶性杂质,然后再使用乙醇洗涤,可以充分利用乙醇的易挥发性,使晶体迅速干燥,
防止CuCl被氧化。
第4页共7页
16.【答案】
(1)放热
(2)c
(3)不是
随着温度升高,催化剂活性降低(或发生副反应)
(4)空气
a
N,H4+4OH-4e=N,+4H,0
5.6
【详解】(1)由计算可得,该反应是放热反应:
(2)a.化学反应速率之比等于化学计量数之比,2vH,)V邀c0,)则正逆反应速率不相等,反应没有达
到平衡,a错误;
b.K只受温度的影响,恒温恒容的密闭容器中,K不变不能说明反应达到平衡状态,b错误;
c.CO2的体积分数不再变化,说明平衡不再移动,正逆反应速率相等,反应达到平衡状态,c正确
d.反应前后都是气体,气体质量不变,容器恒容,则气体密度是个定值,当气体密度不变不能说明反应
达到平衡状态,d错误;
故选c;
(3)使用不同催化剂①、②、③时,反应至相同时间,容器中尿素的物质的量随温度变化的曲线,A点
不是平衡状态,因为催化剂不改变平衡转化率,A点尿素的量低于③催化剂时的量,TC以上曲线
②[CONH)]下降的原因可能是:随着温度升高,催化剂活性降低(或发生副反应):
(4)燃料电池中,燃料在负极发生氧化反应,氧化剂(空气/氧气)在正极发生还原反应。电子由负极流
向正极,电解质中的阴离子向负极移动:根据图示,电极通入燃料N,H4(肼),是负极,电极反应式:
N,H,+4OH-4e=N,+4H,0;b电极通入空气(含O2),是正极,电极反应式:O,+2H,O+4e=4OH:
正极是b电极,故该燃料电池中正极通入的物质是空气;在原电池中,阴离子向负极移动。负极是电极,
所以该燃料电池工作时,溶液中OH向a电极移动;负极的电极反应式为N,H,+4OH-4e=N2+4H,O;根
据负极反应式N,H,+4OH-4e=N,+4H,0,可知每转移4mol电子,生成1molN2气体,当电路对外提供1
mol电子时,生成N2的物质的量为0.25mol,在标准状况下,生成N2的体积为
VN2)=n(N2)×'=0.25mol×22.4L/mol=5.6L。
第5页共7页
17.【答案】
(1)氧化(1分)
90°C
(2)Si0,
(3)MnO,+2Fe2++4H+=2Fe++Mn2++2H,O
(4)Mn(OH
(⑤)取最后一次洗涤液,先加入盐酸酸化,后加几滴BCl2溶液,若无沉淀,则已洗净
O55+12+48)x3×109%(其它答案合理也可)
2000mm
【分析】软锰矿的主要成分是MnO2,含有少量的FO4、AlO3、SiO2,向其中加入稀硫酸,除SiO,外
金属氧化物均可溶解,加入SO2后可将Fe+还原为Fe+,二氧化锰还原为锰离子,过滤后滤渣I为SiO2,
滤液中存在Ht、SO子、Mm2+、Fe2+、A1;向滤液中加入MnO2,可将Fe2+氧化为Fe3+,加入MnCO3调
节pH可除去溶液中的A1+和Fe+,使AI+和Fe+转化为Fe(O)2、Al(OD3,故滤渣Ⅱ为F(OD3和Al(O田3,
过滤后滤液中存在SO4和Mn+,加入H4HCO3,将Mm+转化为MnCO3。
【详解】(1)由分析可知SO做还原剂,将Fe+还原为Fe+,将二氧化锰还原为锰离子,发生氧化反应:
由图可知,90C时,MS,O。的生成率低,锰浸出率高,温度再高,变化不大,则浸锰的适宜温度是90C:
(2)见分析,过滤后滤渣I为SiO2:
(3)“氧化操作中,MnO2与Fe2+之间发生氧化还原反应,使Fe+氧化为Fe+,离子方程式为
MnO2+2Fe2++4Ht=2Fe3++Mn2++2H,0;
(4)由题目信息可知,Mm(OD2开始沉淀时pH为7.7,若加入NH4HC03溶液调节溶液pH>7.7时,会导
致产品中混有Mn(OHD2;故答案为:Mn(OH田2:
(5)生成的碳酸锰产品需要充分洗涤,由于原溶液中含有硫酸根,检验碳酸锰产品是否洗净的操作为:
取最后一次洗涤液,先加入盐酸酸化,后加几滴BC1溶液,若无沉淀,则已洗净:
(6)碳酸锰与硫酸反应生成硫酸锰,而后与KMnO4反应生成MnO2,化合价由+2价变成十4价,KMO4
由十7价变成十4价,根据化合价升降规律,设碳酸锰的物质的量为n,所以n×2=V×103×c×3,解得
n=3cVx103
3cV×103
2
o1.故MC0,质量分数为2X55+12+106-S5+12+4树ew3x106.
名
2000m
第6页共7页
18.【答案】
HH
①HCCH
(2)加成反应
羟基(1分)
+CH2-CHJ
(3)
(4)2CH,CH,OH+O:-2CH,CHO+2H,O
CH,
(⑤)②
(6)8 (CH3),C(OH)CH2CH3
【分析】A是一种重要的有机化工原料,其产量通常用来衡量一个国家的石油化学工业发展水平,A是乙
烯;乙烯和水发生加成反应生成乙醇,B是乙醇;乙醇和D反应生成E,由E逆推,D是CH=CH-COOH:
乙醇发生催化氧化生成乙醛;丙烯在一定条件下生成高分子化合物G,G是聚丙烯。
HH
【详解】(1)A是乙烯,电子式为
H:C::C:H
(2)①是乙烯和水发生加成反应生成乙醇,反应类型为加成反应;根据Y的结构简式,可知Y中的官能
团名称是羟基:
-CH2-CH
(3)丙烯在一定条件下生成高分子化合物G,G是聚丙烯,其结构简式为
CH
(4)B→X是乙醇发生催化氧化生成乙醛和水,反应的化学方程式为
2CH,CH,0H+02a→2CH,CH0+2H,0;
(5)Y为乙二醇HOCH,CH,OH
①同系物要求结构相似、官能团种类数目相同,乙二醇是二元醇,乙醇是一元醇,不互为同系物,错误;
②乙二醇含多个亲水基羟基,能与水任意比互溶,正确:③ImolCH2=CH2充分燃烧消耗3molO2,1mol乙
二醇充分燃烧,消耗2.5mol02,耗氧量不同,错误故选②:
(6)乙醇分子量为46,该醇分子量为46+42=88,结合醇通式CnH2n+20,得n=5,为戊醇CH,OH,
戊醇的同分异构体分别是1.CH,CH,CH,CH,CH,OH(1-戊醇)2.CH,CH,CH,CH(OH)CH,(2-戊醇)3.
CH,CH,CH(OH)CH,CH3(3-戊醇)4.(CH3)2CHCH,CH2OH(3-甲基-1-丁醇)5.
CH,CHCH(CH3)CH,OH(2-甲基-1-丁醇)6.(CH3)2C(OHCH,CH(2-甲基-2-丁醇)7.
(CH3)2CHCH(OH)CH3(3-甲基-2-丁醇)8.(CH3)3CCH,OH(2,2-二甲基-1-丙醇),共8种;催化氧化要求
羟基所连碳上有氢,不能催化氧化的是羟基连在叔碳(无氢)的结构,即(CH,),C(OH)CHCH3。
第7页共7页
资源预览图

1

2

3
4
相关资源
由于学科网是一个信息分享及获取的平台,不确保部分用户上传资料的 来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系学科网,我们核实后将及时进行处理。