山东济宁市第一中学2025-2026学年高一下学期期中考试 化学试题
2026-05-15
|
3份
|
11页
|
72人阅读
|
20人下载
资源信息
| 学段 | 高中 |
|---|---|
| 学科 | 化学 |
| 教材版本 | - |
| 年级 | 高一 |
| 章节 | - |
| 类型 | 试卷 |
| 知识点 | - |
| 使用场景 | 同步教学-期中 |
| 学年 | 2026-2027 |
| 地区(省份) | 山东省 |
| 地区(市) | 济宁市 |
| 地区(区县) | - |
| 文件格式 | ZIP |
| 文件大小 | 1.78 MB |
| 发布时间 | 2026-05-15 |
| 更新时间 | 2026-05-16 |
| 作者 | 匿名 |
| 品牌系列 | - |
| 审核时间 | 2026-05-11 |
| 下载链接 | https://m.zxxk.com/soft/57808895.html |
| 价格 | 0.50储值(1储值=1元) |
| 来源 | 学科网 |
内容正文:
高一化学试题答案
一、
选择题(1-10每题2分。11-20每题3分)
1
2
3
4
5
6
7
8
10
12
13
14
15
16
17
18
19
20
D
A
B
C
A
B
O
B
D
B
B
D
A
B
O
B
C高一化学
注意事项:
1.答题前,考生先将自己的姓名、考生号、座号填写在相应位置,认真核对条形码上的姓名、考生号
和座号,并将条形码粘贴在指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。
3.回答非选择题时,必须使用0.5毫米黑色签字笔书写,按照题号在各题目的答题区域内作答,超
出答题区域书写的答案无效:在草稿纸,试题卷上答题无效。保持卡面清洁,不折叠,不破损。
可能用到的原子量:H1C12N14016A127Cu64Zn65
一、选择题(本题共20小题,1到10每小题2分,11到20每小题3分,共50分。每小题只有一个选项符合题意)
1.我国正处于迈向科技强国的关键阶段。下列关于科技成果的描述正确的是
A.用于医学领域的3D打印生物陶瓷支架属于传统无机非金属材料
B.C919国产大飞机所用复合材料外壳属于纯金属材料
C.沉陷区光伏项目的太阳能电池板使用的材料主要是二氧化硅
D.航天防护服所用聚乙烯纤维属于合成有机高分子材料
2.下列化学用语或图示正确的是
A.乙炔的电子式:H:C:C:H
B.CCl4的空间填充模型:
C.乙烯的结构简式:CH,H,
D.钾离子的结构示意图:
3.实验室中下列做法正确的是
A.氢氟酸保存在棕色玻璃试剂瓶中
B.锂保存在装有石蜡的广口瓶中
C.烧碱溶液保存在玻璃塞试剂瓶中
D.浓硝酸保存在带橡胶塞的棕色细口瓶中
4.N。为阿伏加德罗常数的值。下列叙述正确的是
A.1 mol Fe溶于过量硝酸,转移电子的数目为2W4
B.标准状况下,2.24LS03中质子的数目为4W4
C.1molN2与4molH2反应生成NH3分子的数目小于2Na
D.14g乙烯与丙烯(CH-CH-CH)的混合物中原子总数目为1.5M
5.下列关于有机化合物的结构、性质及基本概念等知识的理解正确的是
A.分子式为C4H1o的烷烃,其一氯取代物共有4种
B.分子式为CH4和CH的烃一定属于同系物
C.氯乙烯(CH2=CHCI)是一种不饱和烃
D.CH,CH-C(CH3),所有原子都处在同一平面上
6.对下列有关装置的说法正确的是
1
Mg-
A
生铁
碳棒
MnO,糊
NH,CI糊
硫酸
锌筒
NaOH溶液PbO2(正极)
Pb(负极)
-稀硫酸
I
I
IV
A.装置I中镁为原电池的负极
B.装置Ⅱ在工作时正负极质量均增加
C.装置Ⅲ不能构成原电池
D.装置V工作时,锌筒作负极,发生还原反应,锌筒会变薄
7.关于工业制备高纯硅、硝酸和硫酸中,下列说法错误的是
A.工业制硝酸:H催化氧化生成N0的反应中,每消耗0.4molH3,转移2.0mol电子
B.工业制备的浓硝酸经常呈黄色,是因为溶有O2,可以加入适量O2除去
C工业制高纯硅第一步的主要反应:签0,+c高温s+C0,t
高温
D.工业制硫酸,煅烧黄铁矿的反应为:4FeS2+1102=2Fe,O3+8S02
8.元素及其化合物的转化关系是化学学习的重要内容之一,下列7组转化关系不能通过一步反应完成的组数为
①SiO2一→i(粗硅)→iHCl3→Si(高纯硅);
②Al→AlO3→Al(OH)3→A1Cl3;
③Si→SiO2→HSiO3→Na2Sio3
④N2→NH3→NO2→HNO3:
⑤Fe→Fe(SO43→Fe(OHD3→FeO3:
⑥S→S03→HS04→BaSO4;
⑦Na→NaOH→NaCIo→Cl2
A.5
B.4
C.3
D.2
9.实验室探究甲烷与氯气反应的装置如图。下列说法正确的是
条光源
CH4和Cl2
:E
饱和NaCI溶液
A.试管内混合气体颜色变浅,主要是因为氯气部分溶于饱和食盐水
B.试管壁出现了油状液滴,主要是因为该反应生成了一氯甲烷
C.若开始反应前试管中的甲烷和氯气的体积比为1:1,充分反应后试管内充满液体
D.若15g乙烷与足量氯气发生取代反应时,最多生成3N个HC1
10.下列离子方程式正确的是
A.漂白粉溶液中通入S02气体:Ca2++2ClO+S0,+H,O=CaS0,↓+2HC1O
B.向硫化钠溶液中通入足量二氧化硫:2S2-+5S0,+2H,0=3S↓+4HSO
2
C.铜溶于浓硝酸:3Cu+8+2NO3=3Cu2++4H2O+2NO↑
D.向NH,HCO3溶液中滴加足量稀NaOH溶液:HCO?+OH=H,O+CO
11.丙烯可发生如下转化,下列说法错误的是
Br
C.Hs Br
BrCH,-CH-CH.cCI.C
光照
C,H,Br2
X
Y
注:X能使酸性反应1
反应2
催化剂
KMO4溶液褪色
(C3H6)
Z
A.丙烯分子中最多7个原子共平面
B.X的结构简式为CHCH=CHBr
-CH2一CH
C.反应2的反应类型为加成反应
D.聚合物Z的链节为
CH:
12.在催化剂作用下由粗硅制备SiHCI的反应为Si(s)+3SiCl4(g)+2H2(g)=4sHCl(g)。一定温度下,在某容积
为2L的恒容密闭容器中发生上述反应,起始加入足量的Si(s)、0.3 mol SiCl4(g)和0.2molH2(g),l0min后反应
达到平衡,此时c(H2)=0.08molL1。下列说法正确的是
A.0~10min内,v(SiCl4)=0.18mol.L1.s
B.10min时,c(SiHCI3)=0.16mol.L-1
C.反应达到平衡时,SiC14(g)的转化率为10%
D.平衡时体系的压强与初始压强之为24:25
13.己知298K,101kPa时,CO2(g)+3H2(g)、一CHOH(g)+H2O(g)。该反应在密闭的刚性容器中进行,C02
的初始浓度相同,在不同温度和催化剂条件下,c(CO)-t关系如图所示。下列说法错误的是
A.若初始时cH):c(C0)=1:1,当C02体积分数不变时反应达到平衡
催化剂1
0.40
B.T2下,反应达到平衡时c(CH3OH=0.22mol/L
/催化剂2
C.T下,催化剂2的催化效果比催化剂1好
8
T2
催化剂3
D.其他条件不变,20min时,向容器中充入氦气反应速率不变
0
10
20 t/min
14.酸性MnO4溶液与H,C,O4(草酸,一种弱酸)溶液反应
过程中,含Mn粒子的浓度随时间变化如下图所示。下列说法
0.8
◆
Mn(VT⑩)
0.6
错误的是
0.4
o-Mn(⑩
Mn(II)
A.由图可知,M(II)能够氧化HC,O4
0.01088
。一。一年
1013152025
时间/min
B.0~13min,随着反应物浓度的减小,反应速率逐渐减小
3
C.0~13nin内的平均反应速率:y(MnOa)=7.7×106mol.L1.mim
D.总反应为5HC,04+2MnO4+6H+=2Mn2++10C02个+8H,O
15.绿水青山是习近平总书记构建美丽中国的伟大构想,某工厂拟综合处理含NH废水和工业废气(主要含N2、CO2、
SO2、NO、CO,不考虑其他成分),设计了如图流程,下列说法错误的是
A.固体1中主要含有CaCO3 CaSO3 Ca(OH),
NaNO
含NH废水
NaOH
溶液
过量
→气体
)X溶液
B.X可以是空气,但不能过量
工业石灰乳
废气
气体2
捕获剂无污染气体
C.捕获剂所捕获的气体主要是CO
固体1
捕获产物
D.处理含NH废水时,发生的反应为:2NH+2NO,=2N2个+3H,O+2H
16.用于处理废水(酸性)中的有机物及脱除硝态氨的微生物电池具有很好的发展前景,如图所示的电池说法正确的
是
负载
N
电极mCO
电极n
NO:
C6H1206二生
物
质子交换膜
A.电子由m极经导线到n极
B.生成1moIN2,则有10molH+通过质子交换膜移向m极室
C.m电极反应为2NO3+6H0+10e=N2+120H
D.若电路中有1mol电子通过,m极室质量减少1.6g
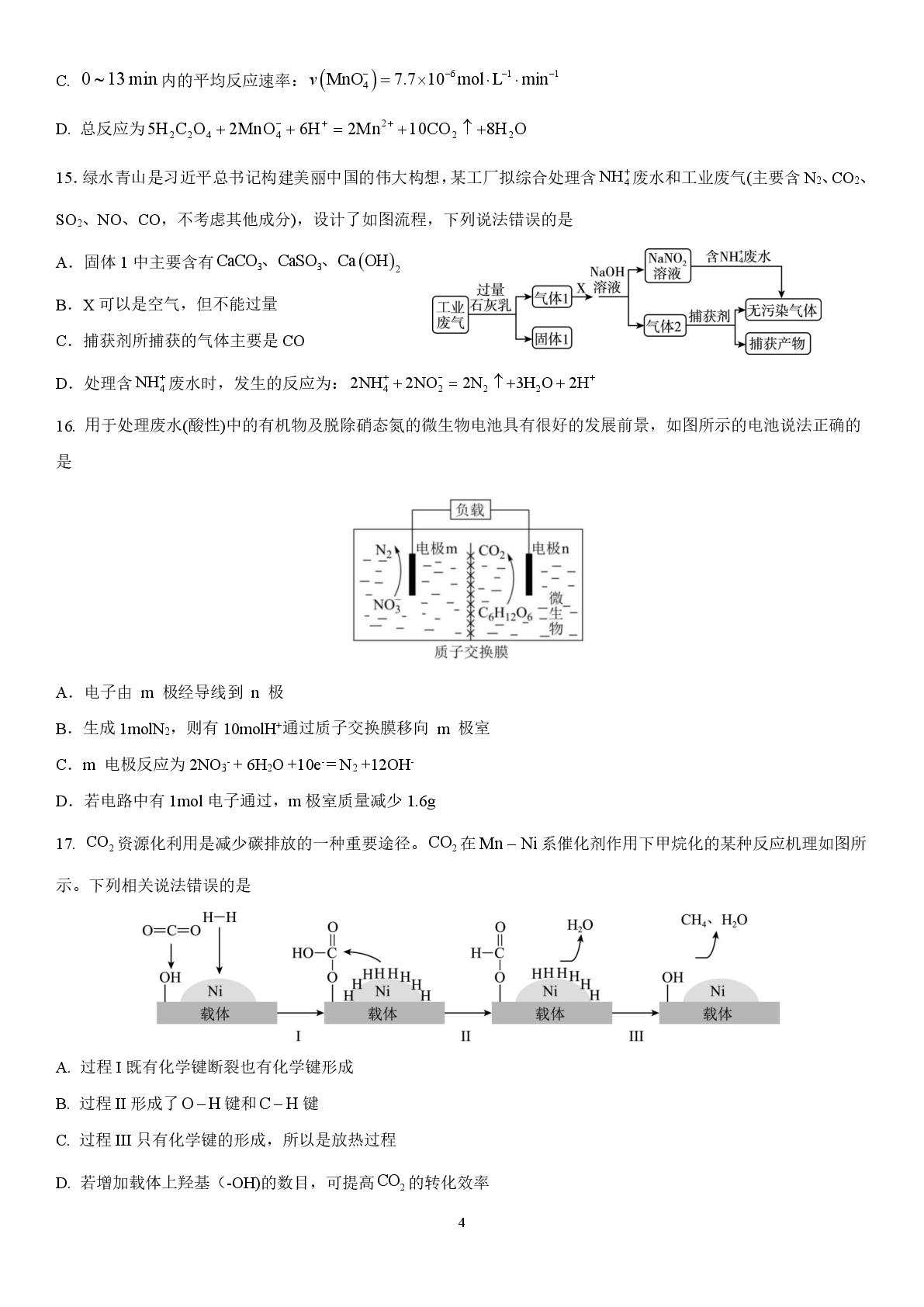
17.CO2资源化利用是减少碳排放的一种重要途径。CO,在Mn-Ni系催化剂作用下甲烷化的某种反应机理如图所
示。下列相关说法错误的是
H-H
CH4、HO
0=C=0
O
H,O
HO-C
H-C
OH
0
HHHE
OH
Ni
Ni
Ni
H
Ni
载体
载体
载体
载体
分
A.过程I既有化学键断裂也有化学键形成
B.过程IⅡ形成了O-H键和C-H键
C.过程IⅡ只有化学键的形成,所以是放热过程
D.若增加载体上羟基(-OD的数目,可提高CO2的转化效率
4
18.下列实验方案能达到实验目的的是
选项
实验目的
实验方案
A
证明:金属性Fe>Cu
把Cu电极和Fe电极用导线相连后插入浓硝酸,Fe电极表面有气泡产生
向装有X溶液的试管中滴入稀NaOH溶液,取一张湿润的红色石蕊试纸
B
检验X溶液中有无N4
置于试管口,观察试纸是否变蓝
验证Fe+与I反应是否
取2mL0.0lmol.L-1KI溶液和1nL0.01mol.L1FeCL溶液充分反应,再
存在限度
加入几滴KSCN溶液,观察溶液是否变红
D
氧化性:H,O2>Fe3+
向硫酸酸化的HO,溶液中滴入Fe(NO)2,溶液变黄
19.
为探究Ag$O3能否溶于硝酸,某实验小组进行如下实验。下列说法错误的是
1mL 0.1mol-L
0.04mL浓HNO3
NaSO,溶液
混合后cHNO)=0.3molL
②略有浑浊
③沉淀溶解
(需仔细观察)
①1mL0.1molL
AgNO,溶液
1mL 0.1mol-L!
0.04mL浓HNO
将沉淀滤出,洗净
Na,SO,溶液
混合后c(HNO=0.3moL
i加入浓硝酸
加入BaCl溶液
④产生白色沉淀
⑤沉淀无变化
i.沉淀溶解,产生红棕
色气体;i产生白色沉淀
A.由②③知少量的Ag2SO4能溶于稀硝酸
B.④中白色沉淀为AgSO4
C.⑥中沉淀溶解发生反应:AgSO3+2HNO3(浓)=Ag2SO4+2NO↑+HO
D.上述实验表明AgSO3能否溶于硝酸与硝酸的浓度有关
20.将总质量为15.00g的铝铜合金粉末投入200mL稀硝酸和稀硫酸的混合溶液中,合金与混酸恰好反应完全(设
反应中还原产物只有NO),此时溶质只有硫酸盐。向反应后的溶液中逐滴加入4mol·L1NaOH溶液,当沉淀质量
达到最大值时,消耗NaOH溶液的体积为300mL。下列说法正确的是
A.反应过程中转移电子的物质的量为0.6mol
B.产生的NO在标准状况下的体积为5.6L
C.原混酸中HSO4的物质的量浓度为3.0mol.L
D.若将合金中的铜换成等物质的量的锌,沉淀质量最大时消耗NaOH溶液的体积变小
二、非选择题(本大题共4小题,共50分)
21.(12分)有机化合物的组成、结构、性质及转化是学习有机化学的必备知识。
I图中显示的是几种烃中的碳原子相互结合的方式。
B
E
(1)上图中互为同分异构体的是
(填标号)。
(2)A的一氯代物有
种;A的同系物中最简单的有机物的空间构型为
Ⅱ石蜡是由分子中碳原子数为17~36的多种烷烃或环烷烃组成的混合物。A的产量被用作衡量一个国家石油化工
产业发展水平的标志,其相对分子质量为28。有关物质的转化关系如图所示。
加压
B
①H,0/催化剂,△,
一定条件
②H,Ni,△
石蜡
A
⑤催化剂,△
③HCV催化剂,△
④C以光照
E
D
(1)通过反应①可制乙醇,写出反应①的化学方程式
(2)写出反应④的化学方程式
,该反应类型为
(3E为高分子化合物,请写出E的结构简式
(4)下列说法正确的是
A.反应②和反应③的反应类型相同
B.A和C均能与酸性高锰酸钾溶液反应
C.物质D中存在离子键和共价键
D.等物质的量的A和C充分燃烧,C消耗O2的量更多
22.(13分)能量、速率与限度是认识和研究化学反应的重要视角。
I.化学反应在发生物质变化的同时伴随有能量变化,是人类获取能量的重要途径
太阳能
2H,0
H,个+02个,根据下表数据回答:
TiO,
化学键
H-H
0=0
H-O
键能(kJ·molr)
436
496
463
当2 mol H,O(g)完全分解时需
(填“放出或吸收”)能量
kJ。
IⅡ.一定条件下铁可以和CO2发生反应:Fe(S)+CO2g)≥FO()+CO(g)。一定温度下,向某密闭容器中加入足量
6
铁粉并充入一定量的CO2气体,反应过程中CO,气体和C0气体的浓度与时间的关系如图所示。
(1)tmin时,正、逆反应速率的大小关系为y正y逆填><'或=)。
个cmo/L)
0.7
CO
(2)反应达到平衡状态时,C0的体积分数为
%(保留1位小数)
0.5
(3)下列描述能说明上述反应已达到平衡状态的是
(填选项字母)。
CO
0.2
A.(C02(CO)
0
4
t/min
B.容器中气体压强不随时间变化而变化
C.单位时间内生成nmolCO2的同时也生成molCO
D.容器中气体的平均相对分子质量不随时间变化而变化
Ⅲ人们应用原电池原理设计如图所示装置,消除氮的化合物的污染,使其转化为
负载
NH,
NO
无毒物质,同时充分利用化学能。
电极A
电极B
(1)为了让电池持续工作,交换膜为
(填“阴”或“阳”)离子交换膜。
(2)电极B上发生的电极反应式为
KOH
溶液
K
(3)放电时,当A电极生成11.2L(标况下)气体时,通过交换膜的离子的物质
溶液
交换膜
的量为
(4)电池工作一段时间后,负极区溶液中c(OH)
(填“增大”、“减小”或“不变”)。
23.(13分)学习小组探究了如下反应。回答下列问题:
I铜与浓硝酸反应的装置如图所示,装置B的作用为
写出C中吸收NO2的离子方程式
浓硝酸
铜片一
NaOH溶液
A
Ⅱ实验室通过如图所示装置甲制取乙烯,该学习小组发现实验过程中圆底烧瓶内的液体颜色变黑,查阅资料表明,
装置甲产生的气体不只有乙烯,还有S02、C02。请写出S02通入装置乙中发生反应的离子方程式
。若装置丙中有白色沉淀出现能说明装置甲产生C02吗?
(填“能”或“不能”),
请说明理由
温度计
乙醇和
浓硫酸
接足量澄清石灰水
装置甲
/装置乙装置丙
足量酸性KMnO:溶液
.(1)铜与过量H,O2反应的探究如下:
+Na2SO,溶液
①
>无明显现象
过量30%H202
②
→铜片溶解,溶液变蓝,少量无色气体产生
铜片
+稀H2SO4
实验②中Cu溶解的离子方程式为
:产生的气体为
。比较
实验①和②,从氧化还原角度说明H+的作用是
(2)用足量NaOH溶液处理实验②新制的溶液得到沉淀CuO2。设计如下方案测定CuO2含量:取含CuO2粗品0.1000
g(杂质不参加反应)与过量的酸性KI完全反应后,调节溶液至弱酸性。以淀粉为指示剂,用0.1000 mol.L'Na,S,O,标
准溶液滴定,滴定终点时消耗NaS,O3标准溶液25.00mL。
已知:2Cu02+8I-+8H+=2CIl+3I2+4H0,I2+2S,O}=2I+S4O
则粗品中CO2的质量百分含量为
24.(12分)某工厂采用如下工艺处理镍钴矿硫酸浸取液(含Ni+、Co2+、Fe2+、Fe、Mg2+和Mm2+),实现镍、钴、
镁元素的回收。
混合气
石灰乳(S02+空气)
NaOH
NaOH
滤液
滤液
硫酸浸取液
氧化
沉钴镍
沉镁→上层清液
滤渣
钴镍渣
沉渣
(1)用硫酸浸取镍钴矿时,提高浸取速率的方法为
(填字母)。
a.将镍钴矿粉碎b.适当升高温度c.将稀硫酸换成浓硫酸d.延长浸取时间
(2沙“氧化操作中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸H,$O),HS05中不同价态氧原
子的数目之比为
0
(3)氧化”操作中,用石灰乳调节pH=4,Mn+被HS0,氧化为MnO2,该反应的离子方程式为(HSO,的电
离第一步完全,第二步微):滤渣的成分为MO,、
(填化学式)。
(4)氧化”操作中保持空气通入速率不变,随着$O2体积分数的增大M+氧化速率呈现先增大后减小的趋势。分析当
继续增大s02体积分数时,+氧化速率减小的原因是
(5)沉钴镍中得到的Co(OHD2在空气中850℃煅烧可获取C03O4,该反应的化学方程式为
(6)沉镁”中检验Mg2+是否沉淀完全的实验操作可以为
8■
高一化学答题卡
姓名:
考场:
座号:
贴条形码区
班级:
考号:
1.答题前,考h请先将姓名、准考证号填号清楚,并认真核对考试科目;如有条形码请在规定位置贴好。
注意
?.选择题必须使用2B铅笔填涂:非选择请使用0,5毫米黑色签字笔书写,要求字体工整、笔迹清楚。
事项
3.请严格按照题号在响应的答题区域内作答,超出答题区域的答案无效;在草萄纸、试题卷上答题无效。
4保持卷面清洁、不要装订、不要折叠、不要破损。5正确填涂:☐错误填涂:√一ㄧ⊙
选择题(共20题,满分50分,1到10每小题2分,11到20每小题3分)
1.
[A][B][c][D]
6.[A][B][c][D]11.[A][B][c][D]
16.[A][B][c][D]
2.[A][B][C][D]
7.[A][B][C][D]12.[A][B][c][D]
17.[A][B][C][D]
3.[A][B][c][D]
8.[A][B][c][D]13.[A][B][c][D]
18.[A][B][c][D]
4.[A][B][C][D]
9.[A][B][C][D]14.[A][B][C][D]
19.[A][B][C][D]
5.[A][B][c][D]
10.[A][B][c1[D]15.[A][B][C][D]
20.[A][B][C][D]
二、
填空题(四个大题,共50分)
21.(12分)
I.(1)
(1分)
(2)
(2分)
(1分)
Ⅱ.(1)
(2分)
(2)
(2分)
(1分)
(3)
(1分)(4)
(2分)
22.(13分)
(1分)
(2分)
Ⅱ.(1)
(1分)
(2)
(1分)
(3)
(2分)
Ⅲ.(1)
(1分)
(2)
(2分)
(3)
(2分)
(4)
(1分)
-1
■
■
■
23.(13分)
(1分)
(2分)
I.
(2分)
(1分)
(1分)
正.(1)
(2分)
(1分)
(1分)
(2)
(2分)
24.(12分)
(1)
(1分)
(2)
(2分)
(3)
(2分)
(2分)
(4)
(1分)
(5)
(2分)
(6)
(2分)
a
-2
a
资源预览图

1

2

3
4
相关资源
由于学科网是一个信息分享及获取的平台,不确保部分用户上传资料的 来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系学科网,我们核实后将及时进行处理。