湖北襄阳市2026届高三上学期期末考试 化学试卷
2026-02-07
|
2份
|
9页
|
935人阅读
|
13人下载
资源信息
| 学段 | 高中 |
|---|---|
| 学科 | 化学 |
| 教材版本 | - |
| 年级 | 高三 |
| 章节 | - |
| 类型 | 试卷 |
| 知识点 | - |
| 使用场景 | 同步教学-期末 |
| 学年 | 2026-2027 |
| 地区(省份) | 湖北省 |
| 地区(市) | 襄阳市 |
| 地区(区县) | - |
| 文件格式 | ZIP |
| 文件大小 | 2.15 MB |
| 发布时间 | 2026-02-07 |
| 更新时间 | 2026-02-07 |
| 作者 | 匿名 |
| 品牌系列 | - |
| 审核时间 | 2026-02-07 |
| 下载链接 | https://m.zxxk.com/soft/56379921.html |
| 价格 | 1.00储值(1储值=1元) |
| 来源 | 学科网 |
内容正文:
2026届高三上学期期末考试
高三化学参考答案
题号
1
2
3
4
5
6
8
9
10
11
12
13
14
15
答案
B
A
D
C
A
D
A
B
D
C
D
B
B
16、除标注外,每空2分,共13分
(1)①2H0+2+S02=S0?+4H+2I(1分)
②B(1分)
(2)①-90.2kJ小mo1'(1分)
低温(1分)
②CH0(1分)
D
③反应i为放热反应,反应ⅱ为吸热反应,在其他条件不变时,升高温度,反应ⅱ正向移动的程度大
于反应i逆向移动的程度,导致CO2的平衡转化率逐渐升高
0.117
9
①2 2(kPa)
17、除标注外,每空2分,共14分
(1)3d(1分)
(2)FeV,04+2Cl,加压.格楼FeCb+2V0,C
(3)SiO2(1分)硝酸被还原时会生成NO、NO2等有毒气体,污染环境
(4)Fe3*具有催化作用,会加速H202的分解
(5)NH+3Fe3*+2SO+6H2O=NH4Fe3(SO4)2(OH)61+6H*
(6)V205+4OH=V204+2H20
(7)V,05+5C+N,商2N+5C0
18、除标注外,每空2分,共14分
(1)BC
(2)①盐酸浓度低
40mL4mol-LI
②大于
③向U形管左侧滴加浓硫酸至c(H)≥7moL1
MnO2氧化盐酸的反应中,HCI的还原性与c(H)无关(1分):
MnO2的氧化性与c(H)有关,c(H)越大,MnO2的氧化性越强(1分)
19、每空2分,共14分
(1)1一氨基一2一丙醇
(2)加成反应
(3)保护酚羟基
CH.COO
(4)CH.coo
(5)CH3CH(OH)CH2CI+2NH3-CH3CH(OH)CH2NH2+NH4CI
COCN
COCN
OCOOCN
OCOOCN
(6)4
(提示:
H.CO.
OCH:
H.C
CH:
H,CO
OCH
H.O
CH
CH.COO
NH
(7)
CH.COO
OH
第1页共1页2026届高三上学期期末考试
化学试卷
注意事项:
1.答题前,先将自己的姓名、准考证号、考场号、座位号填写在试卷和答题卡上,并将准考证号条
形码粘贴在答题卡上的指定位置。
2.请按题号顺序在答题卡上各题目的答题区域内作答,写在试卷、草稿纸和答题卡上的非答题区域
均无效。
3.选择题用2B铅笔在答题卡上把对应题目所选答案的标号涂黑;非选择题用黑色签字笔直接答在答
题卡上对应的答题区域内。
4.考试结束后,请将本试卷和答题卡一并上交。
可能用到的相对原子质量:H1C12N14016Na23Mg24A127S32C135.5
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.化学之美,外美于现象,内美于原理。下列说法错误的是
A.制作泡菜时加入少量维生素C,维生素C可去除泡菜中的亚硝酸盐
B.晶莹剔透的六角形雪花完美对称,六角形雪花融化为吸热反应
C.通电时,液晶电视显示器中液晶的长轴取向发生改变,从而显示数字、文字或图像
D.缺角的硫酸铜晶体在饱和硫酸铜溶液中能变为完美的晶体
2.化学用语可以表达化学过程。下列化学用语表达错误的是
A.用电子式表示HC的形成过程:HC:→H[
B.用电子云轮廓图表示N2中2px一2px、2p一2pπ键的形成过程:
2p.2p
C.由1,6-己二胺和己二酸制备尼龙66:
nH2N(CH2)NH2+nHOOC(CH2)COOH
催化剂三HO
H+(2n-1)H0
D.“钠与水反应”实验有关图标:
3.常温下,BF3是一种无色液体,常用于核燃料生产和处理,遇水立即发生反应:
3BrF3+5H2O=HBrO3+Br2十9HF+O2↑
设N为阿伏加德罗常数的值。下列有关说法正确的是
A.在标准状况下,11.2LHF含电子数为5NA
B.0.1 mol HBrO3晶体含离子数目为0.2Na
C.1 mol BrF3中心原子的价层电子对数为4NA
D.该反应中氧化产物与还原产物的物质的量之比为2:1
4.宏观辨识与微观探析是化学学科核心素养之一。下列离子方程式的书写正确的是
A.H180中投入Na2O2固体:2H180+2Na2O2=4Na+4OH+1802↑
B.向Ca(ClO)2溶液中通入少量SO2:SO2+H20+Ca2++C1O=CaSO4+2H+C1
C.向HPO2(次磷酸,一元弱酸)溶液中滴入足量的NaOH溶液:HPO2十OH一HPO2+H20
D.用浓盐酸酸化的KMnO4溶液与HO2反应,证明HO2具有还原性:
2Mn04+6H+5H202=2Mn2++502↑+8H0
高三化学第1页共8页
5.高分子材料Q的合成路线如图所示,下列说法正确的是
HC≡CH
CH,COOH,X催化剂,
H,△
A.制备Q时消耗W与Y的物质的量之比为2:nB.生成X的反应为取代反应
C.物质Y为CH;CH2OH
D.Z在水中的溶解度大于W
6.
下列方案设计、现象和结论都正确的是
选项
目的
方案设计
现象和结论
Y
比较HC1O和醋酸
用pH试纸测定等浓度的NaCIo溶
pH:NaClo溶液>CH3COONa,
的酸性强弱
液、CH3COONa溶液的pH
CH3COOH的酸性强
B
比较Kp(AgCI)和
向同浓度NaCl、Nal混合溶液中滴入
有黄色沉淀生成,Ks即(AgCI)<
Ksp(Ag)的大小
少量AgNO3溶液
K'sp(AgI)
探究铁粉脱氧剂中
将脱氧剂样品溶于盐酸,滴加KSCN
若溶液没变红,说明铁粉脱氧剂
是否有Fe3
溶液
中没有Fe3+
试管1:2mL0.001 mol-L FeCl3:溶液
探究反应物的浓度
+2mL0.003 nol.LKSCN溶液
试管2中红色更深,增大反应物
D
对化学平衡的影响
试管2:2mL0.001 mol-LFeCl3溶液
浓度,化学平衡正向移动
+2mL0.006 mol.L KSCN溶液
7
结构决定性质,性质决定用途。下列事实解释错误的是
选项
结构或性质
解释
A
硬度:金刚石>石墨
石墨中碳碳键键能小于金刚石中碳碳键键能
B
键角:NO,>NH
中心原子杂化方式不同
C
O3的溶解度:CCl4>HO
O3的极性仅是H20的极性的28%
D
酸性:K2(邻羟基苯甲酸)<Ka(苯酚)
邻羟基苯甲酸根离子能形成分子内氢键
8.某配离子是一种常用的有机催化剂,其结构如图所示。X、Y、Z、M、Q为五种原子序数依次增大的
前四周期元素;Y、Z、M同周期,Y元素是形成化合物种类数最多的元素;基态Q原子的价电子数
等于基态Y原子与基态M原子的价电子数之和。下列说法正确的是
A.M的第一电离能和电负性均是同周期中最大的
YM.
YM
12
B.Q的最高价氧化物对应的水化物可溶于某些酸和碱
C.元素Y、Z的简单氢化物分子的VSEPR模型、中心原子的杂化方
X】
式和分子的空间结构均完全不相同
D.简单氢化物的沸点:Z>M,是因为前者简单氢化物形成的分子间
YM:
YM
氢键强于后者的
9.瓜环是继冠醚、环糊精、杯芳烃之后的新一代有机大环主体分子,由2n个亚甲基桥联n个苷脲单体(=5,
6,7,8.)构成的笼状化合物,具有分子识别功能。具体合成路线和不同大小形状的瓜环形状结构
如图所示。
0
BrBr
NH2 NH2
c=aH股-装H-H
CH,O-C一OCH,HN NH HCHO/催化剂
H
取代
成环
BrBr
HN、NH
缩合
NH2 NH2
n
(a)
(b)
d
高三化学第2页共8页
下列说法错误的是
A.不同瓜环识别的分子或金属离子不同,且与识别的分子间一般不形成化学键
B.一定条件下,苷脲既能与盐酸反应又能与NaOH溶液反应
C.由苷脲单体缩合形成1mol瓜环[7]时生成14molH20
D.瓜环都属于有机高分子
10.已知A、B、C、D、E、F、G、H、X、Y是中学化学常见物质,其中A是一种活泼金属,D是一种
黑色非金属固体单质,且除A、D外,其余物质均为化合物:E、F、H、X、Y中含有同种元素,F
是一种红棕色气体。它们之间在一定条件下存在下列转化关系:
④
8
A
B
点燃
E
F
E
☒
3
B
D②
回
g
己知:反应④中物质A、E以物质的量之比n(A):n(E)=2:5反应,且生成物X、Y均属于盐类
下列叙述正确的是
A.物质B、F、H均是大气污染物,且均能形成酸雨
B.反应②中每转移2mole,标准状况下产生的还原产物与氧化产物的体积差为33.6L
C.反应②、④中物质E表现的化学性质不完全相同
D.若在反应④所得溶液中加入过量NaOH浓溶液且加热时,会观察到有白色沉淀生成,并产生使蓝
色石蕊试纸变红气体
11.MFC一EF耦合装置是微生物燃料电池(MFC)与电芬顿(EF)技术结合的难降解有机物(如丙烯腈,能降
解为CO2、N2和HO)废水处理系统,核心是“产电十高级氧化降解”协同工作。“PS”代表产生自由
基需要电解活化,但该装置中是用MFC自身的产电替代了外加电源,实现了“无外加电源的电解活
化”。其工作原理如下所示:
PS
HO
电
CO
离
有机物
X
空气
Fe
换
CHO
膜
H,O,
Fe
下列说法正确的是
A.若处理0.1ol丙烯腈,理论上需要补充空气42L(标准状况下,假设空气中氧气的体积分数为20%
B.装置工作过程中存在反应:2Fe2++HO2+2H一2Fe3++H20+OH
C.离子交换膜为质子交换膜,H从左侧电极室迁移到右侧电极室
D.装置工作时,装置内温度越高,处理废水的效率越高
12.四碘合汞酸银(Ag2HgL4)是一种热致变色材料,存在两种晶体结构分别为a一Ag2Hgl4、B一Ag2Hg4。低
温下AgHg4以B型结构存在,其晶胞结构如图,I厂以面心立方结构密堆积,A原子分数坐标为(0,0,0),
B-Ag2Hgl4升温至50.7C转变为a-Ag2HgL4,a、B两者结构相似,区别是a-Ag2HgL4中Ag和Hg2*如
图形式随机占据四面体空隙。a一AgHg4晶体可以导电,而且导电粒子几乎全是Ag,a、B间晶体结
构的转变也导致性质的一些变化,如颜色、导电性等。若将晶胞中各粒子看作刚性球体。下列说法错
误的是
投影:
B-Ag,Hgl,
a-Ag,Hgl
高三化学第3页共8页
相关离子半径I「:261pm、Ag:115pm、Hg2*:102pm;√3≈1.732)
115
A.B-Agstigi品胞结构中Hg分数坐标为(}人2g
B.B-Ag2Hgl4晶胞中四面体空隙填充率为37.5%
C.a一Ag2HgI4晶体导电时导电粒子几乎全为Ag是因为Ag比Hg带电荷数少,与阴离子间作用力
弱,且四面体侧面的空隙半径(空隙内切圆半径)大于Ag半径
D.B一Ag2Hg4晶胞沿y轴方向晶胞投影如上图所示
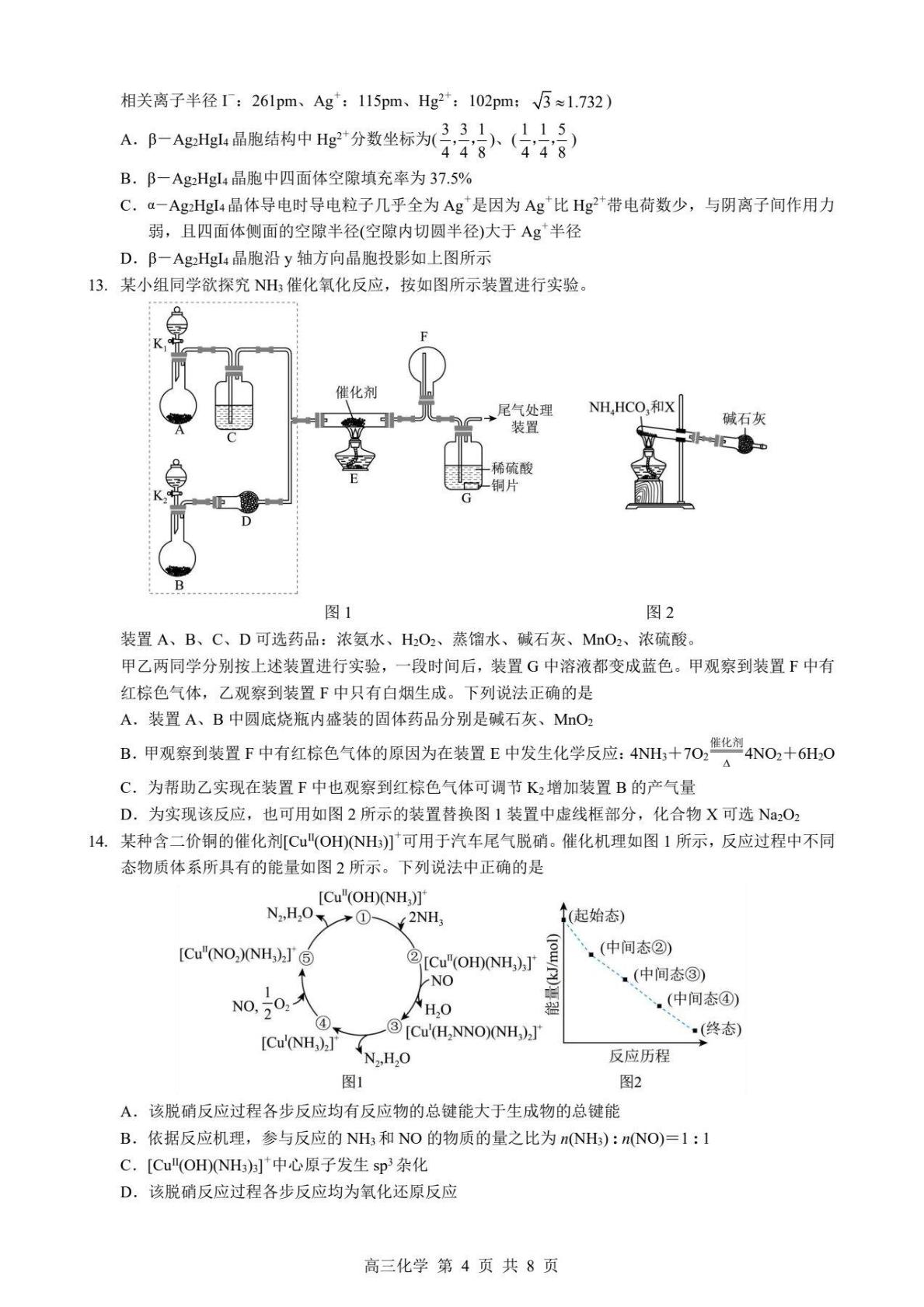
13.某小组同学欲探究NH催化氧化反应,按如图所示装置进行实验。
催化剂
尾气处理
NH,HCO,和X
装置
碱石灰
稀硫酸
铜片
G
图1
图2
装置A、B、C、D可选药品:浓氨水、HO2、蒸馏水、碱石灰、MO2、浓硫酸。
甲乙两同学分别按上述装置进行实验,一段时间后,装置G中溶液都变成蓝色。甲观察到装置F中有
红棕色气体,乙观察到装置F中只有白烟生成。下列说法正确的是
A.装置A、B中圆底烧瓶内盛装的固体药品分别是碱石灰、MnO2
B.甲观察到装置F中有红棕色气体的原因为在装置E中发生化学反应:4N+70,失40+6H0
C.为帮助乙实现在装置F中也观察到红棕色气体可调节K2增加装置B的产气量
D.为实现该反应,也可用如图2所示的装置替换图1装置中虚线框部分,化合物X可选N2O,
14.某种含二价铜的催化剂[C"(OHNH)]可用于汽车尾气脱硝。催化机理如图1所示,反应过程中不同
态物质体系所具有的能量如图2所示。下列说法中正确的是
[Cu"(OH)(NH)]
NH,0→①2NH,
1(起始态)
[Cu"NO,)NH,J'⑤
②[Cu"(oHNH,
.(中间态②)
NO
.(中间态③)
N0,20
H,0
.(中间态④)
④
③[Cu'H,NNO)NH,h
(终态)
[Cu'(NH)2]'
AN HO
反应历程
图1
图2
A.该脱硝反应过程各步反应均有反应物的总键能大于生成物的总键能
B.依据反应机理,参与反应的NH3和NO的物质的量之比为nNH):nNO)=1:1
C.[Cu(OH)NH)中心原子发生sp3杂化
D.该脱硝反应过程各步反应均为氧化还原反应
高三化学第4页共8页
15.25℃下,保持溶液中c(HF)=0.1molL1恒定,通过调节pH使Pb2、Ba2+
pX
形成氟化物而分离,体系中pH与pX(X表示F、Pb+、Ba2)的关系如图
6
(3.25.4)
(4.2.5.7)
所示。已知:[pX=-lg[c(X)/(molL)];Ksp(BaF2)>Ksp(PbF2)。下列叙述
5
错误的是
②
A.线③表示pH与p(Pb)的关系
B.25C时,反应BaF2(s)+Pb2(aq)PbF2(s)+Ba2(aq)的平衡常数K=102-7
C.25℃时,K(HF)=1032
D.线①与线②的交点的pH为2.3
PH
二、非选择题:本题共4小题,共55分。
16.(13分)
研究碳、氮、硫元素化合物的性质及其相互转化对建设生态文明、美丽中国具有重要意义。请回答下
列问题:
(1)已知I厂可以催化二氧化硫在水溶液中发生歧化反应:3SO2(g)+2HO①一2HSO4(aq)+S(s)△H
<0。催化原理分为两步:
第一步:S02+4I+4H=2H0+S+22△H>0慢反应
第二步:2H20+2十
+2IT△H<0快反应
①请完整写出第二步反应的离子方程式
50
②能正确表示I催化S02歧化反应原理的能量变化示意图为
(填字母)
能量
能量
能量
能量
反应进程
反应进程
反应进程
反应进程
A
B
C
(2)一种以CO2为碳源,在催化剂作用下催化加氢制备可再生能源甲醇的反应如下:
反应i:CO2(g)+3H2(g)、广CH3OH(g)+HO(g)△H1=-49.1 kJ-mol厂1
反应i:CO2(g)+H(g)—CO(g)十HO(g)
△H2=+41.1 kJ-mol1
①试计算反应ii:CO(g)+2H(g)、一CHOH(g)
△H3=
该反应能自发进行的条件为
(填“高温”“低温”或“任何温度”)。
②反应ⅰ在某非金属催化剂催化下的反应历程如下图所示,容易得到的副产物有C0和CH2O,其中相
对较少的副产物为;上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中(填
字母)的能量变化。
0.95
2.73
CO
CHO
0.45
CH.OH
0.28
1.12/
器
136CO
*CH.OH
器
-1.38
*CO十*H,O
-1.11
0.58
*C020.28
*0CH0.60月
*OCH.
*CO+*OH
*OCH,
反应历程
A.*OCH3→*CH3OH
B.*CO→*OCH
C.*OCH2→*OCH3
D.*C0十*OH→*C0十*H2O
③往某一恒容密闭容器中按投料比n(CO2):n(H)=1:3充入4mol反应物,在合适催化剂作用下发生
反应ⅰ和反应i,CO2的平衡转化率和甲醇的选择性如图所示。随着温度的升高,ABC所在曲线逐渐升高
的原因是
。在513K达平衡时,甲醇的物质的量为
mol(计算结果保留三位有效数字)。
[已知:甲醇的选择性=转化为甲醇的CO)】
n(参加反应的CO2)
高三化学第5页共8页
24
D(473,86
C(553.21)90
20f
E(513,78)
80
18
16f
14F
B(513,15)
12
A(473,13.2)
E(553.,60)
60
10
460
480
500520540560
温度K
④恒温恒压密闭容器中,加入2molC02和4molH2,同时发生反应i、i和i。初始压强为PokPa,在
300C发生反应,反应达平衡时,C02的转化率为50%,甲醇的选择性为75%。反应i的平衡常数K,一一
(K,为以分压表示的平衡常数,分压=总压×物质的量分数)。
17.(14分)
稀有金属钒和钛在钢铁、化工、航空航天等领域应用广泛。一种利用钒钛磁铁矿精矿[主要成分为F3O4、
F®V2O4(V为十3价)、TiO2和SiO2]综合提取钒、钛,并同步制备黄铵铁矾的工艺流程如下图所示:
有机萃
酸化的
Na2CO,溶液
NHCI
盐酸
适量Fe粉HO2
取剂RN
Na,SOa溶液
有机相「
反萃取
一系列操作.,V,05
钒钛
加
有机相
磁铁矿
洗涤
精矿
焙烧一酸浸→沉钛一氧化一一萃取
沉铁
黄铵铁钒
水相
NHaFe:(SO4)2(OH)6
NH,
浸出渣TiO(OH)2
废液相
(NH3)2SO4
己知:
①“加压焙烧”过程中存在反应2FeCl3(S)=2FCl(s)十C(g),生成的Cl2会对钒钛磁铁矿精矿“二
次氯化”:
②“酸浸”所得溶液中钒、钛以VO、TO形式存在。
③“萃取”时,VO先转化为H2V1oO再与萃取剂RN结合,其过程可表示为:
4R3N+4H*+H2V10=[R3NH]4H2V100286
回答下列问题:
(1)在离子化合物FeV2O4中,Fe存在形式的价电子排布式为
(2)“加压焙烧”中FeV2O4经“二次氯化”转化为VO2Cl和FeCl2的化学方程式为
(3)“酸浸”时,产生的“浸出渣”的主要成分为
(填化学式)。
“酸浸”时,若用硝酸代替盐酸,弊端有:
①硝酸有强氧化性,会将Fe+氧化Fe3,导致下一工序会额外消耗更多的铁粉:
②
(4)“氧化”时,H202的使用量远大于理论计算量,可能的原因为
(5)“沉铁”时,生成黄铵铁矾的离子方程式为
(6)V2O5可溶于强酸强碱,常温时不同pH、不同钒元素浓度时,十5价V存在形态如图所示(忽略溶
液前后体积变化):
0
V,0月
VO
V.O
2
3
HVO
H:VO
14
12
10
8
6
pH
高三化学第6页共8页
常温下,将0.01molV2O5溶解在200mL烧碱溶液中,剩余溶液的c(OH)=0.01moL1,则该反应
的离子方程式为
(7)V2O5在氮气氛围中,用碳高温条件下还原氮化制备VN,还生成一种分子结构中存在配位键的气
体,则该反应的化学方程式为
18.(14分)
氯气是一种重要的化工原料,在生产生活中有着重要的应用。请回答下列问题:
(一)实验室利用以下装置进行相关实验。
(1)其中难以达到预期目的的是
干燥的
气体
尾气吸收
尾气
饱和
浓硫酸
食盐水
NaOH (aq)
鲜花
A.净化、干燥C2
B.收集C
C.验证Cl,的漂白性
D.吸收尾气C
(二)探究盐酸与MnO2的反应。
(2)实验用4moL1的盐酸与一定量的MnO2反应时,没有产生明显实验现象。小组同学猜测可能原
因是:
猜想1:反应温度低
猜想2:
…
①上述猜想2为
请完成如下实验设计并证明上述猜想是否成立。
可选药品:4molL1盐酸、7moL1盐酸、MnO2、4 mol-L NaOH溶液。
序号
试剂
反应温度
现象
40mL4molL1盐酸、一药匙MnO2
65℃
无明显现象
女
盐酸、一药匙MnO2
80℃
无明显现象
Ⅲ
盐酸、一药匙MnO2
65℃
产生黄绿色气体
表中实验Ⅱ所用试剂中盐酸的规格为
根据上述实验可知猜想
(填“1”或“2”)成立。
②实验I中无明显现象的原因可能是cH)或c(CI)较低,设计实验进行探究:
序号
试剂
反应温度
现象
IV
20mL8molL1盐酸、20mL2molL1硫酸、一药匙MnO2
65℃
无明显现象
V
20mL8moL1盐酸、20mL3molL1硫酸、
药匙MnO2
65C
产生黄绿色气体
VI
40mL4moL1盐酸、11.7 gNaCl固体、一药匙MnO2
65℃
无明显现象
VIl
40mL4moL1盐酸、14.04gNaC1固体、一药匙MnO2
65℃
产生黄绿色气体
由上述实验结果可知MnO2氧化盐酸的反应中,c(H)变化的影响
(填“大于”或“小于”)(C)
变化的影响。
高三化学第7页共8页
③为探究cH变化究竟是影响了MO2的氧化性还是影响了CI的还原性,用如图所示装置(A、B均
为石墨电极,恒温水浴加热装置省略)进行实验
序号
操作
现象
i
K闭合
指针向左偏转
向U形管右侧滴加浓硫酸至c(H)
MnO,
4mol-L-
ii
指针偏转幅度变化不大
≥7molL1
和水
盐酸
盐桥
ini
指针向左偏转幅度逐渐增大
实验ⅲ的操作为
将ⅱ、ⅱ与i作对比,分别可得出结论:
19.(14分)某研究小组按下列路线合成多巴胺单体Y(部分反应条件及试剂已简化)。
CH
HO
COOH
HO
(CH,CO,0*CHO。
A
B
g
CH.COO
NH
CHNO.
CH.COO
CH,=CH-CH
HCIO
O.CHCIONH.CH.CH(OHCH.NH.
G
OH
回
D
®
回
HO
(CH);N
KCO;
HO
CH OH
CHNOs
回
NO,
NH,
OH
已知:①
Fe
NaNO2
⊙(苯胺、苯酚易被氧化)
HCI
H20
R"X
2
R
(CH)NR、
请回答:
(1)化合物F的名称是
(2)化合物D→E的反应类型为
(3)化合物B→C是在B的氧原子上引入乙酰基(CHCO-),其目的是
(4)化合物1的结构简式」
(5)E+NH(足量)→F反应的化学方程式为
(6)同时符合下列条件的多巴胺单体Y的同分异构体有种。
①分子中只含有1个环,且为苯环
②分子结构中有氰基(一CN,无羟基、醛基和过氧键(一O一O一)
③H一NMR谱和R谱检测表明:分子中共有3种不同环境的氢原子
(7)化合物D→E的反应会生成E的位置异构的同分异构体E',若以E'代替E参与合成路线,则生成
物G的同分异构体G的结构简式为
高三化学第8页共8页
资源预览图

1

2

3
4
所属专辑
相关资源
由于学科网是一个信息分享及获取的平台,不确保部分用户上传资料的 来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系学科网,我们核实后将及时进行处理。
