(教师版)3 第一章 第2节 第I课时 元素周期肆-【创新教程】2025-2026学年高中化学必修第二册五维课堂同步复习(鲁科版)
2026-02-02
|
6页
|
20人阅读
|
0人下载
教辅
资源信息
| 学段 | 高中 |
|---|---|
| 学科 | 化学 |
| 教材版本 | 高中化学鲁科版必修第二册 |
| 年级 | 高一 |
| 章节 | 第2节 元素周期律和元素周期表 |
| 类型 | 教案-讲义 |
| 知识点 | - |
| 使用场景 | 同步教学-新授课 |
| 学年 | 2026-2027 |
| 地区(省份) | 全国 |
| 地区(市) | - |
| 地区(区县) | - |
| 文件格式 | |
| 文件大小 | 1.15 MB |
| 发布时间 | 2026-02-02 |
| 更新时间 | 2026-02-02 |
| 作者 | 山东鼎鑫书业有限公司 |
| 品牌系列 | 创新教程·高中五维课堂同步 |
| 审核时间 | 2026-02-02 |
| 下载链接 | https://m.zxxk.com/soft/56272947.html |
| 价格 | 3.00储值(1储值=1元) |
| 来源 | 学科网 |
内容正文:
第一章原子结构元素周期律
五维课堂型
第2节
元素周期律和元素周期表
第1课时
元素周期律
课程标准
核心素养
1.结合有关数据和实验认识原子
①宏观辨识与
能运用原子结构描述物质及其变化的过程,解释同类
结构、元素性质呈周期性变化的
微观探析
的不同物质性质变化的规律
规律,构建元素周期律
2.体会元素周期律(表)在学习元
素及其化合物知识及科学研究
②证据推理与
能从原子结构的相关数据上收集证据,从不同视角分
中的重要作用
模型认知
析元素性质的问题,推出合理的结论
教材梳理。探新知
对应学生讲义P8
[知识梳理]
2.元素性质的递变规律
一、原子序数
(1)元素原子半径的周期性变化。
1.概念:元素在元素周期表中的序号。
Li
厚Na
3
2.原子序数与原子结构的关系:原子序数=核电荷数
于半径
\Be
PC N O E
径
=质子数=核外电子数。
0
原子序数(2)
0
原子序数(z)
二、元素周期律
第2周期
第3周期
1.1~18号元素核外电子排布的变化规律(最外层电
规律:随着原子序数的递增,元素原子的半径呈现
由大到小的周期性变化
子排布)
(2)元素主要化合价的周期性变化。
原子序数
电子
最外层电子
以1~18号元素为例探究化合价的变化,图示
原子结构
(a的取值)
层数
数(x的取值)
如下:
1→2
1
1→2
化
、13×3只
低负化
0*1
170
3→10
1-→8
12345678910111213141516
2
22
深子数
22
3
4
规律:随着原子序数的递增,元素的最高正化合价
©
11→18
3
18
呈现十1→+7(O、F除外),最低负化合价呈现一4
一1的周期性变化。
三、元素周期律
随着原子序数的递增,元素原子的最外
1.内容:元素的性质随着原子序数的递增而呈周期性
结论
层电子排布呈现由1到8(第1周期为1
变化。
2.实质:元素性质的周期性变化是原子核外电子排布
到2)的周期性变化
周期性变化的必然结果。
·13·
世五维课堂
化学(LK)·必修第二册
重难突破。释疑惑
对应学生讲义P9
要点一化合价与最外层电字数之间的关系
要点二
微粒平径天小的比较
1.元素的主要化合价与最外层电子数的关系
1.原子
主族元素最高正化合价=最外层电子数(O、F除外)
(1)同一横行,从左到右,核电荷数依次增大,原子半
最低负化合价=最外层电子数一8。
径依次减小。如r(Na)>r(Mg)>r(Al)>
最高正化合价+最低负化合价|=8。
r(Si)>r(P)>r(S)>r(C1).
2.常见元素化合价的特点
(2)同一纵列,自上而下,电子层数依次增多,原子半
(1)氢元素:十1、-1、0价,如H2O、NaH、H2。
径依次增大。如r(Li)<r(Na)<r(K)<r(Rb)<
(2)氟元素:一1、0价,如NaF、F2,氟无正价。
r(Cs)。
(3)氧元素:-2、-1、0价,如CaO、NaO2、O2,氧无
2.离子
最高正价。
(1)同一纵列,自上而下,电子层数依次增多,离子半
(4)金属只有正价。
径依次增大。如r(Li)<r(Na)<r(K+)<
(5)非金属元素既有正价又有负价(O、F除外)。
r(Rb+)<r(Cs+)。
[易错提醒]元素化合价的“三个三”
(2)具有相同电子层结构的离子,随核电荷数的增大,
(1)二“特殊”:F无正价,O无最高正价。
(2)二“只有”:金属只有正价,只有非金属才有负价。
离子半径依次减小。如r(S2)>r(CI)>r(K+)
(3)二“等式”:对于主族元素,最高正价=最外层电
>r(Ca2+)。
子数,最低负价数值十最高正价数值|=8(除
3.同一元素的不同粒子:核外电子数越多,半径越大。
O、F外)
(1)阳离子:r(原子)>r(阳离子)。
O[典例示范]
如r(Na)>r(Na+)。
[典例1]下列各组元素中,按最高正价递增的顺序
(2)阴离子:r(原子)<r(阴离子)。
排列的是
如r(C1)<r(C1)。
A.C、N、O、F
B.K、Mg、C、S
(3)多种价态的离子:价态越高,半径越小。
C.H、He、Li、Be
D.P、S、Cl、Ar
r(Fe)>r(Fe2)r(Fe).
解析:B[根据元素的最高正化合价在数值上一般
O[典例示范]
等于其最外层电子数及特殊元素的化合价来分析
[典例2]下列微粒半径大小的比较中,正确的是
各选项。A项,C:十4价,N:十5价,F无正价,O
(
无最高正价;B项,K:+1价,Mg:+2价,C:+4
A.Na+<Mg2+<A+<O
价,S:+6价;C项,H:+1价,He无最高正价,Ii:
B.S2->C1>Na+>A13+
+1价,Be:十2价;D项,P:+5价,S:+6价,Cl:+
C.Na<Mg<Al<S
7价,Ar无最高正价。]
D.Cs<Rb<K<Na
O[学以致用]
解析:B[四种离子核外电子数相同,随着核电荷
1.某元素X的最高价氧化物对应水化物的化学式是
数的增多,离子半径依次减小,即微粒半径:A+<
H2XO,则X的简单气态氢化物的分子式为
Mg2+<Na+<O2-,A项错;因S2、C1比Na+、
(
A.HX
B.H,X
A13+多一个电子层,则S2、C1半径比Na+、A13+
C.XH
D.XH
大,再根据“序小径大”的规则,则微粒半径:S2>
解析:D[X元素的最高价氧化物对应的水化物的
CI>Na>A13+,B项正确;Na、Mg、Al、S的原子
化学式为H,XO,,则X的最高正化合价为+4价,
半径依次减小,C项错;Na、K、Rb、Cs最外层电子
说明X原子最外层有4个电子,最低负化合价为
数相同,电子层数依次增多,半径依次增大,
一4价,形成的简单气态氢化物的分子式为XH4。]
D项错。]
·14·
第一章原子结构元素周期律
五维课堂型
[规律总结]短周期中具有相同电子层结构的离子
O[学以致用]
的半径大小比较是粒子半径大小比较中最典型的
2.下列四种离子化合物中,阳离子与阴离子的离子半
题目。在解题时要先把四种离子(常考形式:一般
径比值最小的是
为两种阳离子和两种阴离子)的相对位置确定好,
A.LiI
B.NaCl
其中阳离子:正电荷数即为族序数,阴离子:族序数
C.KBr
D.RbF
=8一负电荷数,因此题目中四种离子的相对位置
解析:A[Li、Na、K+、Rb+等4种阳离子中,
为
B A
CD,则所讨论问题随之解决。
Li+半径最小,I厂、CI厂、Br、F4种阴离子中,I厂半
径最大,所以r(Li)/r(I)最小。]
随堂自测⊙夯基础
对应学生讲义P10
-●
1.下列关于元素周期律的叙述正确的是
()
4.下列各组微粒,半径大小比较中错误的是()
A.随着元素原子序数的递增,原子最外层电子数
A.K>NaLi
B.Na+>Mg2+>A13+
总是从1到8重复出现
C.Mg2+>Nat>F
D.CI>F>F
B.元素的性质随着原子序数的递增而呈周期性
解析:C[最外层电子数相同时,电子层数越多,半
变化
径越大,A项正确;核外电子排布相同的微粒,核电
C.随着元素原子序数的递增,元素的最高化合价从
荷数越大,微粒半径越小,B项正确,C项错误;C1
+1价到+7价,最低化合价从一7价到一1价
比F多一个电子层,离子半径C1>F,同一元素
重复出现
D.元素性质的周期性变化是指原子核外电子排布
的不同微粒,核外电子数越多,半径越大,则微粒半
的周期性变化、原子半径的周期性变化及元素
径F>F,则半径C1>F>F,D项正确。]
主要化合价的周期性变化
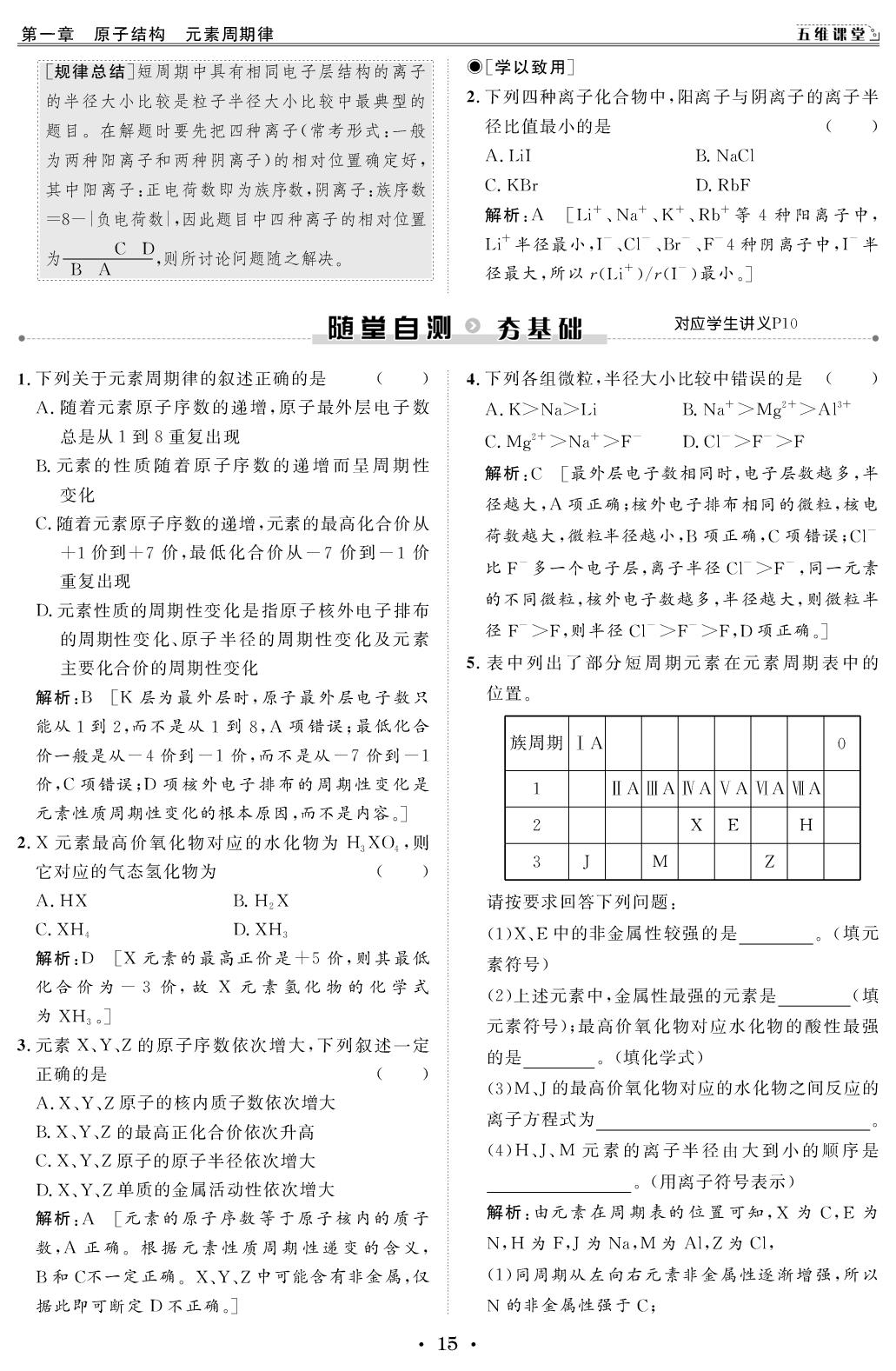
5.表中列出了部分短周期元素在元素周期表中的
解析:B[K层为最外层时,原子最外层电子数只
位置。
能从1到2,而不是从1到8,A项错误;最低化合
族周期
价一般是从一4价到一1价,而不是从一7价到一1
0
价,C项错误;D项核外电子排布的周期性变化是
1
ⅡAⅢAIV A VAVA MI A
元素性质周期性变化的根本原因,而不是内容。]
2
X
H
2.X元素最高价氧化物对应的水化物为HXO,,则
它对应的气态氢化物为
(
M
A.HX
B.H2X
请按要求回答下列问题:
C.XH
D.XH
(1)X、E中的非金属性较强的是
(填元
解析:D[X元素的最高正价是十5价,则其最低
素符号)
化合价为一3价,故X元素氢化物的化学式
(2)上述元素中,金属性最强的元素是
(填
为XH3]
元素符号);最高价氧化物对应水化物的酸性最强
3.元素X、Y、Z的原子序数依次增大,下列叙述一定
的是
。
(填化学式)
正确的是
(3)M、J的最高价氧化物对应的水化物之间反应的
A.X、Y、Z原子的核内质子数依次增大
离子方程式为
B.X、Y、Z的最高正化合价依次升高
C.X、Y、Z原子的原子半径依次增大
(4)H、J、M元素的离子半径由大到小的顺序是
D.X、Y、Z单质的金属活动性依次增大
。
(用离子符号表示)
解析:A[元素的原子序数等于原子核内的质子
解析:由元素在周期表的位置可知,X为C,E为
数,A正确。根据元素性质周期性递变的含义,
N,H为F,J为Na,M为Al,Z为Cl,
B和C不一定正确。X、Y、Z中可能含有非金属,仅
(1)同周期从左向右元素非金属性逐渐增强,所以
据此即可断定D不正确。]
N的非金属性强于C;
·15
世五维课堂
化学(LK)·必修第二册
(2)同周期从左向右元素金属性逐渐减弱,同主族
(3)Na和Al的最高价氧化物的水化物分别为
从上到下金属性逐渐增强,所以金属性最强的元素
NaOH、A1(OH)3,两者反应的离子方程式为:
Al(OH)+OH -A10,+2H,O;
是Na,非金属性越强,最高价氧化物对应水化物的
(4)F、Na+、A13+电子层数都为2层,原子序数越
酸性越强,上述元素中,非金属性最强的元素是F
小,离子半径越大,所以离子半径由大到小的顺序
是:F>Na+>A13+。
元素,但氟元素不存在正价,则最高价氧化物对应
答案:(1)N(2)NaHC1O4(3)A1(OH)3+
水化物的酸性最强的是HCIO4;
OH=A1O2+2H2O(4)F->Na+>A13+
课时评价⊙提能力
对应课时作业P4
1.下列元素的原子半径依次增大是
3.短周期元素X、Y、Z、W、Q在元素周期表中的位置
A.Na、Mg、Al
B.Na、O、F
如表所示,其中X元素的原子内层电子数是最外层
C.P、Si、A1
D.C、Si、P
电子数的一半,则下列说法正确的是
(
解析:C[比较元素原子半径的大小有两条规律:
Y
①具有相同电子层数的元素,随着原子序数的递
W
Q
增,原子半径递减;②具有相同最外层电子数的元
A.钠与W可能形成NaW,化合物
素,随着电子层数的增加,原子半径增大。A项,
B.Z是地壳中含量最多的非金属元素
r(Na)>r(Mg)>r(Al);B项,r(Na)>r(O)>
C.W得电子能力比Q强
r(F);D项,r(Si)>r(P)]
D.X的单质有多种同素异形体,而Y的单质不存
2.短周期主族元素X,Y,Z,W的原子序数依次增大,
在同素异形体
X原子核外最外层电子数是其电子层数的2倍,X,
解析:A[由短周期元素X、Y、Z、W、Q在元素周
Y的核电荷数之比为3:4,W的最外层为8电子
期表中的位置可知,X、Y处于第2周期,Z、W、Q
处于第3周期,X元素的原子内层电子数是最外层
结构,金属单质Z在空气中燃烧生成的化合物可与
电子数的一半,则最外层电子数为4,故X为C元
水发生氧化还原反应,下列说法正确的是()
素,则Z为Si元素、Y为O元素、W为S元素、
A.X与Y能形成多种化合物,一般条件下都能与
Q为C1元素,以此解答该题。由以上分析可知X
Z的最高价氧化物的水化物发生反应
为C元素,Y为O元素,Z为Si元素,W为S元素,
B.原子半径大小:X<Y,Z>W
Q为C1元素,A.钠与W可能形成NaS化合物,
C.化合物Z2Y和ZWY,都只存在离子键
类似过氧化钠,故A正确;B.Y为地壳中含量最多
D.Y、W的某些单质或两元素之间形成的某些化合
的非金属元素,故B错误;C.同周期从左向右非金
物可作水的消毒剂
属性增强,则W得电子能力比Q弱,故C错误;D
解析:D[A.X与Y形成的化合物有CO、CO2
X、Y均存在多种同素异形体,如金刚石、石墨为碳
元素的不同单质,氧气、臭氧为氧元素的不同单质,
等,Z的最高价氧化物的水化物为NaOH,CO和
故D错误;故选:A。]
NaOH不反应,故A错误;B.一般说来,电子层数
4.I是常规核裂变产物之一,可以通过测定大气或
越多,原子半径越大,电子层数相同,质子数越多,
水中I的含量变化来监测核电站是否发生放射性
半径越小,则原子半径大小X>Y,Z>W,故B错
物质泄漏。下列有关3I的叙述中正确的是(
误;C.化合物Z2Y和ZWY3分别为NaO、Na-
A.I的化学性质与31相同
CIO3,NaClO3存在离子键和共价键,故C错误;
B.131的原子序数为53
D.Y的单质臭氧,W的单质氯气,对应的化合物
C.I的原子核外电子数为78
ClO2,可作为水的消毒剂,故D正确。故选:D。]
D.I的原子核内质子数多于中子数
·16
第一章原子结构元素周期律
五维课堂型
解析:B[A.1与3I核外电子数相同,质子数相
解析:C[Xm+、Ym-和Ar具有相同的电子层结
同,最外层电子数相同,化学性质相同,故A错误:
构,其原子序数:X>A>Y,A项错误;X原子最外
B.原子序数=核电荷数=核外电子数=质子数=
层电子数比Y的少,B项错误;X的原子半径比Y
53,故B正确;C.质子数=核外电子数=原子序数
的大,C项正确;X元素的最高正价比Y的小,D项
=核电荷数,原子核外电子数53,故C错误;D.原子核
错误。]
内质子数=53,中子数=质量数一质子数=131一53=
9.已知原子序数小于18的元素的离子aA+、bB+、
78,原子核内质子数少于中子数,故D错误;]
cC2、dD都具有相同的电子层结构,则下列叙述
5.下列说法中正确的是
正确的是
(
A.非金属元素呈现的最低化合价,其绝对值等于
A.原子半径;A>B>D>C
该元素原子的最外层电子数
B.离子半径:C2->D>B+>A+
B.非金属元素呈现的最高化合价不超过该元素原
C.原子序数:d>c>b>a
子的最外层电子数
D.原子的最外层电子数目:A>B>D>C
C.最外层有2个电子的原子都是金属原子
解析:B[由4种离子具有相同的电子层结构可得
D.金属元素只有正价和零价,而非金属元素既有
a-2=b-1=c十2=d+1,a>b>d>c,故C项错
正价又有负价和零价
误;原子的最外层电子数目:D>C>A>B,故D项
解析:B[非金属元素最低化合价的绝对值等于8
错误;原子半径B>A>C>D,故A项错误,]
减去最外层电子数,A错误;非金属元素的最高化
10.(双选)A、B、C均为1~18号元素,A、B原子具有
合价等于该元素原子的最外层电子数,不会超过该
相同的电子层数,A、C的最低价阴离子分别为
数值,B正确;氦氨原子最外层有2个电子,C错误;
A2、C,A2半径大于C,B+与C具有相同的
并非所有非金属元素都有正价,如F无正价,
电子层结构。下列叙述中一定不正确的是()
D错误。]
A.原子序数:C>A>B
6.下列各元素性质递变情况中,错误的是(
B.离子半径:A2>C>B+
A.Li、Be、B原子最外层电子数依次增多
C.原子半径:C>B>A
B.P、S,C1元素最高化合价依次升高
D.最外层电子数:C>A>B
C.N、O、F原子半径依次增大
解析:AC[由A、C的最低价阴离子分别为A
D.P、S、CI元素的最低化合价依次为一3价、一2
和C知A为MA族元素,C为ⅧA族元素,B+
价、一1价
和C具有相同的电子层结构,则B在C的下一
解析:C[根据原子的核外电子排布可知,A项正
周期,且A、B、C均为短周期元素,B处于第3周
确;P、S、C1的最高化合价依次为+5价、十6价、+
期A族,故B为Mg,C为F,A、B同周期,则A为S。
7价,B项正确;在电子层数相同的情况下,核电荷
原子序数:A>B>C,故A错误;离子的电子层数越
数越大,半径越小,C项错误;P、S、C1的最低化合
多,半径越大,电子层数相同的离子,核电荷数越大,
价依次为一3价、一2价、一1价,D项正确。]
离子半径越小(0族元素除外),所以离子半径A2>
7.原子序数小于20的X元素能形成H2X和XO2两
C>B+,故B正确;同周期主族元素的原子半径从
种化合物,该元素的原子序数是
(
左到右逐渐减小,同主族元素自上而下原子半径逐
A.13
B.14
渐增大,原子半径:B>A>C,故C错误;A为S,B为
C.15
D.16
Mg,C为F,原子最外层电子数分别为6、2、7,故最外
解析:D[X元素在H2X中呈一2价,在XO2中呈
层电子数:C>A>B,故D正确。]
十4价,一般在氢化物中呈现最低负价,该元素的
11.有下列四种微粒:①O②Na③Mg
最高正价为十6价,即最外层电子数为6,只有原子
④N。
序数为16时符合条件。]
(1)按原子半径由大到小的顺序排列为
8.X元素的阳离子和Y元素的阴离子具有与氩离子
(只填序号,下同)。
相同的电子层结构,下列叙述正确的是
()
(2)按离子半径由大到小的顺序排列为
A.X原子序数比Y的小
(3)微粒中质子数小于中子数的是
B.X原子最外层电子数比Y的多
(4)能形成X2Y2型化合物的是
C.X的原子半径比Y的大
(5)通常情况下,化合价有0价、正价和负价的是
D.X元素的最高正价比Y的大
·17·
世五维课堂
化学(LK)·必修第二册
解析:(1)Na与Mg具有相同的电子层数,最外层
13.在1~18号的短周期主族元素中,表中的字母代
电子数分别为1、2,O与N具有相同的电子层数,
表一种元素,回答下列问题:
最外层电子数分别为6、5:原子半径大小为Na>
Mg>N>O。(2)四种离子Na+、Mg2+、N3-和
O核外电子排布相同,半径大小为r(Mg+)<
A
B
E
r(Na+)<r(O2)<r(N3-)。(3)四种核素质子数
和中子数分别是:O>8、10;Na→11、12;Mg→12、
(1)金属性最强的元素是
12:N→7、7。(5)通常情况下O元素不显正价,
(2)画出D的原子结构示意图
Na、Mg不显负价,只有N元素有0价、正价和
(3)地壳中含量最多的元素是
负价。
(4)Ne原子的最外层电子数是
(5)E和F分别形成的气态氢化物中最稳定的是
答案:(1)②③④①(2)④①②③(3)①②
。(填写氢化物的化学式)
(4)①②(5)④
(6)Mg(OH)2与A1(OH)3能与强碱反应的是
12.有A、B、C、D、E五种元素,它们的原子序数按E、
C、D、A、B依次增大,E原子最外层有4个电子;
(7)用于制造光导纤维的物质是
。(填
A与B的核外电子排布相同;D的气态氢化物
“Si”或“SiO,”)
的化学式为H,D,最高价氧化物中D的质量分数
(8)肼(N2H)中氮元素和氢元素的质量比m(N)
为40%,且D原子核内质子数和中子数相等;C
:m(H)=
。(相对原子质量:N一
的原子序数比D少9,比B少12,其气态氢化物中
14,H-1)
氢元素的质量分数约为17.65%。
(9)次氯酸(HCIO)具有杀菌漂白作用,其中C1元
(1)写出五种元素的符号:A
、B
素的化合价为
,HC1O不稳定,易分解生
,D
,E
成HC1和O,写出其在光照条件下分解的化学方
(2)画出A、B+的结构示意图:
程式:
解析:(1)上述元素中,金属性最强的是Na元素;
(2)D为N元素,原子核外有2个电子层,最外层
(3)A、D最高价氧化物对应的水化物的化学式分
别为
电子数为5,N的原子结构示意图为:
(4)写出E的最高价氧化物与过量的B的最高价
(3)地壳中含量最多的元素是O元素;
氧化物对应的水化物反应的离子方程式:
(4)Ne原子为10号元素,核电荷数为10,最外层
(⑤)写出B、C最高价氧化物对应的水化物之间相
电子8;(5)E和F分别形成的气态氢化物为
互反应的化学方程式:
H2S、HCl,非金属性CI>S,氢化物稳定性中最稳
解析:D的气态氢化物的化学式为HD,最高价氧
定的是HCl;(6)Mg(OH)2与Al(OH)3能与强
化物中D的质量分数为40%,可推出D的相对原
碱反应的是A1(OH)3;(7)用于制造光导纤维的物
子质量为32,从而推出D为S元素:C原子序数
质是:SiO2;(8)肼(N2H,)中氨元素和氢元素的质
比D少9,比B少12,则C为N元素,B为K元
量比m(N):m(H)=2×1:4×1=7:1;(9)次氯
素;A与B核外电子排布相同,则A为C1元素;
酸(HC1O)具有杀菌漂白作用,氢元素化合价+1
E原子最外层有4个电子,且原子序数按E、C、D、
价,氧元素化合价一2,其中C1元素的化合价为+
A、B依次增大,则E为C元素。
1价,HCIO不稳定,易分解生成HC1和O2,反应
答案:(1)C1KNSC
的化学方程式为:2HC1O光照
O2↑+2HC1。
(3)HCIO,H,SO
答案:(1)Na
(3)O(4)8(5)HC1
(4)CO2+2OH
-CO+H,O
(6)A1(OH)3
(7)SiO,
(8)7:1(9)+1
(5)KOH+HNO,-KNO,+H,O
2HC10光展2HC1+0,+
·18·
资源预览图

1

2
3
相关资源
由于学科网是一个信息分享及获取的平台,不确保部分用户上传资料的 来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系学科网,我们核实后将及时进行处理。

