17.2024年安徽省中考题型真题汇编卷十二-【中考金卷王】2025年安徽中考化学试题汇编
2025-12-30
|
2份
|
9页
|
139人阅读
|
5人下载
资源信息
| 学段 | 初中 |
|---|---|
| 学科 | 化学 |
| 教材版本 | - |
| 年级 | 九年级 |
| 章节 | - |
| 类型 | 题集-试题汇编 |
| 知识点 | - |
| 使用场景 | 中考复习-真题 |
| 学年 | 2025-2026 |
| 地区(省份) | 安徽省 |
| 地区(市) | - |
| 地区(区县) | - |
| 文件格式 | ZIP |
| 文件大小 | 6.06 MB |
| 发布时间 | 2025-12-30 |
| 更新时间 | 2025-12-30 |
| 作者 | 安徽庐阳书社图书有限公司 |
| 品牌系列 | - |
| 审核时间 | 2025-12-30 |
| 下载链接 | https://m.zxxk.com/soft/55695331.html |
| 价格 | 3.00储值(1储值=1元) |
| 来源 | 学科网 |
内容正文:
(2)O4Fe0一定条件Fe,0,十Fe②ABC
[解析](1)①气态水的分子间隔比固态水的分子间隔更大;
②由微粒的变化可知,水由固态变为气态时水分子间的间隙发
生了变化,但水分子本身没有发生变化,所以化学性质没有改
变。(2)①在一定条件下,FeO分解生成FeO4和单质铁,反应
的化学方程式为4Fe0一定条件Fe,O,十Fe②磁铁矿是工业
炼铁的重要原料之一,故A正确;铁锈的主要成分是氧化铁的
水合物,可表示为FeO,·xH2O,故B正确;合金的特点是硬
度大,熔点低,耐腐蚀,因此相比于纯金属,合金具有更广泛的
用途,故C正确。
14.(1)铁架台
(2)2KMn0,△K,Mm0,十Mn0,+O,个氧气不易溶于水
把导管移出水面
(3)变浑浊
(4)与空气接触温度达到可燃物的着火点
[解析](1)由题图可知,仪器a的名称为铁架台。(2)高锰酸钾
在加热的条件下生成锰酸钾、二氧化锰和氧气,反应的化学方
程式为2KMnO,△K,MnO,十MnO,十O.+;氧气可采用排
水法进行收集,体现了氧气的物理性质是不易溶于水;停止加
热时,为防止倒吸,应先进行的操作是把导管移出水面。(3)木
炭在氧气中燃烧生成二氧化碳,二氧化碳与澄清石灰水的主要
成分氢氧化钙反应生成碳酸钙和水,可观察到澄清石灰水变浑
浊。(4)甲中液面降低后,白磷与空气接触开始燃烧,说明燃烧
需要与空气接触;乙中原先白鳞与空气接触不燃烧,热水进入
后乙中白磷燃烧,说明燃烧需要温度达到可燃物的着火点。
15.(1)将红渣块粉碎(或升高温度或搅拌)
(2)Fe2O3+3H2SO4—Fe2(S04)3+3H2O
(3)SiO,
(4)B
[解析](1)为加快“酸浸”的反应速率,可采取的措施是将红渣
块粉碎或升高温度或搅拌。(2)“酸浸”中发生的反应是氧化铁
与硫酸反应生成硫酸铁和水,反应的化学方程式为F2O3十
3H2SO4一Fe2(SO4)3十3H2O。(3)红渣块的主要成分为
Fe2O3和SiO2,SiO2不溶于水和常见的酸,因此“滤渣”的主要
成分是二氧化硅。(4)锌、铜与硫酸铁反应除生成疏酸亚铁外,
还会生成硫酸锌、硫酸铜,而铁与硫酸铁反应只生成硫酸亚铁,
因此,“适量的金属”最佳的选择是铁。
16.(1)①物理变化②升高
(2)氨气分子间的间隙
(3)N
(4)解:设氨气质量是x。
2NH,+H2 SO-(NH)2 SO
172024年安徽省中
1.D[解析]采粽叶过程中只是将粽叶采摘下来,没有新物质生
成,属于物理变化,故A错误;洗粽叶过程中只是洗掉杂质,没有
新物质生成,属于物理变化,故B错误;包粽子过程中只是形状
的改变,没有新物质生成,属于物理变化,故C错误;煮粽子过程
中,涉及燃烧,有新物质生成,属于化学变化,故D正确。
2.A[解析]糯米的主要成分是淀粉,淀粉属于糖类。
3.C[解析]推广利用太阳能和风能发电,与环保理念相符,故A
正确:减少使用塑料袋,减少白色污染,与环保理念相符,故B正
确;生活中经常使用一次性碗筷,与环保理念不相符,故C错误;
合理使用化肥,与环保理念相符,故D正确。
2
34
98
9.8g×10%
34
989.8g×10%
x=0.34g
14
氢元素质量为0.34g×14十3X×100%=0.28g
0.28g
废水中的氮元素含量为200X10元=1.4gL
答:该废水中的氨元素含量为1.4g·L1。
(5)BD
(6)3NaCIO++2NH,-N2+3NaCl+3H2O
②部分氨气被转化为NO2或NO留在废水中
[解析](1)①可通过分离液态空气获得原料N2,该过程中没有
生成新物质,是物理变化;②高温下,部分FeO,被H2还原为
FO,转化过程中固体中铁元素质量不变,固体质量减小,固体
所含铁元素的质量分数升高。(2)液氨可用作制冷剂,氨气转
化为液氨过程中,发生改变的是氨气分子间的间隙,即间隙变
小。(3)利用NH去除汽车尾气中的NO,生成水和一种气体
单质,即氮气。该过程中化合价发生变化的元素是氮元素,即
氮元素化合价由一氧化氮中的十2价变成氮气中的0价。
(5)“吹脱”时,加入物质X,将NH转化为NH3,并通入热空气
将NH?吹出。物质X可选用氢氧化钠溶液(氢氧根离子能和
铵根离子结合生成氨分子和水)、生石灰(生石灰和水反应生成
氢氧化钙,放热)。(6)①次氯酸钠和氨气反应生成氨气、氯化
钠和水,NaClO将NH反应转化为N2的化学方程式为
3NaC1O+2NH3—N2+3NaC1+3H2O;②当m(NaCIO)>m1
时,废水中总氮残留率上升的原因是部分氨气被转化为NO,
或NO2留在废水中。
17.解:(1)26
(2)粉末中锌的质量是32.5g一26g=6.5g。
设反应生成硫酸锌质量是x,反应生成氢气质量是y。
Zn+H2SO4—ZnSO.+H2↑
65
1612
6.5g
y
65_6.5gx=16.1g
161x
65_6.5gy=0.2g
2
y
恰好完全反应时,所得溶液的溶质质量分数为
16.1g
X100%=16.1%
6.5g+93.7g-0.2g
答:硫酸锌质量分数是16.1%。
考题型真题汇编卷十二
4.D[解析]A.“锂”带“钅”字旁,属于金属元素,故选项说法错
误;B.根据元素周期表中的一格可知,汉字下面的数字表示相对
原子质量,该元素的相对原子质量为6.941,故选项说法错误;
C.锂原子的最外层电子数为1,在化学反应中易失去1个电子而
形成带1个单位正电荷的阳离子,化合价的数值等于离子所带
电荷的数值,且符号一致,则该元素的化合价为十1价,氯元素显
一1价,氯化锂的化学式为LiCl,故选项说法错误;D.锂原子的
最外层电子数是1,少于4,在化学反应中易失去1个电子而形成
阳离子,故选项说法正确。
5.B[解析]A.氯乙烯中碳、氢、氯三种元素的质量比为(12×2):
(1×3):(35.5×1)=24:3:35.5,则氯乙烯中氢元素质量分
数最小,故选项说法正确;B.氯乙烯是由氯乙烯分子构成的,1个
氯乙烯分子是由2个碳原子、3个氢原子、1个氯原子构成的,故
选项说法错误;C.氯乙烯是含碳元素的化合物,属于有机物,故
选项说法正确;D.氯乙烯中碳、氢元素质量比为(12X2):(1X
3)=8:1,故选项说法正确。
6.C[解析]A.该装置是散开装置,气体能够进出试管,不能检验
是否漏气,故选项不正确;B.取下瓶塞,瓶塞应该倒放在桌上,瓶
口要紧贴着试管口,故选项不正确;C.加热液体时,液体体积不
能超过试管体积的三分之一,并且试管与桌面呈45度角,故选
项正确;D.不能把实验废液直接倒入水池中,应该处理达标后再
排放,该选项不正确。
7.C[解析]A.通过沉降、过滤可除去水中的不溶性杂质,选项说
法正确;B.生活中常用煮沸的方法对水进行杀菌消毒,选项说法
正确;C.溶液中各种微观粒子并不是静止不动,是在不断运动
的,选项说法错误;D.设需要加水的质量为x,则50g×20%=
(x+50g)×5%,解得x=150g,选项说法正确。
8.D[解析门A.甲中微粒表示的是水分子,水是由水分子构成的,
则甲中微粒能保持水的化学性质,故选项说法正确;B.乙中微粒
表示的是氢原子和氧原子,在化学变化过程中没有发生改变,故
选项说法正确;C.丙中物质中含有氢气、氧气,属于混合物,故选
项说法正确:D.丙中生成2个氢分子和1个氧分子,氢气和氧气
的质量比为(2×2):32=1:8,故选项说法错误。
9.C[解析]A.Cu(NO3)2和AgNO3溶液均能与足量的铝粉反
应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故
选项不能达到实验目的;B.变质的氢氧化钠中含有碳酸钠,取
样,加入稀疏酸观察是否产生气体,只能证明氢氧化钠是否变
质,不能检验变质的程度,故选项不能达到实验目的;C.氯化钠
易溶于水,硫酸钡难溶于水,加水溶解,过滤、蒸发结晶,能分离
出氯化钠,清洗滤渣并晾干,能分离出硫酸钡,故选项能达到实
验目的;D.CHa和H2燃烧均能生成水,点燃,在火焰上方罩
个干冷的烧杯,烧杯内壁均会出现水雾,不能鉴别,故选项不能
达到实验目的。
10.A[解析]A.合金是金属材料,该选项正确;B.青铜是合金,容
点低于纯铜,该选项不正确;C.青铜硬度比纯锡大,该选项不正
确;D.铜不能和稀硫酸反应,该选项不正确。
11.C[解析]向一集满CO2的集气瓶中放入一片蓝色石蕊试纸,
注入适量的蒸馏水,盖上玻璃片,上下振荡,再将其倒置,把手
移开,玻璃片没有掉下来,说明瓶内压强减小;蓝色石蕊试纸在
注入蒸馏水并振荡后变红,说明生成了酸性物质,故C选项
正确。
12.D[解析]高于40℃时,碳酸钠的溶解度随温度的升高而减
小,故A错误;在比较物质的溶解度时,需要指明温度,温度不
能确定,溶解度也不能确定,故B错误;T℃时,氯化钠的溶解
度大于30g,但小于60g,所以30gNaC1不能完全溶解于50g
水中,故C错误;T℃时,Na2CO3和NaCl的溶解度相等,所以
两种饱和溶液的溶质质量分数相,故D正确。
13.(1)过滤
(2)分子是在不断运动的
(3)有机物14:5
4④3Fe十4H,0高温Fe,0,十4H:置换反应
[解析](1)“浇纸”是用滤网分离出纸浆,该操作与化学实验中
的过滤相似。(2)普洱茶茶香四溢,从分子角度对此现象的解
释是分子是在不断运动的。(3)靛蓝(C16HN2O2)是一种含碳
}
-28
元素的混合物,属于有机物,其中氮、氢元素的质量比为(14×
2):(1×10)=14:5。(4)铁在高温下与水蒸气反应生成四氧
化三铁和氢气。该反应的化学方程式为3F®十4H,0商温
Fe3O4十4H2,该反应是一种单质和一种化合物反应生成了另
一种单质和另一种化合物,属于置换反应。
14.(1)长颈漏斗
(2)2KMnO4
△K,MnO,+MnO2+O:t
(3)C m E
[解析门](1)由题图可知,标号a的仪器名称是长颈漏斗。(2)A
装置是固体加热型发生装置,试管口有一团棉花,D装置是用
排水法收集气体,则AD装置适用于高锰酸钾制取氧气,高锰
酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,反应的化
学方程式为2KMn0,△K,MnO,十MnO,+O,个。(3)在加
热的条件下,铜与浓硫酸可反应生成SO2,若要制取SO2,需要
固液加热型发生装置,则可选择发生装置是C。SO2是一种密
度比空气大的有毒气体,若用G装置收集SO2,气体应从m进
入。SO2部分化学性质与CO2相似,则SO2也能和氢氧化钠
反应,所以制取SO2过程中,为防止污染环境,还应选择装有氢
氧化钠溶液的E装置进行尾气处理。
15.(1)氢氧化钠溶液
(2)2HCI+Mg(OH)2-MgCl2+2H2 O
(3)蒸发结晶
(4)2LiC1+Na2 CO3=Li2 CO3+2NaCl
(5)防止MgCl2与Na2CO3反应生成MgCO3沉淀,导致
Li2CO3不纯
[解析](1)根据流程,为避免引入新杂质,过程工中加入的适量
物质X是氢氧化钠溶液,氢氧化钠和氯化镁反应生成氢氧化镁
沉淀和氯化钠,氯化钠是已知物质,不是新的杂质。(2)制镁过
程中,氢氧化镁和盐酸反应生成氯化镁和水,该反应是酸和碱
反应生成盐和水,属于中和反应,化学方程式为2HC1十
Mg(OH)2一MgCl2+2H2O。(3)氯化钠的溶解度受温度变
化影响较小,氯化钠的结晶方法是蒸发结晶。(4)过程Ⅲ中氯
化锂和碳酸钠相互交换成分(复分解反应)生成碳酸锂沉淀和
氯化钠,化学方程式为2LiCl+Na2CO3一Li,CO3¥十2NaCl。
(⑤)用盐湖卤水制取碳酸锂,要先除去卤水中的氯化镁,防止
MgCl2与Na2CO3反应生成MgCO3沉淀,导致Li2CO3不纯。
16.【作出猜想】Na2CO3、NaHCO
【实验验证】变红NaHCOg
【交流反思】加快固体物质的溶解浓度大于0.83%的碳酸氢
钠溶液中加入0.1%的氯化钙溶液,也会产生白色沉淀,不能说
明含有Na2COg
【实验验证】CaCl2+Na2CO3—CaCO3Y+2NaCl
【交流反思】2 NaHCO,.△Na,CO,+H,O+CO,+
【迁移应用】低温贮存
【拓展延伸】取样品少量,滴加食醋,有气泡产生的是果蔬洗盐,
无明显现象的是食盐
[解析]【作出猜想】根据标签和猜想1、猜想3可知,猜想2为
Naz COa、NaHCO3。
【实验验证】碳酸钠、碳酸氢钠的水溶液都显碱性,取样溶于水,
滴加无色酚酞溶液,溶液变红;澄清石灰水变浑浊,说明有二氧
化碳生成,碳酸钠受热不分解,碳酸氢钠受热分解生成碳酸钠、
水和二氧化碳,所以可得出含有碳酸氢钠。
【交流反思】实验3中玻璃棒搅拌的作用是加快固体物质的溶
解;由资料可知,浓度大于0.83%的碳酸氢钠溶液中加入
0.1%的氯化钙溶液,产生白色沉淀,不能说明含有Na2COa,也
可能有NaHCO3。
【实验验证】氯化钙与碳酸钠反应生成碳酸钙和氯化钠,该反应
的化学方程式为CaCl2+Na2COa-CaCO3Y+2NaCl。
【交流反思】碳酸氢钠受热分解生成碳酸钠、水和二氧化碳,该
反应的化学方程式为2NaHC0,△Na,C0,+H,0+C0,个。
【迁移应用】碳酸氢钠在50℃以上逐渐分解产生二氧化碳、碳
酸钠和水,此类果蔬洗盐的贮存条件是低温贮存。
【拓展延伸】取样品少量,滴加食醋,有气泡产生的是果蔬洗盐,
182024年安徽省中
1.C[解析]A.粮食酿酒,酒精是新物质,属于化学变化,故选项
错误;B.陶瓷烧制,瓷器是新物质,属于化学变化,故选项错误;
C.活字印刷没有新物质生成,属于物理变化,故选项正确;D.火
药爆炸生成有害气体和烟尘,属于化学变化,故选项错误。
2.B[解析]元素是具有相同核电荷数(即核内质子数)的一类原
子的总称,是宏观概念,只讲种类,不讲个数。这里的“氟、碘
锌”是指元素。
3.C[解析]分类回收生活垃圾,可以节约资源,减少污染,故A正
确;工业废水中含有有害物质,工业废水净化达标排放可以防止
水体污染,有利于环境保护,故B正确;推广使用煤炭燃料,会造
成环境的污染,故C错误;使用可降解塑料,可以减少白色污染,
保护环境,故D正确。
4.B[解析]A.“硒”带“石”字旁,属于固态非金属元素,故选项说
法错误;B.根据元素周期表中的一格可知,字母表示该元素的元
素符号,硒的元素符号为Se,故选项说法正确;C.根据元素周期
表中的一格可知,左上角的数字表示原子序数,该元素的原子序
数为34;根据原子中原子序数=核电荷数=质子数=核外电子
数,则硒原子的核外电子数为34,而不是最外层电子数为34,故
选项说法错误;D.根据元素周期表中的一格可知,汉字下面的数
字表示相对原子质量,该元素的相对原子质量为78.96,相对原
子质量单位是“1”,不是“g”,故选项说法错误。
5.A[解析]A.向试管中倾倒液体药品时,瓶塞要倒放,标签要对
准手心,瓶口紧挨试管口,图中所示操作错误;B.使用酒精灯时
要注意“两查、两禁、一不可”,可用火柴点燃酒精灯,图中所示操
作正确;C.蒸发时,应用玻璃棒不断搅拌,以防止局部温度过高,造
成液体飞溅,图中所示操作正确;D.使用胶头滴管滴加少量液体时,
注意胶头滴管不能伸入到烧杯内或接触烧杯内壁,应垂直悬空在烧
杯口上方滴加液体,防止污染胶头滴管,图中所示操作正确。
6.D[解析]A.鱼腥草素是由鱼腥草素分子构成的,不含氧分子,
故选项说法错误;B.相对分子质量单位是“1”,不是“g”,常常省
略不写,故选项说法错误;C.元素只讲种类、不讲个数,故选项说
法错误;D.1个鱼腥草素分子是由12个碳原子、22个氢原子和2
个氧原子构成的,则1个鱼腥草素分子含有36个原子,故选项
说法正确。
7.D[解析]海水蒸发说明水分子在不断运动,运动到空气中了,
故A正确;地球表面约有71%被水覆盖着,其中海洋水占全球
总水量的96.5%,海水占全球总储水量的绝大多数,故B正确;
蒸馏可以除去水中的杂质,得到的蒸馏水属于纯水,所以说蒸馏
可以从海水中获得淡水,故C正确;纯水中只含有水,而海水中
含有较多自由移动的离子,所以相同条件下海水的导电能力比
纯水强,故D错误。
一2
无明显现象的是食盐。
17.解:(1)5:2
(2)设参加反应的水的质量是x。
CaO+H2O=Ca(OH)2
5618
56g x
5656g
18x
x=18g
答:参加反应的H20的质量是18g。
考题型真题汇编卷十三
8.C[解析]A.由反应的微观示意图,微观上该反应是水分子和
二氧化碳分子在一定条件下生成甲烷分子和氧分子,反应的化
学方程式为2H,0十C0,一定条件CH,十20,则参加反应的
甲、乙质量比为(18×2):44=9:11,故选项说法错误;B.化学
反应前后分子种类一定会发生改变,分子的个数可能会发生改
变,故选项说法错误;C.反应物中氧元素显一2价,生成物中氧
气属于单质,氧元素显0价,则反应前后氧元素的化合价发生了
改变,故选项说法正确;D.甲、乙、均为化合物,丁是单质,故选项
说法错误。
9.B[解析]A.不锈钢的组成成分中不含铝,题图中实验不能用于
比较合金与其组分金属的硬度,故选项不能达到相应目的;B.铜
片和锌粒分别放入硫酸亚铁溶液中,Z与硫酸亚铁溶液反应置
换出铁,说明了金属活动性Zn>Fe;铜片与疏酸亚铁溶液不反
应,说明了金属活动性Fe>Cu;由此可得出三种金属活动性
Zn>Fe>Cu,故选项能达到相应目的;C.第一支试管中的铜片
能与二氧化碳、水充分接触,第二支试管中的铜片能与氧气、水
充分接触,第三支试管中的铜片能与二氧化碳、氧气、水接触;一
段时间后,前两支试管中的铜片设有生锈,第三支试管中的铜片
生锈,可用于探究铜生锈条件是与二氧化碳、氧气有关,无法证
明是否与水有关,故选项不能达到相应目的;D.铁和稀硫酸反应
生成碗酸亚铁和氢气,反应过程中氢气逸出,反应后烧杯中的物
质质量减少,不能直接用于验证质量守恒定律,故选项不能达到
相应目的。
10.C[解析]根据原物质和杂质的性质选择适当的除杂剂和分离
方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改
变。除杂至少要满足“不增不减”的原则,“不增”是指不增加新
杂质,“不减”是指不减少目标物质的质量。A.氧气通过灼热的
铜网时可与铜发生反应生成氧化铜,而氮气不与铜反应,反而
会把原物质除去,不符合除杂原则,故选项错误;B.KC1易溶于
水,MnO2难溶于水,可采取加水溶解、过滤、蒸发结晶的方法进
行分离除杂,故选项错误;C.CO能与足量的氧化铜在加热条件
下反应生成铜和二氧化碳,能除去杂质且没有引入新的杂质,
符合除杂原则,故选项正确;D.稀疏酸能与适量的Ba(NO3)2
溶液反应生成疏酸钡沉淀和硝酸,能除去杂质但引入了新的杂
质硝酸,不符合除杂原则,故选项错误。
11.D[解析]A.酒能变醋,需要通过化学反应才能表现出来,属
于化学性质,故选项说法正确;B.在金属活动性顺序中,铅的位
置排在氢之前,铅能与醋酸反应产生氢气,故选项说法正确;
C.PbCO3中碳酸根显一2价,设铅元素的化合价是x,根据在
化合物中正负化合价代数和为零,可得x十(一2)=0,则x=
十2价,故选项说法正确;D.加热浮粉(PbCO3)得铅白(PbO)固17
2024年安徽省中考题型真题汇编卷十二
化
学
注意事项:
1.本卷共两大题17小题,满分40分。化学与物理的考试时间共120分钟。
2.可能用到的相对原子质量:H-1C-120-16N-14Na-23S-32C1-35.5
Cu-64Ca-40
题号
二
总分
得分
得分
评卷人
一、选择题(本大题包括12小题,每小题1分,共12分。每小题的4个选项中只有
1个符合题意。)
(2024·湖北)阅读下列材料,回答1一2题。
彩缕碧筠粽,香粳白玉团。端午时节,粽叶飘香。粽子是用粽叶包裹糯米等蒸煮而成的食品,因
粽叶中含有对乙烯基苯酚,从而会散发出清香。
1.在下列粽子制作过程中,一定发生化学变化的是
(
A.采粽叶
B.洗粽叶
C.包粽子
D.煮粽子
2.糯米的主要成分是淀粉,淀粉属于
A.糖类
B.油脂
C.蛋白质
D.维生素
3.(2024·新疆)今年世界地球日的主题是“全球战塑”,旨在提高公众环保意识。下列做法与环保理
念不相符的是
()
A.推广利用太阳能和风能发电
B.减少使用塑料袋
C.生活中经常使用一次性碗筷
D.合理使用化肥
4.(2024·黑龙江)有“锂”走遍天下,无“锂”寸步难行。科学不断进步,锂电池应用日益广泛。如图
是锂元素在元素周期表中的部分信息及原子结构示意图,下列说法正确的是
3
Li
锂
6.941
A.锂元素属于非金属元素
B.锂元素的相对原子质量为3
C.氯化锂的化学式为LiCl2
D.锂原子在化学反应中容易失去电子
·17-1·
5.(2024·绥化)“冰墩墩”外壳的主要成分是PVC(聚氯乙烯)及PC(聚碳酸酯),其中聚氯乙烯的单
体是氯乙烯,其化学式为C2HC1。下列选项不正确的是
A.氯乙烯中氢元素质量分数最小
B.氯乙烯由2个碳原子、3个氢原子、1个氯原子构成
C.氯乙烯是有机化合物
D.氯乙烯中碳、氢元素质量比为8:1
6.(2024·赤峰)规范操作是实验成功的保障,下列操作正确的是
@4
水池
目
A.检查气密性
B.液体的倾倒
C.给液体加热
D.处理实验废液
7.(2024·烟台)下列有关水和溶液的说法错误的是
A.通过沉降、过滤可除去水中的不溶性杂质
B.生活中常用煮沸的方法对水进行杀菌消毒
C.溶液具有均一性、稳定性的原因是溶液中各种微观粒子都静止不动
D.将50g溶质质量分数为20%的硝酸钾溶液稀释成5%,需要加水150g
8.(2024·盐城)如图是电解水反应的微观示意图。据此判断下列说法中不正确的是
。氢原子
00
氧原子
甲
丙
A.甲中微粒能保持水的化学性质
B.乙中微粒在化学变化过程中没有发生改变
C.丙中的物质属于混合物
D.丙中氢气和氧气的质量比为2:1
9.(2024·重庆A卷)下列实验方法和主要操作能达到实验目的的是
(
)
选项
物质
方法和主要操作
实验目的
A
Cu(NO3)2和AgNO3的混合溶液
加入足量的铝粉,过滤
除去AgNO3
B
久置的NaOH
取样,加入稀硫酸观察是否产生气体
检验变质程度
C
NaCl和BaSO,
加水溶解,过滤、蒸发结晶,清洗滤渣并晾干
分离提纯
0
CH4和H2
点燃,在火焰上方罩一个干冷的烧杯
鉴别
10.(2024·湖北)湖北省博物馆馆藏的越王勾践青铜剑,其主要成分为铜锡合金。下列有关铜锡合
金说法正确的是
()
A.属于金属材料
B.熔点高于纯铜
C.硬度低于纯锡
D.铜、锡均能与稀硫酸反应
·17-2·
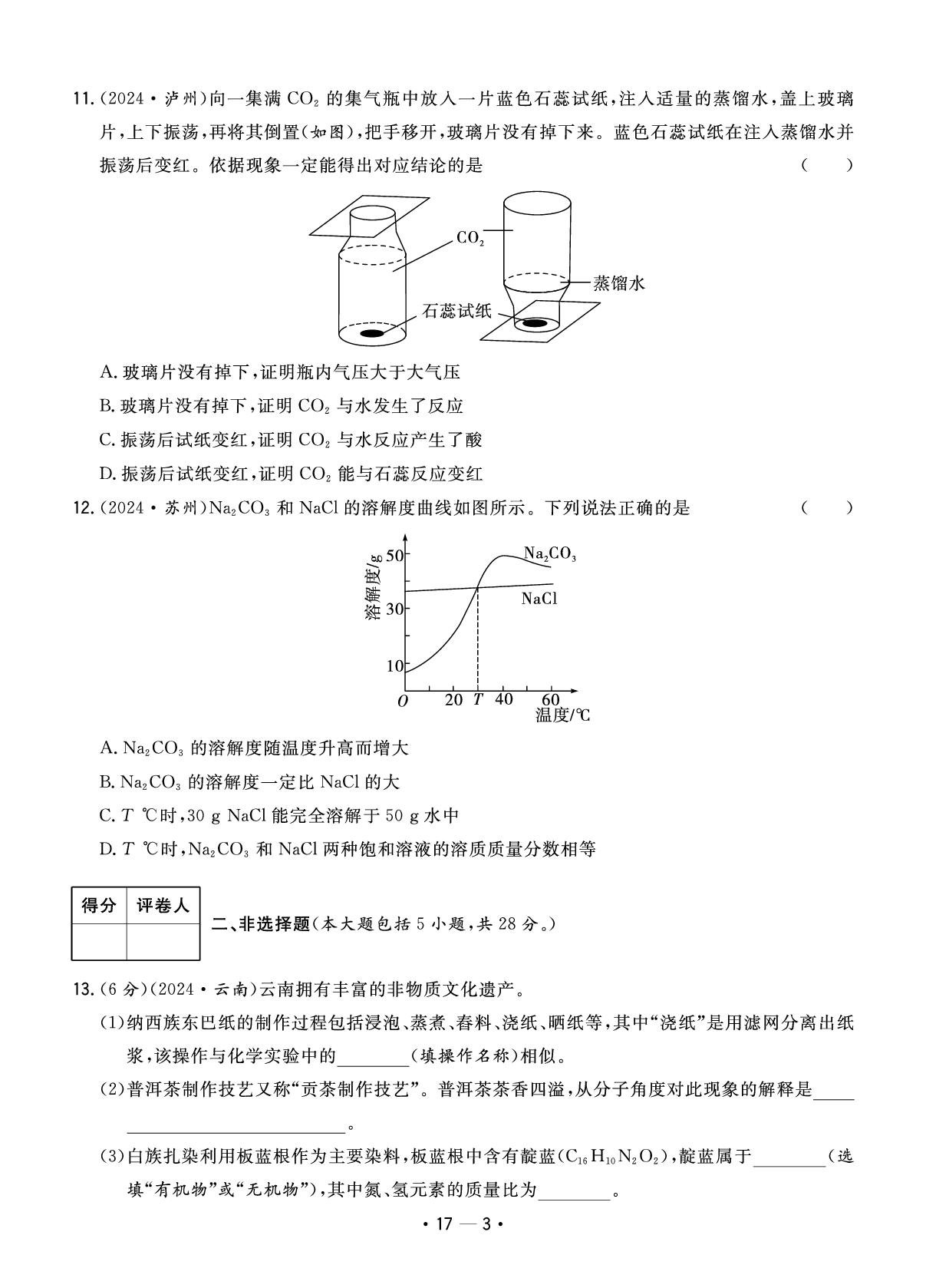
11.(2024·泸州)向一集满C02的集气瓶中放入一片蓝色石蕊试纸,注入适量的蒸馏水,盖上玻璃
片,上下振荡,再将其倒置(如图),把手移开,玻璃片没有掉下来。蓝色石蕊试纸在注入蒸馏水并
振荡后变红。依据现象一定能得出对应结论的是
()
CO
蒸馏水
石蕊试纸
A.玻璃片没有掉下,证明瓶内气压大于大气压
B.玻璃片没有掉下,证明CO2与水发生了反应
C.振荡后试纸变红,证明CO2与水反应产生了酸
D.振荡后试纸变红,证明CO2能与石蕊反应变红
12.(2024·苏州)Na2CO3和NaCl的溶解度曲线如图所示。下列说法正确的是
(
050
Na,CO3
盘
NaCl
301
10
020T4060→
温度/℃
A.Na2CO3的溶解度随温度升高而增大
B.Na2CO3的溶解度一定比NaCl的大
C.T℃时,30gNaC1能完全溶解于50g水中
D.T℃时,Na2CO3和NaCl两种饱和溶液的溶质质量分数相等
得分
评卷人
二、非选择题(本大题包括5小题,共28分。)
13.(6分)(2024·云南)云南拥有丰富的非物质文化遗产。
(1)纳西族东巴纸的制作过程包括浸泡、蒸煮、春料、浇纸、晒纸等,其中“浇纸”是用滤网分离出纸
浆,该操作与化学实验中的
(填操作名称)相似。
(2)普洱茶制作技艺又称“贡茶制作技艺”。普洱茶茶香四溢,从分子角度对此现象的解释是
(3)白族扎染利用板蓝根作为主要染料,板蓝根中含有靛蓝(C16HoN2O2),靛蓝属于
(选
填“有机物”或“无机物”),其中氮、氢元素的质量比为
·17-3·
(4)阿昌族户撒刀始终保持着手工制作的特点,“淬火”是制作过程中最为突出的技艺。“淬火”的
原理是高温下铁和水蒸气反应生成四氧化三铁和氢气。该反应的化学方程式为
,该反应属于
(填基本反应类型)。
14.(5分)(2024·广元)如图是实验室制取气体的常用装置,请回答下列问题:
氢氧
里化钠
溶液
酸
B
D
E
(1)标号a的仪器名称是
(2)选用A、D装置制取氧气的化学方程式为
(3)在加热的条件下,铜与浓硫酸可反应生成SO2。SO2是一种密度比空气大的有毒气体,其部
分化学性质与CO2相似。若要制取SO2,可选择发生装置
(填字母代号)。若用G
装置收集SO2,气体应从
(选填“m”或“n”)端进入。制取SO2过程中,为防止污染环
境,还应选择
(填字母代号)装置进行尾气处理。
15.(6分)(2024·烟台)电动汽车的兴起对金属镁和碳酸锂(Li2C03)的需求增大。以盐湖卤水(主
要成分是MgCl2、NaCl、LiCl)为原料,制备金属镁和碳酸锂的主要物质转化流程如图:
加稀盐酸
通电
Mg(OH)2
MgCL,溶液
MgCl2
Mg
盐湖加适量X
加Na,C0,溶液
卤水
过程I
富锂溶液
Li,C0,固体
过程Ⅲ
滤液1
过程Ⅱ
NaCl晶体
资料:①碳酸钠能与氯化镁发生复分解反应;②部分物质的溶解度如表:
物质
LizCO
MgCO:
LiOH
LiCl
MgCl2
Mg(OH)2
20℃时溶解度/g
1.32
0.039
12.8
77
54.8
难溶
(1)为避免引入新杂质,过程I中加入的适量物质X是
(2)制镁过程中发生中和反应的化学方程式是
0
(3)过程Ⅱ的目的是浓缩含锂溶液。这个过程中,氯化钠的结晶方法是
(选填“蒸发
结晶”或“降温结晶”)。
(4)过程Ⅲ发生了复分解反应,其反应的化学方程式是
(5)用盐湖卤水制取碳酸锂,要先除去卤水中的氯化镁,其原因是
16.(6分)(2024·新疆)水果、蔬菜等在生长及运输过程中可能会使用到杀虫剂、防腐剂等,食用前需
要去除残留,果蔬洗盐能达到此效果。学校兴趣小组同学对某临期果蔬洗盐在成分及含量上是
否变质进行研究。
·17-4·
【阅读标签】如图所示:
产品参数
【配料】碳酸氢钠、食盐、碳酸钠
【保质期】24个月
【净含量】350克
【贮存条件】
【查阅资料】
(1)碳酸钠溶液与氯化钙溶液反应产生白色沉淀。
(2)碳酸氢钠在50℃以上逐渐分解产生二氧化碳、碳酸钠和水;碳酸钠受热不分解。
(3)浓度大于0.83%的碳酸氢钠溶液中加入0.1%的氯化钙溶液,产生白色沉淀;浓度小于
0.83%的碳酸氢钠溶液中加入0.1%的氯化钙溶液则无现象。室温下,碳酸氢钠饱和溶液的
浓度为8.8%。
【任务一】验证该临期果蔬洗盐的成分
【作出猜想】
猜想1:该临期果蔬洗盐中除了NaCl外,可能还有Na2CO3。
猜想2:该临期果蔬洗盐中除了NaCI外,可能还有
猜想3:该临期果蔬洗盐中除了NaCl外,可能还有NaHCO3。
【实验验证】
实验操作
实验现象
实验结论
实验1:取样溶于水,滴加无色酚酞溶液
溶液
溶液呈碱性
实验2:取样加热,将产生的气体通入澄清石灰水
澄清石灰水变浑浊
含有
实验3:为使现象明显,取样溶于水,并用玻璃棒搅
产生白色沉淀
含有Na2COg
拌形成饱和溶液,加入0.1%的CaCl2溶液
【交流反思】
实验3中玻璃棒搅拌的作用是
小组同学认为实验3中结论不严谨,理由是
【实验验证】
为保证实验的严谨性,小组同学进一步探究。
实验操作
实验现象
实验结论
含有Na2CO3、化学方程
实验4:另取8g样品与992g水配制成溶液,向
产生白色沉淀
式为
其中滴加0.1%的CaC12溶液
·17-5·
【实验结论】
猜想2正确
【任务二】验证该临期果蔬洗盐的成分含量变化
【实验方案】查阅资料、实验探究、数据分析。
【实验结论】确定该临期果蔬洗盐中碳酸钠的质量分数增大。
【注意:若答对以下小题奖励3分,化学总得分不超过40分。】
【交流反思】由于该样品长期放置在灶台旁受热引起变质。请根据资料信息写出变质所涉及的化
学方程式
【迁移应用】
推测此类果蔬洗盐的贮存条件:
【拓展延伸】
小明的弟弟比较顽皮,将盛放食盐与果蔬洗盐的容器标签损毁,请借助家庭中的生活用品或食品
等设计方案进行区分:
(写明所选物品、现象及结论)。
17.(5分)(2024·吉林)1839年,林则徐在虎门海滩主持销烟,显示了中华民族反抗外来侵略的坚强
意志。这次销烟过程利用了生石灰(CO)与水反应的原理。化学活动小组依据这一原理设计了
系列实验,请参与计算:
(I)CaO中钙元素和氧元素质量的最简整数比为
(2)利用化学方程式计算:56g的CaO与H2O恰好完全反应生成Ca(OH)2时,参加反应的H2O
的质量。
。17—6
资源预览图

1

2
3
相关资源
由于学科网是一个信息分享及获取的平台,不确保部分用户上传资料的 来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系学科网,我们核实后将及时进行处理。

