福建省厦门市第六中学2024-2025学年高二下学期3月月考化学试题
2025-03-22
|
9页
|
318人阅读
|
7人下载
资源信息
| 学段 | 高中 |
|---|---|
| 学科 | 化学 |
| 教材版本 | - |
| 年级 | 高二 |
| 章节 | - |
| 类型 | 试卷 |
| 知识点 | - |
| 使用场景 | 同步教学-阶段检测 |
| 学年 | 2025-2026 |
| 地区(省份) | 福建省 |
| 地区(市) | 厦门市 |
| 地区(区县) | - |
| 文件格式 | |
| 文件大小 | 5.15 MB |
| 发布时间 | 2025-03-22 |
| 更新时间 | 2025-03-22 |
| 作者 | 匿名 |
| 品牌系列 | - |
| 审核时间 | 2025-03-22 |
| 下载链接 | https://m.zxxk.com/soft/51186373.html |
| 价格 | 1.00储值(1储值=1元) |
| 来源 | 学科网 |
内容正文:
福建省厦门第六中学2024一2025学年第一学期化学学科3月月考
厦门六中2023级高二3月测试
化学
考试时间:75分钟
相对原子质量:1C-12B-11N-140-16Mg-24Si-28C1-35.5Fe-56Cu-64
一、选择题(本题包括15小题,每小题3分,共45分,每小题只有一个选项符合题意)
1.下列化学用语或模型正确的是
A邻羟基苯甲醛的分子内氢键:
B.NH的结构式:
C.SnBn分子中Sn的杂化类型是sp3
D.SO32的VSEPR模型:
2.根据元素周期律,下列说法不正确的是
A.化合物中离子键百分数:AO3>MgO
B.化合物中键的极性:SiCl4>PCl3
C.碱性:KOH>LiOH
D.第一电离能:GeSe<As
3.BCL,可以以单体、二聚体和多聚体的形式存在.下列关于BcCl,的说法不正确的是
G-R-GG-G
单体
二聚体
多聚体
A.单体的空间构型是直线形,属于含极性键的非极性分子
B.二聚体和多聚体中均存在Be→C配位键
C.单体、二聚体、多聚体中Be的杂化方式分别是psp2、sp3
D.单体的沸点比二聚体低
4.下列有关63℃u的基态原子说法错误的有
①位于周期表d区
②电子占据15个原子轨道
③6.3g基态63Cu2*的未成对电子数为0.1Na
④占据6个能级
⑤基态3Cu原子的
2比基态Zn原子小⑥价电子排布式为3d4s2
A.①③④⑥
B.①④⑤⑧
C.②③⑤⑥
D.①②④⑤
第1页共8页
福建省厦门第六中学2024一2025学年第一学期化学学科3月月考
5.下列图像表示正确的是
键能
◆沸点
键的极性
键角
HCIHBr
B
NH PH,
H-/H-
NH,
H
0
H-C
H,0
AsH
SiHa
卤素原子半轻
相对分子质量
H-X键中X原子序数
中心原子的弧电子对数
6.下列关于[CrNH3)3(H2O)2zC2*说法错误的是
瓜.基态Cr3的核外电子排布式为Ar]38
B.基态氯原子核外电子共有9种不同的空间运动状态
C.NH和H20的中心原子价层电子对空间构型相同
D.键角和沸点都是NH3>H2O
7.二氧化二硫(S2C)是一种黄红色液体,分子中各原子最外层均有8个电子。它的分子结
构与H202相似,下列说法正确的是
A.52C2与5C2分子中的硫原子均采取sp杂化
B.5dk电子式为Cl::5:C
C.SzC2是含有极性键的非极性分子
D.SzC2的相对分子质量比H202大,熔、沸点:S2Cl2>H2Oz
&.一种可吸附甲醇的材料,其化学式为CNH2a4[B(OCH4C1,部分晶体结构如下图所
示,其中[C(NH2]为平面结构。下列说法正确的是
A,晶体中B、N和O原子轨道的杂化类型相同
B.该晶体中存在N-HO氢键
C.基态原子未成对电子数:B<C<O<N
D.基态原子的第一电离能:C<N<O
第2页共8页
福建省厦门第六中学2024一2025学年第一学期化学学科3月月考
9.联氨(NH)可用于镜面镀银,其原理为AgI2r+Nh-Ag!+N2t+NA+NH3(未配平),
设A为阿伏伽德罗常数,下列说法错误的是
A32gNH中非极性键的数目为NA
B.1 mol NHaNO,晶体中c键的数目为7NA
C.1L0.01 mol-L[Ag(NHa2JNo3溶液中Ag*的数目为0.01mol
D.该反应中每转移1mol电子生成N2的数目为0.25NA
10.下列叙述及解释均正确的是
事实
解释
A
F的热稳定性比HCI强
HF可形成分子间氢键而HC1不能
B
碱金属中的熔点最高
碱金属中L的价电子数最少,金属键最强
气态M如2“再失去一个电子比气态
M血2+的价层电子排布为3d5,3d轨道为半充
F“再失去一个电子更难
满的稳定状态,较难失去电子
D
NCL,与BCl3分子的空间构型相同
二者中心原子杂化轨道类型都是$p
11.酸性溶液中过氧化氢能使Cr20转化成蓝色的过氧化铬(Cr05,分子结构为
该反应可用来检验Cr20号的存在,其反应的离子方程式为4州20z+Cr20号+2H=2Cr0s+5H20。
下列说法不正确的是
A.CO5分子中既有极性键又有非极性键
B.1 mol Cr(05分子中含有o键数为7N
C.该反应中Cros表现了氧化性
D.过氧化铬中铬元素的化合价为十6
12.种金属有机框架材料的化学式为M2ZXW)4,其结构如图。X、Y、Z、M为原子序数依
次增大的136号元素,期中X、Z位于不同周期,四种元素中Y的第一电离能最大,M
的d轨道全充满,下列说法正确的是
A.键角:Z>ZXW
B.最简单氢化物沸点:ZDY>X
C.电负性:XDM
D.最高价氧化物对应的水化物酸性:Z>X
第3页共8页
福建省厦门第六中学2024一2025学年第一学期化学学科3月月考
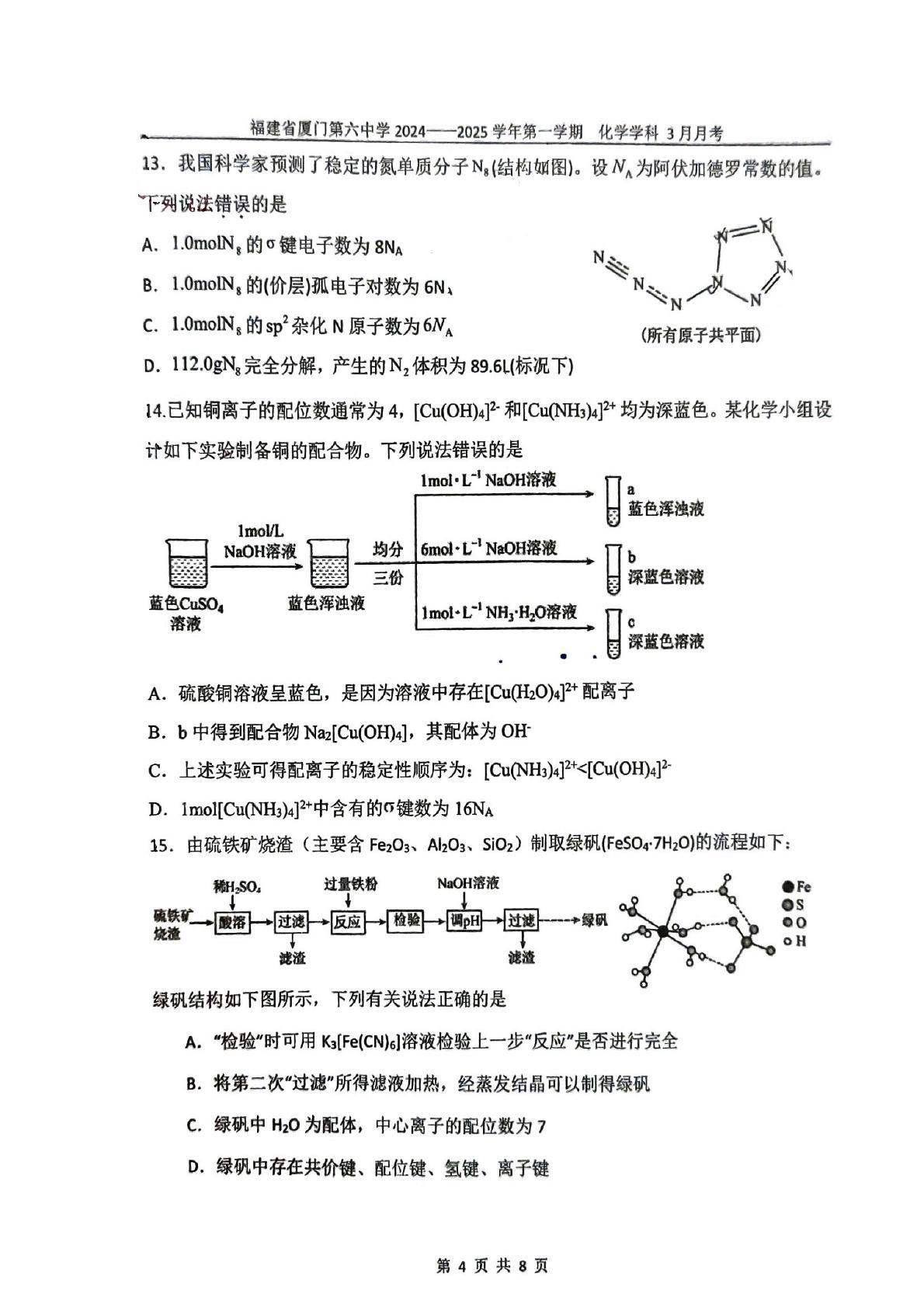
13.我国科学家预测了稳定的氮单质分子N,(结构如图)。设N为阿伏加德罗常数的值.
下列说法错误的是
A.1.0moN,的c键电子数为8Na
B.1.0moN,的价层)孤电子对数为6N,
C.1.0moN,的sp杂化N原子数为6NA
(所有原子共平面)
D.112.0gN完全分解,产生的N2体积为89.6L(标况下)
14.已知铜离子的配位数通常为4,[Cu(OH田]2和[CuNH)4]2+均为深蓝色。某化学小组设
计如下实验制备铜的配合物。下列说法错误的是
1mol.L NaOH溶液
蓝色浑浊液
1mol/L
NaOH溶液
均分
6mol·L1NaOH溶液
磁
三份
深蓝色溶液
蓝色CuS0
蓝色浑浊液
溶液
1 mol-L-NH,H20溶液
深蓝色溶液
A.硫酸铜溶液呈蓝色,是因为溶液中存在[CuHO)4]+配离子
B.b中得到配合物Na[Cu(OH田4],其配体为OH
C.上述实验可得配离子的稳定性顺序为:[CuNH)4<[Cu(OH)4]
D.1mol[Cu(NH)4]2+中含有的G键数为16Na
15.由硫铁矿烧渣(主要含FezO3、Al203、Sio2)制取绿矾(FeS0r7HzO)的流程如下:
陆S0
过量铁粉
NaOH溶液
Fe
os
整阔一甲-國图应吧
00
oH
滤渣
滤渣
绿矾结构如下图所示,下列有关说法正确的是
A.“检验"时可用K3[Fe(CN)6J溶液检验上一步“反应"是否进行完全
B.将第二次“过滤“所得滤液加热,经蒸发结晶可以制得绿矾
C,绿矾中H20为配体,中心离子的配位数为7
D.绿巩中存在共价键、配位键、氢键、离子键
第4页共8页
福建省厦门第六中学2024一025学年第一学期化学学科3列号月考
二、填空:
16.(15分)请回答以下问题:
()第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素对应的基态
原子共有
种不同能量的电子。
电离能Umod
沸点RC
13630
100
10540
50
7733
-150
2345周期
图1
图2
(②)如图2所示,每条折线表示周期表IVA-VIIA中的某一族元素氢化物的沸点变化。每
个小黑点代表一种氢化物,其中a点代表的是
(填化学式)。
(3)第一电离能介于A1、P之间的第三周期元素有
种。GaC3原子的杂化方式为
。写出一种与GaCl3互为等电子体的阴离子:
(4)某醋酸盐晶体局部结构如下图,该晶体中含有的化学键是
(填字母标号)。
a极性键b.非极性键
c.配位键d金属键
c.氢键
(5)MO,可作M转化为FDCA的催化剂(见左下图)。FDCA的熔点远大于MF,除相
对分子质量存在差异外,另一重要原因是
BF
FDCA
[BMIMT BF,
(6)BMIM]'BF(见右上图)是MnO,晶型转变的诱导剂。BF的空间构型为
BMM们中咪唑环存在π大π键,则N原子采取的轨道杂化方式为
(7)三价铁的强酸盐溶于水后经水解可以生成如下图所示的二聚体,其中℉®+的配位数
为
,过渡元素的s、P、d轨道可以参与杂化,含s、p、d轨道的杂化类型有:①dsp2、
②spd、③sp'd,④sp该二聚体中Fe采取的杂化类型为
(填标号)。
OH
H.C
福建省厦门第六中学2024一2025学年第一学期化学学科3月月考
17.(14分)氮族元素(N、P、As、Sb等)及其化合物在工农业生产、环境等方面有
重要应用。
I.氨族元素氢化物RH(NH、PH、AsH)的某种性质随R的核电荷数的Y变化趋势如
右图所示。
(I)Y轴可表示的氢化物(H)性质可能是
Y
NH,
a.沸点b.稳定性c.分子间作用力d.R一H键能
H
AH,
(2)AsH的电子式为
·核电鸢数
ⅡN、P的单质及化合物有重要的用途。请回答:
(3)白磷P)为正四面体结构,P4分子中P原子的价层电子对数为
,从能量角度看,
氮以N2而白磷以P4形式存在的原因是
化学键
N-N
NeN
P-P
P=P
键能kJ/mol
193
946
197
489
(4)Ns离子的空间结构如右图所示(孤电子对已标出),其空间构型为V形,则N原子a的
杂化类型为
,N原子b的杂化类型为
(⑤)下列说法中正确的是一·
A.电负性:N>P>Si
B.因为N-H键键能大于P-H键,故NH,的沸点高于PH
C.由于成键电子对间的斥力较小,PH3的键角小于NH的键角
D.氧化物对应水化物的酸性:NP
(6)①甘氨酸(结构简式为HNCH2COOH和氢氧化铜反应可制得重要的饲料添加剂甘氨酸
铜,在甘氨酸分子中,存在
个6键,个键(填数字).
②甘氨酸铜有两种结构(如下图),已知两种结构中Cu周围的4个原子共平面,则Cu的
杂化方式是sp吗?
(填“是”或否”,在水中溶解度较大的是(填“A”或“B")。
0
H N
CH
H.C
CH,
H,C.
NH2 H2N
0
顺式甘氨酸铜(A)》
反式甘氨酸铜(B)
第6页共8页
相建省厦门第六中学2024一2025学年第一学期化学学科3月月考
18.(15分)1.硅材料在生活中占有重要地位。
()SiNH)4(以Si为中心)分子中硅原子的杂化轨道类型是
Si(NHz)4受热分
解生成SiN4和NH,其受热不稳定的原因是:
(2)由硅原子核形成的三种微粒,电子排布式分别为:①Nc]3s23p2、②N©3s23p'、
③Ne3s23p4s',有关这些微粒的叙述,正确的是
A.微粒半径:③>①>②
B.电子排布属于基态原子(或离子)的是:①②
C.电离一个电子所需最低能量:①>②>③
D.得电子能力:①>②
Ⅱ.含Cu、Z、Sn及的四元半导体化合物(简写为CZTS),是一种低价、无污染的绿色
环保型光伏材料,可应用于薄膜太阳能电池领域。回答下列问题:
(3)基态S原子的价电子中,两种自旋状态的电子数之比为
(4)SnCl的几何构型为
,其中心原子杂化方式为
(⑤)将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质。下
列物质中,属于顺磁性物质的是
A.[Zn(NH3)4]S04
B.[Cu(NH3)4]SO4
C.[Cu(NH3)2]CI
D.Naz[Zn(OH)4]
(6如图是硫的四种含氧酸根的结构:
[&
根据组成和结构推断,能在酸性溶液中将Mn2*转化为MnO4的是
(填标号),
理由是
Ⅲ.金属镓(G)应用广泛,在半导体和光电材料、合金、磁性材料等领域都有重要应用。
像与铝是同主族元素,性质相似。
(T基态Ga原子的价电子排布式是
(8)GaAs是一种重要的半导体材料,可以用浓硝酸溶解GaAs,生成HAsO,和Ga+,写
出该反应的化学方程式
第7页共8页
福建省厦门第六中学2024一2025学年第一学期化学学科3月月考
19.(1分)精炼铜产生的铜阳极泥富含Cu、Ag、Au等多种元素。研究人员设计了一种
从铜阳极泥中分离提取金和银的流程,如下图所示。
NazS2O,
疏酸、H202
盐酸、H,O
浸渣2
浸出液3
浸取3
电沉积艹Ag
浸渣1
铜阳极泥
浸取1
浸取2
还原
Au
浸出液2
浸出液1
N2H4 N2
(1)Cu位于元素周期表第
周期第
族。
(2)“浸出液1“中含有的金属离子主要是
(3)浸取2"步骤中,单质金转化为HAuCla的化学方程式为
(4)浸取3”"步骤中,“浸渣2“中的
(填化学式)转化为Ag52Q62]P。
(⑤)"电沉积"步骤中阴极的电极反应式为
“电沉积”步
骤完成后,阴极区溶液中可循环利用的物质为
(填化学式)。
(6)"还原"步骤中,被氧化的N2H4与产物Au的物质的量之比为」
(7)Na2SzO可被h氧化为Na2SO6。从物质结构的角度分析S4Og的结构为
i时oo
第8页共8页
L门六中20242025学年高二下学期3月月考答案
化学答案
一,造择题(俸小周3分,共45分):
123456789101112131415
DA+B BC DA B CCC D A
二,非造择题55分)
16.(15分)
(4(2分)
2SiH出(1分)
(3)3(2分);sp2(1分):C02或N0(1分)
(4)abc(2分)漏选错选扣1分
(EDCA形成的分子间氢键更多(2分)
(⑤)正四面体(1分);s即(1分)
(76(1分):③(1分)
17.(14分)
(1bd.(2分)
(2)
(1分)
(③)4(r分);N转化为N的反应为吸热,P转为P,为放热反应或6条PP单键键能总和大于2
个PP三键键能和,而NN三键键能大于3个N-N键能总和。(2分)
(④即(1分);p2(1分)
(⑤AC(2分)】
(⑥①9(1分):1(1分);②否(1分);A(1分)
18.(15分)
(1)sp(1分);Si周围的NH2基团体积较大,受热时斥力较强,Si0NH)4中Si-N键能相对较小,
生成的SN很稳定,该反应是熵增的反应等合理答案。(2分)
(2)AB(2分)
(3)21或1:2(1分)
(4)三角锥形(1分);s即(1分)
(⑤)B(1分)
(6D(1分);D中含有-1价的0,易被还原,具有强氧化性,能将Mm2转化为M0:(2
分)
T⑦4s24p'(1分)
(8GaAs+11HNO=HAs0+Ga0NO)+8NO2↑+4H,0(2分)
19.(11分)
(14(1分);1B(1分)
(20*(1分)
(3)2Au+8HC+3H,02=2 HAuCL+6H0(2s分)】
(④AgC(1分)】
(5AgS,0hP+e=Ag+2S,0,2(2分);NaS,03(1分)
63:4(1分)
(7)a(1分)
1
资源预览图

1

2

3
4
所属专辑
相关资源
由于学科网是一个信息分享及获取的平台,不确保部分用户上传资料的 来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系学科网,我们核实后将及时进行处理。
