四川广安市岳池县第一中学2025-2026学年第二学期第二次月考 高一化学试卷
2026-05-17
|
9页
|
13人阅读
|
0人下载
资源信息
| 学段 | 高中 |
|---|---|
| 学科 | 化学 |
| 教材版本 | 高中化学人教版必修第二册 |
| 年级 | 高一 |
| 章节 | - |
| 类型 | 试卷 |
| 知识点 | - |
| 使用场景 | 同步教学-阶段检测 |
| 学年 | 2026-2027 |
| 地区(省份) | 四川省 |
| 地区(市) | 广安市 |
| 地区(区县) | 岳池县 |
| 文件格式 | |
| 文件大小 | 670 KB |
| 发布时间 | 2026-05-17 |
| 更新时间 | 2026-05-17 |
| 作者 | 匿名 |
| 品牌系列 | - |
| 审核时间 | 2026-05-17 |
| 下载链接 | https://m.zxxk.com/soft/57906596.html |
| 价格 | 1.00储值(1储值=1元) |
| 来源 | 学科网 |
内容正文:
岳池一中高2025级第二学期第二次月考化学试卷
出题人:廖春华审题人:郑时国
注意事项:
1、本试卷满分100分,考试时间75分钟。
2、答卷前,考生务必将自己的姓名、考号填写在答题卡上。
3、回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案
标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,
将答案写在答题卡上,写在本试卷和草稿纸上无效。
可能用到的相对原子质量:A127
一、单选题(每小题3分,共45分)
1.为保护我们岳池县美丽的生态环境,下列做法或说法正确的是
A.澄清的工业废水可以直接排放B.保护生态环境,禁止使用农药和化肥
C.天然气燃烧的产物易形成酸雨D.大力植树造林可减少沙尘天气的发生
2.人形机器人再次登上2026年春晚的舞台,在武术节目《武bot》中与少林武
僧同台,完成后空翻、耍双节棍、精准走位等高难度动作,将传统武术与智能完
美融合,展现中国科技实力与传统文化的创新结合。机器人的制造过程中用到多
种材料,下列说法错误的是
A.机身主体使用的航空级铝合金和钛合金具有高强度、高刚性、良好的散热
性等特点
B.机器人采用的芯片成分为二氧化硅
C.选用锂聚合物电池,实现将化学能转化成电能
D.散热涂层采用的石墨烯是一种新型无机非金属材料
3.甲烷是最简单的有机化合物,很早就被人类发现。化学家为搞清楚甲烷的结
构却用了上百年的时间,用下列图示来表示甲烷的结构,其中最合理的是
A
B
C.H-C-H
4.N。表示阿伏加德罗常数,下列说法正确的是
A.1 molSO,与0.5molO,充分反应后可生成SO3分子数为NA
B.常温条件下,2.7g铝与浓硝酸完全反应生成的NO,分子数为0.3NA
C.0.5mol/LNa,SO4溶液中含有的Na+数目为Na,
D.3 moINO,与水反应转移电子数为2NA
第1页,共8页
5.关于反应2NH,OH+4Fe3+=N,O个+4Fe2++4H+H,O,下列说法正确的是
A.该反应的氧化产物是N,OB.该反应中NH,OH体现了氧化性
C.NH,OH中N是-3价
D.若设计成原电池,Fe+将在负极得电子
6.下列有关有机物的说法正确的是
A.正戊烷分子中所有碳原子在一条直线上
H
B.CH,Cl的电子式:H:C:cI
C.C,H6和C4H0一定互为同系物
H
D.H-
-c互为同分异构体
7.反应A(g)+2B(g)三C(g)+2D(g),在四种不同情况下的反应速率如下,其
中反应进行最快的是
A.v(A)=0.2 mol.L.min
B.v(B)=0.6 mol.L.min
C.v(C)=0.4 mol.L.min1
D.v(D)=0.02mol.L1.s1
8.常温下,下列各组离子在指定溶液中能大量共存的是
A.纯碱溶液:K+、SO、NO
B.KOH溶液:NHNa+、SO
C.含有大量H+的水溶液:Fe+、CI、NO
D.透明溶液:K+、HSO,、OH
9.在密闭容器中发生反应:X(g)十3Y(g)三2Z(g),若X、Y、Z的起始浓度分
别为0.2molL1、0.6mol.L1和0.4molL1。一定条件下,当反应达到一定限度
时,各物质的浓度可能是
A.X为0.4mol.L1
B.Y为0.5mol.L1
C.Z为0.8mol.L1
D.Z为0.2molL1时,Y为0.8molL1
10.下列离子方程式书写正确的是
A.铅蓄电池放电时正极的电极反应式:PbO,+4H+2e=Pb++2H,O
B.向Na,S,O3溶液中加入稀硫酸:3S,O+2H+=4S↓+2SO,个+H,O
C.向BaCl,溶液中通入SO,气体:Ba2++SO,+H,O=BaSO,↓+2H+
D.将过量SO,通入澄清石灰水中:OH+SO,=HSO
11.如图所示的原电池装置,X,Y为两电极,电解质溶液为稀硫酸,外电路中
的电子流向如图所示,对此装置的下列说法正确的是
A.若两电极都是金属,则它们的活动性为X>Y
X
B.若两电极分别为Zn和石墨棒,则侧X为石墨棒,Y为Zn
C.外电路的电流方向为:X→外电路→Y
D.X极上发生的是还原反应,Y极上发生的是氧化反应
第2页,共8页
12.下列实验装置不能达到实验目的的是
浓硫酸
又湿润红色
5
实验
NaOH浓溶液)
石蕊试纸
装置
样品试液、
蔗糖
鲜溴水
实验
A.用所示装置检验样品中是否含有
B.验证浓硫酸具有脱水性和氧
目的
NH;
化性
2滴FeCl,溶液
NH
实验
装置
热
止水夹
水(滴加少
2mL5%H202溶液
量酚酞)
实验
C.验证FeCl,对H,O,分解有催化作用
D.验证氨气的溶解性
目的
13.
依据事实类比推测是化学上研究物质的重要思想,下列类比推测合理的是
事实
类比推测
Mg、A1两棒用导线连接插入盐酸中,
Fe、Cu两棒用导线连接插入浓硝酸溶
A
A1棒表面出现气泡,这是由于活泼性:
液中,Cu棒表面出现气泡
Mg大于Al
Fe和S反应生成FeS
Cu和S反应生成Cu,S
SiO,既能和HF酸反应,又能和
A1,O,既能和HF酸反应,又能和
NaOH反应,故SiO,也属于两性氧化
NaOH反应,故Al,O3属于两性氧化物
物
D
CO,通入Ba(NO),溶液中没有现象
SO,通入Ba(NO),溶液中无明显现象
第3页,共8页
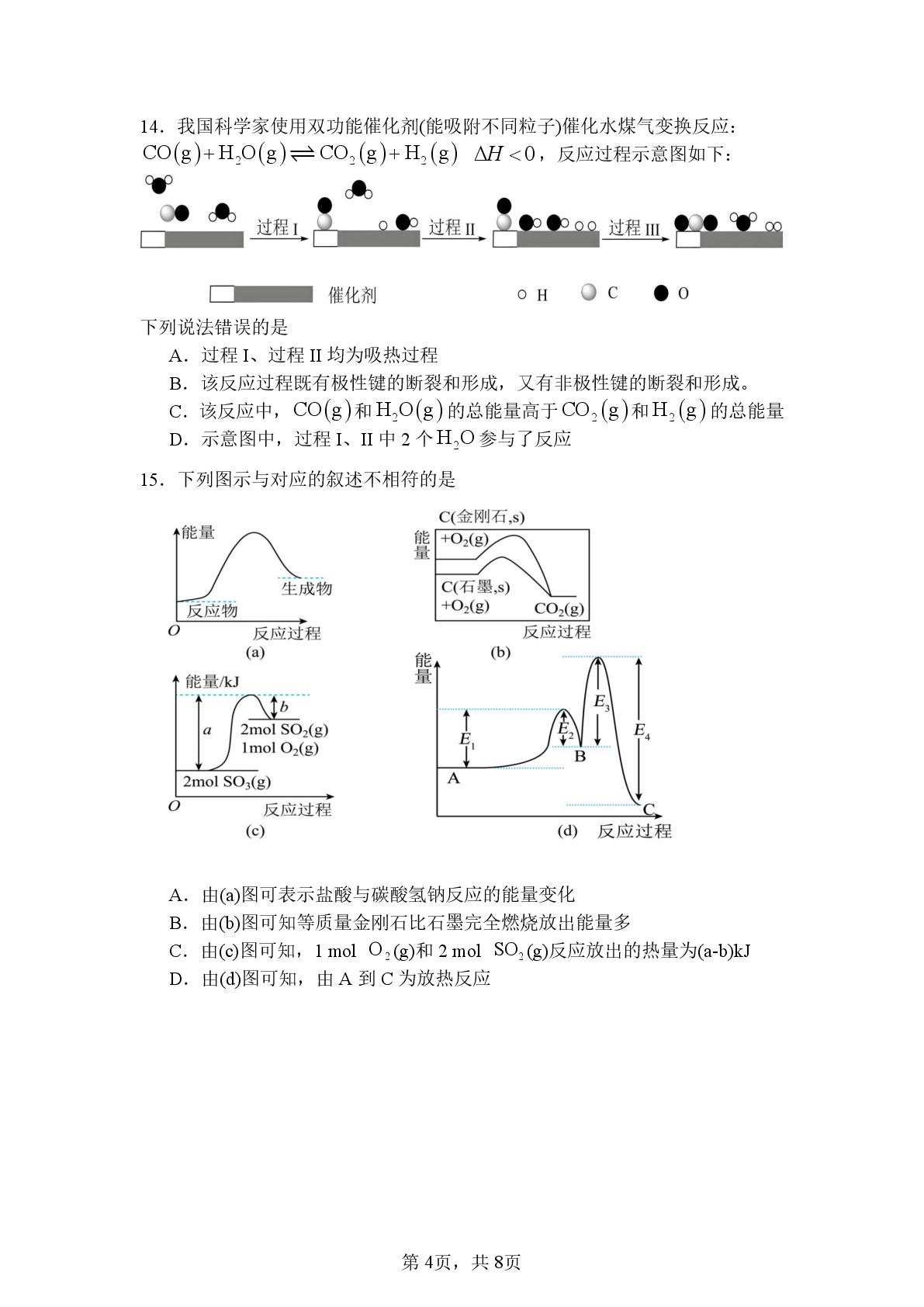
14.我国科学家使用双功能催化剂(能吸附不同粒子)催化水煤气变换反应:
CO(g)+HO(g)=CO,(g)+H,(g)△H<0,反应过程示意图如下:
过程I
过程Ⅱ
p●力o0过程Ⅲ
催化剂
O H
●0
下列说法错误的是
A.过程I、过程I均为吸热过程
B.该反应过程既有极性键的断裂和形成,又有非极性键的断裂和形成。
C.该反应中,CO(g)和H,O(g)的总能量高于CO,(g)和H(g)的总能量
D.示意图中,过程I、IⅡ中2个H,O参与了反应
15.下列图示与对应的叙述不相符的是
C(金刚石,S)
个能量
能
+02(g)
量
生成物
C(石墨,s)
发应物
+02(g)
CO2(g)
反应过程
反应过程
(a)
(b)
个能量/kJ
螚
a
2molS02(g)
1mol O2(g)
2mol SO3(g)
反应过程
(c)
(d)
反应过程
A.由(a)图可表示盐酸与碳酸氢钠反应的能量变化
B.由b)图可知等质量金刚石比石墨完全燃烧放出能量多
C.
由(c图可知,1molO,(g)和2 mol SO2(g)反应放出的热量为(a-b)kJ
D.由(d)图可知,由A到C为放热反应
第4页,共8页
二、填空题(共55分)
16.非金属及其化合物在生产、生活和科学研究中应用广泛。
(1)硅酸盐材料是传统无机非金属材料,下列产品不属于硅酸盐的是
(填序
号)。
①玻璃②石英玻璃③陶瓷④硅芯片⑤光导纤维⑥水泥
(②)SiO是玻璃的主要成分之一,SiO2与氢氧化钠溶液反应的化学方程式为
,工艺师常用
(填物质名称)来雕刻玻璃。
(3)Na,SiO3可通过SiO,与纯碱混合高温熔融反应制得,高温熔融纯碱时下列坩
埚可选用的是
A.普通玻璃坩埚B.石英玻璃坩埚C.铁坩埚
(4)工业上采用接触法制硫酸,硫铁矿(主要成分为FS,)在沸腾炉中和氧气在高
温条件下充分混合发生反应生成$O,反应的化学方程式为
(⑤)浓硫酸是实验室中常见的干燥剂,下列气体不能用浓硫酸干燥的是
(填标
号)
A.SO2
B.Cl,
C.H,S
D.H,
17.氮氧化物能引发酸雨、雾霾等,需处理后才能排放。研究含氮物质的转化是
工业、农业、医药、环保等领域的重要课题。O、NO3的处理方法通常有两种:
(1)氨转化法
某实验小组利用如图所示装置探究NH,能否被NO2氧化(K,、K,为止水夹,
夹持固定装置略去)。
浓氨水
浓硝酸
生石灰
铜片、
E
已知:甲试剂为碱石灰,乙试剂为无水氯化钙
①E装置中制取气体的离子方程式是
②常温下,若NO2能够被NH3还原,预期C装置中能观察到的现象是
③从环保角度,此实验装置存在一个明显的缺陷是
第5页,共8页
(2)氧化吸收法
酸性条件下,加NaC1O溶液可以氧化NO、NO和NO2等生成CI和NO。其
他条件一定,N,O转化为NO的转化率随水体溶液初始pH的变化如图所示。
100
%
70
60
6
8
1012
pH
①N,O为不对称结构,其化学键与CO,相似写出NO的结构式
②在酸性水体中加入NaC1o溶液吸收N,O的离子方程式为
③NaClo/HO2酸性复合吸收剂可有效去除NO。复合吸收剂组成一定时,温度
对NO去除率的影响如图。温度高于60C后,NO去除率下降的主要原因是。
100
90
19
50
60
温度/C
(3)碱液吸收
用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
NO,+NO+2NaOH=2NaNO,+H,O;
2NO,+2NaOH=NaNO,+NaNO,+H,O。现有VL某NaOH溶液能完全吸收含
nmoINO和molNO,的大气污染物,则NaOH溶液的物质的量浓度至少为
mol/L。
18.1.按要求回答下列问题:
(1)下列变化中,反应物的总能量低于生成物总能量的是
(填序号),写出
⑧的电离方程式
①铝片与稀盐酸的反应;②将胆矾加热变为白色粉末;③干冰汽化:④甲烷
在氧气中的燃烧反应;⑤NH4NO3固体溶于水;⑥二氧化碳和炽热的碳反应;
⑦碳酸氢钠与稀盐酸反应;
⑧KHSO4熔融
第6页,共8页
(2)合成氨工业中,合成塔中每产生2 nolNH3,放出92.2kJ热量,已知断开1molH-H
键、1molN=N键分别需要吸收的能量为436kJ、945.8kJ;则1molN-H键断裂吸
收的能量约等于
kJ。
Ⅱ.利用氢氧燃料电池可以将O2转化成重要的化工原料过氧化氢,装置如图。
电
极
极
y
稀硫酸
(3)上述装置中,电极A为(填正”或“负)极
(4)电极B上发生的电极反应式为
。电池工作时,电极A附近溶液的酸性
(填增强减弱或不变)。
(⑤)同温同压时,通入的气体X、Y的体积之比为
19.研究化学反应的速率和限度对促进生产具有重要的意义。
I.CH4、CO等都是重要的能源,也是重要的化工原料,一定条件下,甲烷与
水蒸气发生反应:CH4(g)+HO(g)、三CO(g)+3H(g),工业上可利用此反应生产
合成氨原料气H2。一定温度下,向2L恒容密闭容器中充入1.6 mol CH4(g)和2.4mol
HO(g)发生上述反应,CO(g)的物质的量随时间的变化如图所示。
n(CO)/mol
1.2
2时间/min
(1)0~2min内的平均反应速率vH)=
molL1min1。平衡时容器内气体
的总物质的量与起始时容器内气体的总物质的量的比值为
,平衡时
CH4的转化率为
(2)下列措施能加快反应速率的是
(填字母)。
A.恒压时充入He
B.升高温度
C.恒容时充入CH4
第7页,共8页
(3)下列能说明上述反应达到平衡状态的是(填字母)。
A.V(CH4)=3v(H2)
B.恒温恒容时,容器内混合气体的密度保持不变
C.CH4(g)、HO(g)浓度保持不变
D.断开3molH-H键的同时断开2molO-H键
Ⅱ.利用催化技术可将汽车尾气中的CO和NO转化为CO2和N2,化学方程式为:
2N0+2C02C0,N,在反应物初始浓度相同,突验温度为20℃和90℃
条件下,进行以下实验:
实验
同种催化剂的比
达平衡时所用
实验目的
温度(C)
编号
表面积(mg)
时间(s)
1
对照试验
200
50
t
研究催化剂的比表面
2
积对尾气转化速率的
200
80
t
影响
3
a
300
b
【实验分析与结论】
(④)补全表格:a.
6
(⑤)通过实验可得到温度相同时,增大催化剂的比表面积,可增大尾气的转化速
率的结论,证据是对比实验t1
t2(填>x<”或=)。
第8页,共8页
岳池一中高2025级第二学期第二次月考化学试卷
参考答案
一、单选题(每题3分,共45分)
题号
1
2
3
4
5
6
7
8
答案
D
B
D
D
A
C
D
A
题号
9
10
11
12
13
14
15
答案
B
D
A
C
B
B
C
二、填空题(除标注外,每空2分,共55分)
16.(共12分)
(1)②④⑤
(2)SiO2+2NaOH-Na2SiO3+H2O
氢氟酸
(3)C
(4)4FeS,+110
高温
Fe,O3+8S0,
(5)C
17.(共14分)
(1)Cu+4H*+2NO3=2NO,T+Cu*+2H,O
锥形瓶中混合气体颜色变浅
或消失
缺少尾气吸收装置
(2)N=N=0
4C1O+N,0+H,O=2H++4C1+2NO
H,O,在温度较高时
容易分解,导致其浓度减小,去除率降低
3)m+n)
V
18.(共14分)
(1)②⑥⑦
KHSO=K++HSO
(2)391
(3)负
(4)02+2e+2H+=H,02
增强
(5)1:1
19.(共15分)
(1)0.9
1.6(或8:5)
75%
(2)BC
(3)CD
(4)研究温度对尾气转化速率的影响
50
(5)>(1分)
答案第1页,共1页
资源预览图

1

2

3
4
相关资源
由于学科网是一个信息分享及获取的平台,不确保部分用户上传资料的 来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系学科网,我们核实后将及时进行处理。