广东汕头市潮阳区棉城中学2025-2026学年度高二下学期期中考试 化学试卷
2026-05-15
|
8页
|
32人阅读
|
3人下载
资源信息
| 学段 | 高中 |
|---|---|
| 学科 | 化学 |
| 教材版本 | - |
| 年级 | 高二 |
| 章节 | - |
| 类型 | 试卷 |
| 知识点 | - |
| 使用场景 | 同步教学-期中 |
| 学年 | 2026-2027 |
| 地区(省份) | 广东省 |
| 地区(市) | 汕头市 |
| 地区(区县) | 潮阳区 |
| 文件格式 | |
| 文件大小 | 8.93 MB |
| 发布时间 | 2026-05-15 |
| 更新时间 | 2026-05-15 |
| 作者 | 匿名 |
| 品牌系列 | - |
| 审核时间 | 2026-05-15 |
| 下载链接 | https://m.zxxk.com/soft/57887804.html |
| 价格 | 0.00储值(1储值=1元) |
| 来源 | 学科网 |
内容正文:
棉城中学2025-2026学年度高二下化学期中考试卷
考试时间:75分钟1
第I卷(选择题)
一、单选题
1、下列四种常见的物品中,属于晶体的是
A食盐
B玻璃
C透明塑料
D.炭黑
2.冠醚能与碱金属离子作用,并随环的大小不同而与不同的金属离子作用。18冠-6与K
作用(如图),但不与L计或Na*作用。下列说法正确的是
A.18-冠-6与K作用,不与Li或Na*作用,这反映
了超分子的“自组装”的特征
B.18-冠-6中0原子与K间存在离子键
C.18-冠-6中所有原子在同一平面
18-冠-6
超分子
D.烯烃难溶于水,被KM如O4水溶液氧化的效果较差。若烯烃中溶入冠醚18-冠-6,氧
化效果将明显提升
3.化学与社会、生活、科技密切相关。下列说法正确的是
A.“天问一号”实验舱—所使用的铝合金熔点高于其各组分金属
B.制造C919飞机的材料—氮化硅属于共价晶体
C.电视和电脑的液晶显示器使用的液晶材料属于晶体,表现出晶体的各向异性
D.乙烯可用作水果催熟剂,也是氧割焰的主要气体
4.化学助力科技。下列说法正确的是
A.“核磁共振波谱法”使用的15N与空气中的N2互为同位素
B.“碲化镉薄膜太阳能电池”能有效地将化学能转化为电能
试卷第1页,共8页
C.“"蛟龙号”载人深潜器采用的钛合金材料,属于无机非金属材料
D.“祝融号”火星车上采用的新型碳化硅材料为共价晶体
5.化学与生命科学密不可分。下列说法错误的是
A.
核糖与葡萄糖都是可水解的生物高分子化合物
B.血红素是配位化合物,中心离子是亚铁离子
C.聚乳酸具有生物可吸收性,可用于手术缝合线
D.人体细胞的双分子膜体现了超分子的自组装特征
6.《厉害了,我的国》“中国名片”中航天、军事、天文等领域的发展受到世界啊目。下列说
法正确的是
A.“中国天眼”的“眼眶”圈梁使用的钢铁属于合金
B.“复兴号”车厢连接处使用的聚四氟乙烯属于烃类
C.“神舟十一号推进系统材料中的氮化硼属于分子晶体
D.“天宫二号”存储器中的石墨烯和金刚石属于同位素
7、化学用语是学习化学的工具和基础。下列有关化学用语的表达正确的是
A、质量数为37的氯原子:37C1B.乙烯的填充模型:
C.C0,的结构式:O=C=O
D.次氯酸分子的电子式:H:C:0:
8.下列各组物质中,按官能团进行分类,属于同一类物质的是
OH
CHO
O-CH3
CH3
CH3
OH
CH2-OH·
0
CH;
0
D.-C-0-CH CH:-C-0-CH
试卷第2页,共8页
9、有一种烃可表示为
CH,CHCH,CH(CH,)CH,C(CH2CH,)
CH,CH,
CH;
则命名该烃时主链上
的碳原子数为
A.7
B.8
C.9
D.10
10.我国科学家在青蒿素研究方面为人类健康作出了巨大贡献。在青蒿素研究实验中,下
列叙述错误的是
CH
A.通过X射线衍射可测定青蒿素晶体结构
B.通过现代元素分析仪可获得青蒿素的实验式
C、通过红外光谱可推测青蒿素分子中的官能团
D.通过核磁共振氢谱可推测青蒿素相对分子质量
青蒿素
11.有机物A的核磁共振氢谱图如图所示,则A可能是
A.CH,OCH,B.CH,CH,OCH,
c.CH,CH,OHD.CH,CH(CH),
4+3218/ppm
CH3 CH3
A的核磁共振氢谱
12.某烷烃的结构简式为CH-CH2-C一CH-CH,其系统命名正确的是
CH,
A.2,3,3-三甲基戊烷
B.3,3,4-三甲基戊烷
C.2,3二甲基-2-乙基丁烷
D.2,3-三甲基戊烷
13.现代分析仪器可以给科研、质检等提供定性定量的成像信息。下列说法错误的是
100-
Li
型
80-
60
He
40
20
0-mtmtt
10203040506070
质荷比
A.
光谱分析可鉴定元素
B.质谱法可测定相对分子质量
试卷第3页,共8页
100
mwwmTrTTTrrrrT
40030002000
1000
10
波数/em
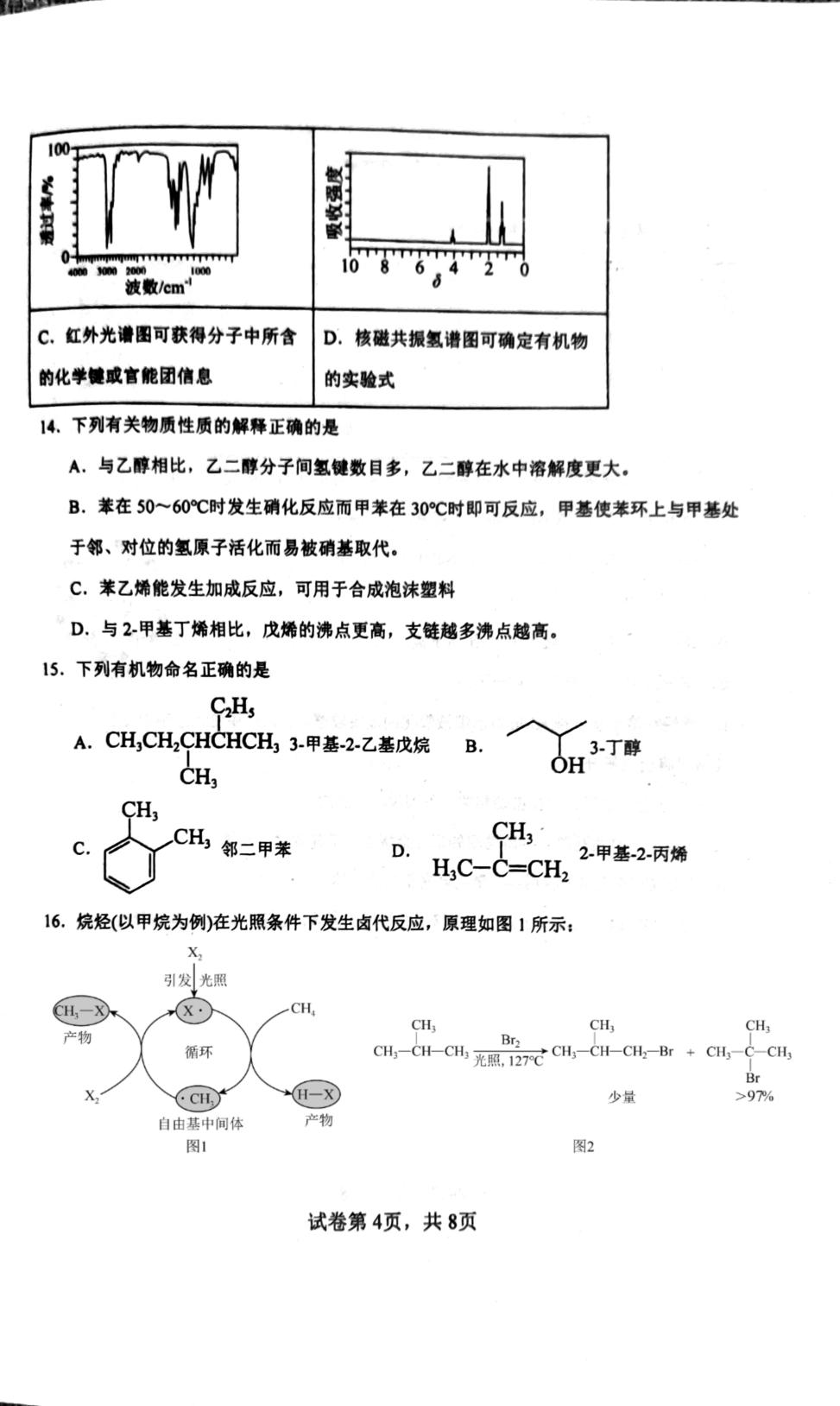
C.红外光谱图可获得分子中所含
D.
核磁共振氢谱图可确定有机物
的化学健或官能团信息
的实验式
14、下列有关物质性质的解释正确的是
A.与乙醇相比,乙二醇分子间氢键数目多,乙二醇在水中溶解度更大。
B.苯在50~60℃时发生硝化反应而甲苯在30℃时即可反应,甲基使苯环上与甲基处
于邻、对位的氢原子活化而易被硝基取代。
C.苯乙烯能发生加成反应,可用于合成泡沫塑料
D.与2甲基丁烯相比,戊烯的沸点更高,支链越多沸点越高。
15.下列有机物命名正确的是
C2H;
A.CH,CH2 CHCHCH33甲基2-乙基戊烷
B.
3-丁醇
CH,
OH
CH,
CH,
CH,
邻二甲苯
D.
H,C-C-CH,
2-甲基-2-丙烯
16.
烷烃(以甲烷为例)在光照条件下发生卤代反应,原理如图1所示:
X
引发光照
CH-X
X·
CH
CH
CH
CH:
产物
循环
Br2
CH-CH-CH无照,127CH,CH-CHBr+CH-C-CH
Br
X
C CH
少量
>97%
自由基中间体
产物
图1
图2
试卷第4页,共8页
已知:自由基中间产物越稳定,产物选择性越高。某研究人员研究了异丁烷发生澳代反应
生成一澳代物的比例,结果如图2下列说法正确的是
A,异丁烷的二澳代物有4种
B.由图2推测丙烷发生澳代反应时,形成的自由基CHCH-CH比CH.CHCH稳定
C.烷烃与卤素单质光照下发生取代反应时,光照越强烈,实验效果越好
D.光照条件下卤素单质分子中化学键断裂是引发卤代反应的关键步骤
第II卷(非选择题)
二、解容题
17、丙烯(CH,CH=CH)是一种重要的化工原料,结合以下合成路线,试回答下列问
题:
CH,CH-CH:H.O
HBr
CH,CHCH2Br
NaOH溶液
△
-CH,CH,CH,OH-
囚
B
g
浓硫酸
△
F
CH,
酸性高锰酸钾溶液
COOH-
D
回
(1)化合物A在一定条件下可形成高分子化合物G,G的结构简式为】
2)F的结构简式为
3)C中官能团的名称是;C发生催化氧化反应生成丙醛(CH,CH,CHO)的化学方
程式为
(4)D→E的反应类型是
(⑤化合物H(ON〈
CH2OH)也是一种重要的有机合成中间体,可通过下列转
化获取。请完成下列转化流程:
试卷第5页,共8页
CH,
CH,
CH,OH
②C,
③NaOH溶液
光照
△
NO,
NO
①的反应试剂及条件】
反应②生成物的结构简式
18.已知A是石油化工发展水平的重要标志,常在汽油中加入适量B作为汽车燃料,可以
节约石油资源,并减少汽车尾气对空气的污染。根据下面的转化关系回答下列问题:
B
发酵
农林产品
催化
葡萄糖
重整
溴苯
⑦
(淀粉或纤维素)
彰⑧
原油一
分馆
A
H0/催化剂,B—
石蜡油
碎瓷片
③
催化剂
+蒸气
②
△⑤CH,-CHC-0CH,CH
→丙烯
0/催化剂
丙烯酸乙酯
④
()已知溴苯是重要的医药中间体。反应①的反应类型为
。制得的溴苯中通常含有
少量的苯,提纯溴苯的实验操作是
。
(填蒸馏或萃取或者过滤或分液)
(2)A的结构简式为。,C中含有官能团的名称为碳碳双键和
(写名称)。
3)写出B和C转化为丙烯酸乙酯的化学方程式为
(4)鉴别苯和丙烯酸乙酯,可选用的试剂是
。
检验反应⑦发酵液中的生成物可用新
制的碱性氢氧化铜或者
溶液(写名称)
何已知丙烯酸乙酯c,一Gu足
ocH,CH,)具有刺鼻的
辛辣气味,可用作制造涂料黏合剂、纺织助剂等。某实验小组
用以下装置制备丙烯酸乙酯:
饱和
Na.Co
①球形干燥管c除起冷凝作用外,它的另一重要作用是
溶液
②待收集到一定量产物后停止加热,取下试管b并振荡、静置,可观察到液面出现油状物
并有气泡,气泡主要成分为
(填化学式)。
试卷第6页,共8页
19.下表为元素周期表的一部分,请参照元素①⑩在表中的位置,用化学用语回答下列问
题:
族
IA
周期
0
①
IIA
IIA
IVA
VA
VIA
VIIA
2
②
③
④
⑤
3
⑧
⑦
⑧
⑨
⑩
(1)原子半径最小的元素是
(填元素名称),写出⑨的价电子排布式
(2)最高价氧化物对应的水化物中,碱性最强的是
(填化学式,下同),酸性最强的是
两者反应的化学方程式为一。
(3)①与⑤形成的化合物中,化学键类型为
(4)⑦与⑩形成的化合物的电子式为,
②与④形成的原子个数比为1:2的化合物的结
构式为一。
(⑤)②、⑨形成的最高价氧化物熔点比较>(填化学式),原因是:
(6)③、④、⑧的简单离子半径比较>>】
(填离子符号)。
20.黄金(Au)是电子工业、现代通信、航天航空等领域的重要材料。现代工业治炼黄金
的原理
氰化法:4Au+8NaCN+O2+2H,O=4Na[Au(C)2]+4NaOH
2Na[Au(CN)2]+Zn=2Au+Naz [Zn(CN),]
疏代硫酸盐法(环保法):Au+2S,O+Fe”=Fe2+[Au(S,O,)2J
回答下列问题:
试卷第7页,共8页
(1)金和铜位于同族,金位于元素周期表区,二者中第一电离能较大的是】
(填“Cu”或“Au”)。
(2)lmol[Au(CN)2J含_二molo键;CN作配体时,配位原子是C,而不是N,其原
因是。
(3)现代最科学方法
(填名称)可证明[Zn(C.'呈正四面体结构,[Zn(CN).
中电负性最大的元素是一。
(4)配离子[Au(S,O,)2的中心离子是(填化学符号).
(5)金晶胞如图(a),晶胞截面如图(b)。已知晶胞边长为pm。
在1个金晶胞中,有个金原子,2个金原子的最近距离为Pm。金晶胞中,
金的原子空间利用率为
(用含π的式子表示,空间利用率
王×100%)·
Va
(a)
(b)
试卷第8页,共8页
资源预览图

1

2

3
4
相关资源
由于学科网是一个信息分享及获取的平台,不确保部分用户上传资料的 来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系学科网,我们核实后将及时进行处理。