湖北监利市第一中学等校2025-2026学年高三上学期2月期末化学试题
2026-02-10
|
8页
|
349人阅读
|
18人下载
资源信息
| 学段 | 高中 |
|---|---|
| 学科 | 化学 |
| 教材版本 | - |
| 年级 | 高三 |
| 章节 | - |
| 类型 | 试卷 |
| 知识点 | - |
| 使用场景 | 同步教学-期末 |
| 学年 | 2026-2027 |
| 地区(省份) | 湖北省 |
| 地区(市) | 荆州市 |
| 地区(区县) | 监利市 |
| 文件格式 | |
| 文件大小 | 5.42 MB |
| 发布时间 | 2026-02-10 |
| 更新时间 | 2026-02-10 |
| 作者 | 匿名 |
| 品牌系列 | - |
| 审核时间 | 2026-02-10 |
| 下载链接 | https://m.zxxk.com/soft/56423542.html |
| 价格 | 0.00储值(1储值=1元) |
| 来源 | 学科网 |
内容正文:
化
学
本试卷共8页,19题。满分100分。考试用时75分钟。
★祝考试顺利★
注意事项:
1.答题前,先将自己的姓名、准考证号填写在试卷和答题卡上,并将准考证号条形码贴在答题卡上的
指定位置。
2.选择题的作答:每小题选出答案后,用2B铅笔把答题卡上对应題目的答案标号涂黑。写在试卷、
草稿纸和答题卡上的非答题区域均无效。
3.非选择题的作答:用黑色签字笔直接答在答题卡上对应的答題区域内。写在试卷、草稿纸和答题
卡上的非答题区域均无效。
4.考试结束后,请将本试卷和答题卡一并上交。
可能用到的相对原子质量:H1C12016Na23S32Ti48Fe56Sr88
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要
求的。
1.食品添加剂满足了人们对食品多样化的需要。下列食品添加剂中不属于凝固剂的是
A.谷氨酸钠
B.氯化镁
C.硫酸钙
D.葡萄糖酸-8-内酯
2.下列化学用语表达正确的是
A.乙酸的实验式:C,H,02
B.甲烷中共价键类型:s-pσ键
C.乙醇的球棍模型
D.碳化钙的电子式:c[:C:g]
3.化学材料在航空航天、军事等领域用途广泛。下列有关材料的说法错误的是
A.氮化硅高温结构陶瓷可用于火箭发动机
B.有机玻璃(PMMA)可制成飞机的风挡
C.特种涂料可用于高性能歼击机的隐形材料
D.聚乙烯可用于航天飞船返回舱的烧蚀材料
4.下列实验示意图或化学图标正确的是
实脸
乙二醇
示意
NHCI和
Ca(OH)
KCI
图成
棉花团
化学
足量酸性
图标
KMnO,辯液
滥项
A.搁独类物质
B.制备乙二酸
C.制备氨气
D.配制KCl溶液
化学试卷
第1页(共8页)
餐巴扫描全能王
额3配人■有用的日mAe
…2-02-
5.基本概念和理论是化学思维的基石。下列说法错误的是
A.基态原子是指处于最低能量状态的原子
B.含有手性碳原子的分子均是手性分子
C.原电池是将化学能转化为电能的装置
D.有效碰撞是指能发生化学反应的碰演
6.没食子儿茶素是茶叶中天然存在的多酚类物质,其结构如下图所示。
OH
HO
OH
OH
OH
下列有关它的说法正确的是
A.属于脂肪烃衍生物
B.可用作抗氧化剂
C.能发生水解反应
D.1mol该物质最多消耗6 mol Na0H
7.离子化合物Z,WXY能预防龋齿。其中X、Y、Z、W是原子序数依次增大的短周期元素。Y是电负性
最强的元素,基态X、Z、W原子的未成对电子数之比为2:1:3。下列说法正确的是
A.第一电离能:X>Y
B.氧化性:X2>Y2
C.离子半径:Z>Y
D.W的最高价氧化物对应的水化物为中强酸
8.下列化学事实与结构因素没有关联的是
选项
化学事实
结构因素
A.
邻二甲苯的沸点高于对二甲苯
分子的极性
B.
CH,的稳定性强于H,S
电负性
C.
实测H,0(g)的相对分子质量大于18
分子的缔合
D.
水晶柱上石蜡在不同方向熔化快慢不同
原子的有序排列
9.聚醚酰酮是一种具有良好热稳定性和拉伸强度的有机高分子材料,其制备原理如下图所示。
H+(2n-1)X
COC
甲
丙
下列说法储误的是
A.甲的核避共振氢谐显示有1组蜂
B.乙中的所有原子可能共平面
C,X代表C
D.高分子丙具有热固性
化学试卷第2页(共8页)
S扫描全能王
额觉人直用的日罐Ae
-。2-。22-。一小
10.X是淡黄色固体,可通过如下图所示的转化关系生成M(部分反应略去反应条件),其中Y为无色无
味的液体,R是无色无味的气体。
QR M
下列说法错误的是
A.1molX与足量R反应转移电子数为N
B.W的一种同素异形体可用于自来水消毒
C.N与W生成X的反应可在坩埚中进行
D.Q和M中只有M能用作食用碱
11.我国科技工作者设计一套如下图所示的电解池装置,能将碱性废水中的亚硝酸盐转化为氨,又能将乙
二醇转化为甲酸盐,实现变废为宝。
电源
阴离子交换膜
化
CH.OH
N02
极
CH.OH
化电极
a
±HC00
NH,
KOH溶液
下列说法错误的是
A.电极a的电势高于电极b
B.阳极区溶液pH会减小
C.阴极区的反应为N0,+6e+5H,0一NH,+70H
D.阴极转化1 mol NO,阳极会消耗31g乙二醇
12.下列实验操作对应的实验目的或现象均正确的是
选项
实验操作
实验目的或现象
先向试管中加人2mL0.5mol·LCuS0,溶液,
溶液由蓝色变为黄绿色,再变为蓝
A
然后加人足量NaCl固体,再将试管置于冰水中
绿色
B
向乙苯和苯乙烯混合溶液中滴加KMnO,溶液
判断乙苯中是否含有苯乙烯
向装有2mL0.1mol·LNa,S,0,溶液的试管中
C.
溶液出现黄色沉淀
加人2ml0.1mol·LH,S0,溶液
将牧有10mL0.5mol·LCH,C00N溶液加热
D.
脸证盐的水解是吸热反应
至70℃,利用传感器测定溶液pI变化
化学试卷第3页(共8页)
S扫描全能王
额3配人影直用的归睡AP
…-022-
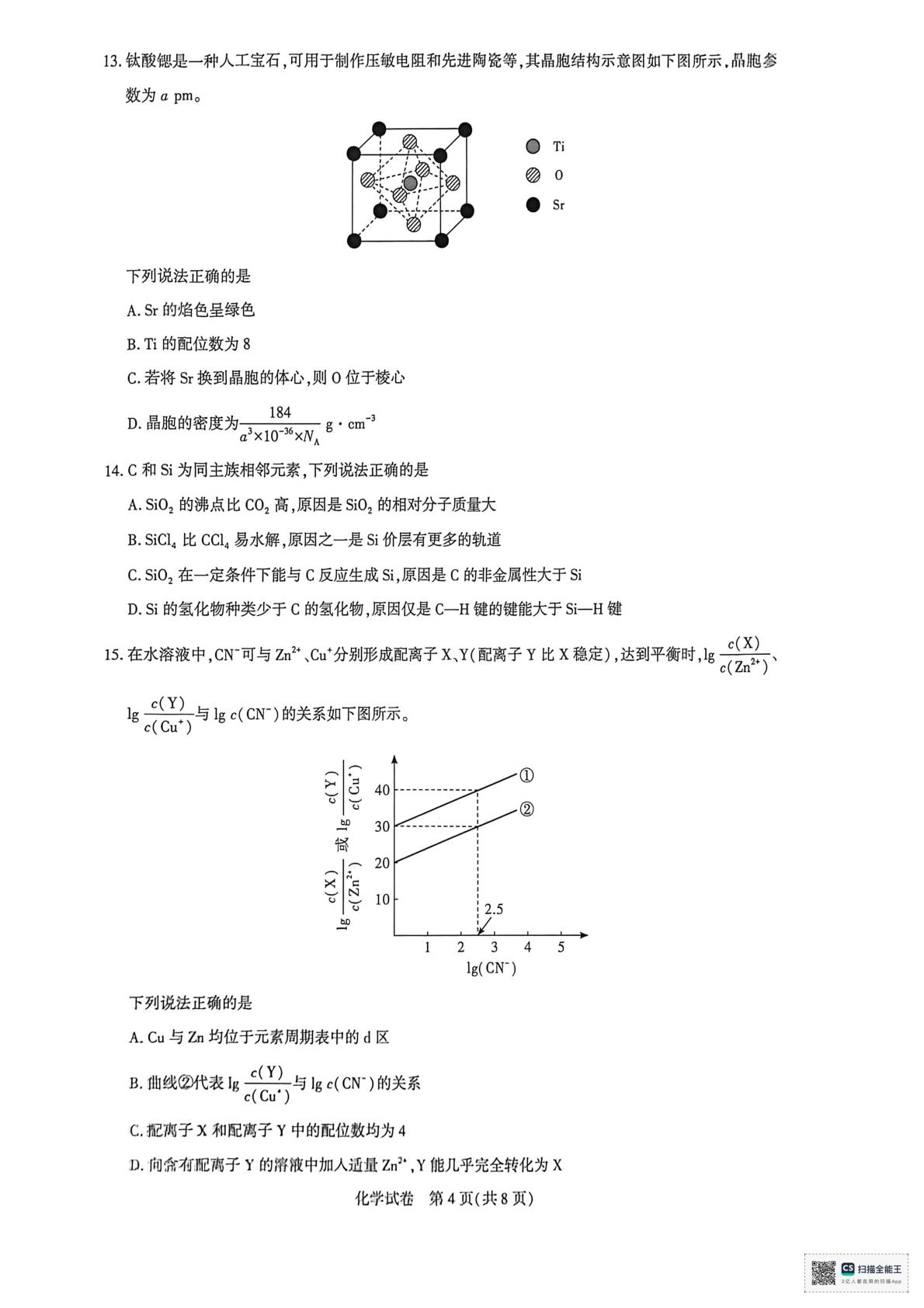
13.钛酸锶是一种人工宝石,可用于制作压敏电阻和先进陶瓷等,其晶胞结构示意图如下图所示,晶胞参
数为apm。
Ti
配
0
●Sr
下列说法正确的是
A.Sr的焰色呈绿色
B.Ti的配位数为8
C.若将Sr换到晶胞的体心,则0位于棱心
D晶胞的密度为、
184
ax105xw8·cm3
14.C和Sǐ为同主族相邻元素,下列说法正确的是
A.Si02的沸点比C02高,原因是Si02的相对分子质量大
B.SiCl4比CCl4易水解,原因之一是Si价层有更多的轨道
C.Si02在一定条件下能与C反应生成Si,原因是C的非金属性大于Si
D.Si的氢化物种类少于C的氢化物,原因仅是C一H键的键能大于Si一H键
15.在水溶液中,CN可与Z2+、Cu*分别形成配离子X、Y(配离子Y比X稳定),达到平衡时,lg
c(X)
c(Zn2)
1g2与1gc(CN)的关系如下图所示。
c(Cu*)
e
①
40-
②
30
念
20
11
X)
10
2.5
0
2
3
5
4
1g(CN-)
下列说法正确的是
A.Cu与Zn均位于元素周期表中的d区
B.曲线②代表g
c(Y)与gc(CN)的关系
c(Cu')
C.配离子X和配离子Y中的配位数均为4
D.向布配商子Y的溶液中加人适量Z·,Y能几乎完全转化为X
化学式卷第4页(共8页)
蠡田全任
…-022-
二、非选择题:本题共4小题,共55分。
16.(13分)
CH,
对甲基苯磺酸钠(
)是一种重要的有机合成中间体,易溶于水。实验室利用甲苯制备对甲基恭
SO,Na
磺酸钠的原理、装置与步骤如下。
CH,
CH,
CH3
CH;
+H2S0,
+H20,
NaOH
+H,0
SO,H
SO,H
SONa
步骤I:向如图所示装置(加热仪器已略去)中加人5mL甲苯、4mL浓硫酸(过量)
和一枚磁子,搅拌并加热保持微沸,一段时间后停止加热。
步骤Ⅱ:将上述反应混合物倒人盛有NaOH溶液的烧杯中,再加人1g活性炭,加热,
趁热过滤。
步骤Ⅲ:向上述滤液中加入适量NaC固体,加热至固体全部溶解,再冷却至室温,过
滤、干燥可得白色样品对甲基苯磺酸钠。
磁子
回答下列问题:
(1)仪器X的名称为
,冷却水从
(填“a”或“b”)口进。
(2)与该实验无关的实验图标是
(填标号)。
D
CH3
(3)步骤I的反应基本结束的现象为
,其中间产物
的pK
(填“>”“<”
SO3H
或“=”)
SO,H
(4)步骤Ⅱ中加人活性炭的目的是
(5)步骤围中加入NaC1固体的作用为
(6)若要进一步精制产品,可采取的方法是
化学试卷第5页(共8页)
-。2-。。224-。。一
17.(14分)
碲(s2Tc)是我国战略性新兴产业发展不可或缺的关键材料。从碲渣[主要成分为N,TO,恭所含
有Zn0、Pb,04、NaSb(OH),和Si02]中分离回收Te、Sb的工艺流程如下图所示。
Na,S
Na,SO,
H,0,
席→取逃液L还原滤液2,氧化,
结晶
Na.SO
没渣1
Te
NaSb(OH)
已知:①K,p(ZnS)=1.5x104,Kn[zn(0H)2]=3×107
②“浸渣1”中含有PbS、ZnS、S和Si02
③“滤液1”中含有Tes?和SbS
回答下列问题:
(1)基态Te价电子排布式为
(2)“浸渣1”中属于共价晶体的是
(3)“浸渣1”中的含锌沉淀是Zs,而不是Zn(0H)2。从沉淀的转化角度计算说明其原因
是
(4)Na2Te0,不溶于水,则“浸取”过程中Na2Te0,发生反应的离子方程式为
0
(5)已知“还原”过程中发生的反应为TS+3S0好一3S20号+S2+Te↓,则“氧化”过程中加人
H202的目的是
(6)Na2S0,·10H,0和Na2S0,的溶解度曲线如图所示,则“结晶”的操作是:加热浓缩至有大量晶体
析出,经
、干燥得Na,S0,固体。
60
50
Na,SO
040A
Na,s0.·10H,0
20
10
32.4℃
0102030405060708090100
温度/℃
(7)已知25℃时,K,(H,S)=106,”,K,(H,S)=1020,则0.01m0l·LNa,S溶液中离子浓度由大
列小的顺序为
化学试爸第6页(共8页)
-022-
18.(14分)
化合物丑是一种用于治疗糖尿病的药物中间体,其合成路线如下图所示。
CH,
CH
NH
NaBH
Cho
B
CH.
H
COOH
NaHCO,
H
OH
HCI
COOH
已知:RCH0+R,NH2→R,CH=NR2+H20
回答下列问题:
(1)A的名称为
(2)B的结构简式为,B→C的反应类型为
(3)G中含氧官能团的名称为醚键
和
-0
(4)F→G的转化过程中NaHC0,的作用之一是提供碱性条件,使F发生分子内加成成环,则
NaHC0,不能换成Na,C0,的理由是
一0
(5)从物质结构的角度解释C能与G形成H的原因是
(6)D有多种同分异构体,其中能与FCl,溶液发生显色反应的共有
种。
化学试爸第7页(共8页)
蠡田全任
…2-。22--
19.(14分)
CH,和C02的干重整与CaC0,的分解反应耦合,可生产合成气(C0和H2),其主要反应如下:
反应I:CH,(g)+C02(g)=2C0(g)+2H(g)△H,
反应Ⅱ:CaC0(s)=Ca0(s)+C02(g)
△H2=+178.8kJ·mol1
反应Ⅲ:C02(g)+H2(g)=C0(g)+H20(g)
△H2=+41.0kJ·mol-
回答下列问题:
(1)上述含碳物质中C原子的杂化方式有
种。
(2)已知各物质的燃烧热如下表所示。
物质
CH,
CO
H2
然烧热/kJ·mol
-890.3
-283.0
-285.8
则△H,=
kJ·mol。为提高反应I中CH,平衡转化率可选择的条件是
(填标
号)。
A.高温高压
B.高温低压
C.低温高压
D.低温低压
(3)反应I和反应Ⅱ的平衡常数K与温度的关系如下图所示。
350
300
--◆·甲烷干重整
250
0一
碳酸钙分解
200
150
100
50
0
01
000个
00
-50
600
650
700
750
800
850
T/℃
①在温度低于650℃时,碳酸钙分解的平衡常数几乎为0。从焓变和熵变的角度分析其原因
为
0
②750℃,p条件下,向密闭容器中加人CaC0,和CH4,若仅发生反应I和Ⅱ,达到平衡后升温至
850℃,体系中n(C02)会(填“不变”“增大”或“减小”)。
(4)在一定温度,100kPa下,若向体系加人1 mol Cac(0,和1 mol CH4,恒压反应至平衡时,CaC03的
转化率为100%,体系中n(C0):n(H2):(C02)=5:3:1,则甲烷的转化率a(CH4)=
、反应
Ⅲ的压强平衡常数为
kPao
化学试卷第8页(共8页)
鬟田全任
0。-。224--
资源预览图

1

2

3
4
相关资源
由于学科网是一个信息分享及获取的平台,不确保部分用户上传资料的 来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系学科网,我们核实后将及时进行处理。