湖北武汉市武昌区2026届高三上学期期末质量检测 化学试卷
2026-01-31
|
2份
|
10页
|
1744人阅读
|
20人下载
资源信息
| 学段 | 高中 |
|---|---|
| 学科 | 化学 |
| 教材版本 | - |
| 年级 | 高三 |
| 章节 | - |
| 类型 | 试卷 |
| 知识点 | - |
| 使用场景 | 同步教学-期末 |
| 学年 | 2026-2027 |
| 地区(省份) | 湖北省 |
| 地区(市) | 武汉市 |
| 地区(区县) | 武昌区 |
| 文件格式 | ZIP |
| 文件大小 | 2.75 MB |
| 发布时间 | 2026-01-31 |
| 更新时间 | 2026-02-07 |
| 作者 | 匿名 |
| 品牌系列 | - |
| 审核时间 | 2026-01-31 |
| 下载链接 | https://m.zxxk.com/soft/56259853.html |
| 价格 | 1.00储值(1储值=1元) |
| 来源 | 学科网 |
内容正文:
2026届高三年级上学期期末质量检测
化学
本试卷共8页,共19题。满分100分,考试用时75分钟。
注意事项:
1.答题前,考生务必将自己的姓名、准考证号填写在答题卡指定位置。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。
如需改动,用橡皮擦擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题
卡上。写在本试卷上无效。
3.考试结束,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H1C12016Na23
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项
是符合题目要求的。
1.2025年九三阅兵展示了我国多种高科技材料。下列材料中属于金属材料的是
A.战机发动机的钛合金部件
B.卫星通信车的碳纤维复合材料
C.地面装备传动系统的氨化硅陶瓷
D.柔性电路基材的聚酰亚胺薄膜
2.化学与生活息息相关。下列物质不能用作净水混凝剂的是
A.硫酸亚铁
B.硫酸铝
C.聚合氯化铝
D.硫酸铜
3.一种用于合成染料和药物的中间体结构如图,下列说法正确的是
A.有3种官能团
CH,O
NHCOCH,
B.有1个手性碳原子
C.名称为对甲氧基乙酰苯胺
D.可与4molH2发生加成反应
4.在电解氯化铜溶液的实验中,未涉及下列图标的操作或警示的是
A
B
5.化学用语是学好化学的基石。下列化学用语表述正确的是
HH
AN2H,的电子式:N成:N:H
B.N2O的中心原子杂化轨道示意图
高三年级化学试卷第1页共8页
H-N-H…O—H
C,氨气和水形成的占比最大的氢键示意图:
D.Mg3N2的水解方程式:Mg3N2+6H2O-3Mg(OH)2+2NH3↑
6.正确的选择和应用方法是迈向成功的关键。下列关于方法的应用错误的是
选项
方法
应用
A.
分类法
SiO2是酸性氧化物,可以和NaOH溶液反应
B.
模型法
NaH2PO2无法电离出H+,属于正盐
类比法
水杨酸含有羧基,可以发生酯化反应
向硫酸铁溶液中加入等体积浓硫酸,通过颜色变化来探
D.
变量控制法
究生成物浓度对盐类水解平衡的影响
7.下列实验操作中,有关现象和结论的描述正确的是
①2mL0.05mol/L②4滴0,1mo1/L③8滴0.1mol/L
NaC溶液
KI溶液
Na,S溶液
乙醇
蛋白质与
浓硝酸的
操作
混合物
酸性重格
酸钾溶液臣
2 mL 0,1mol/L
AgNO,溶液
A.火焰呈
B溶液颜
现象或
C.出现白色
D.操作③后,试管中黄色沉淀转化
黄色,说明
色由橙色
结论
沉淀
为黑色沉淀
样品是钠盐
变为绿色
8.一种可用于固态电池电解质中的物质结构如图所示,其中X、Y、Z、W为原子半径依次增
大的短周期主族元素,且X、Y、Z位于同一周期。下列说法正确的是
A.第一电离能:XZ>Y
Y
B.Y和W的单质均为非极性分子
Na"
XW—Zw-X
C.最高价氧化物对应的水化物酸性最强的是X
D.该物质的熔点高于NaCl
9.依据下列事实进行的推测正确的是
选项
事实
推测
A
盐酸和NaHCO,反应是吸热的
盐酸和Na2COg反应也是吸热的
B.
千冰中C02配位数为12
C60晶胞中配位数也为12
C.
苯酚和浓溴水可以发生取代反应
甲苯和浓溴水也可以发生取代反应
SiH沸点高于CH,
HCI沸点也高于HF
高三年级化学试卷
第2页共8页
10.MOFs材料具有无机材料的刚性和有机材料的柔性特征,可用于存储甲烷和氢气等燃料
气。一种MOFs材料的晶胞结构如图,晶胞参数为apm。下列说法错误的是
A.基态Zn原子的价电子排布式为3d4s2
o锌簇[OZn,
8,距离最近的1,3苯三甲酸的距离为号。P如
●1,3-苯二甲酸
C.与1个锌簇等距且最近的1,3-苯二甲酸有4个
D.该材料存储甲烷和氢气是通过范德华力实现的
11.钠离子电池以其低成本、高安全性能可作为锂离子电池的强力“替补”。一种钠离子电池
的示意图如图所示,总反应可表示为NaMO,+C,赛毫Na-,MO十Na,C。下列说法
错误的是
外电源或用电器
A.放电时,Na1-MO2为正极
B.充电时,Na+移向NaCm电极
C.充电时,外电路转移4moleˉ,理论上阴极增
重92g
D.M可为Ca、Co、Ni元素
Na,-MO,电极
Na,C,电极
12.碳碳键的偶联反应是有机合成中的重要反应,一种碳碳键的偶联反应机理如图,图中L
代表配体、R代表有机基团、X代表卤素。
RX
RSR'
Pd(O)L.
(氧化加成
还原消除
(n-2)L*
L
R-Pd-X
L一Pd=-R'
-Cu三-R
·RNHX
-R
CuX
RN+H-=-R
下列说法错误的是
A.PdLn是该反应的催化剂
B.RN在反应中起到了碱的作用
C.整个过程中Pd的化合价发生了变化
D.若用R'C=CR'代替HC=CR',也会生成R'C=CR
高三年级化学试卷第3页共8页
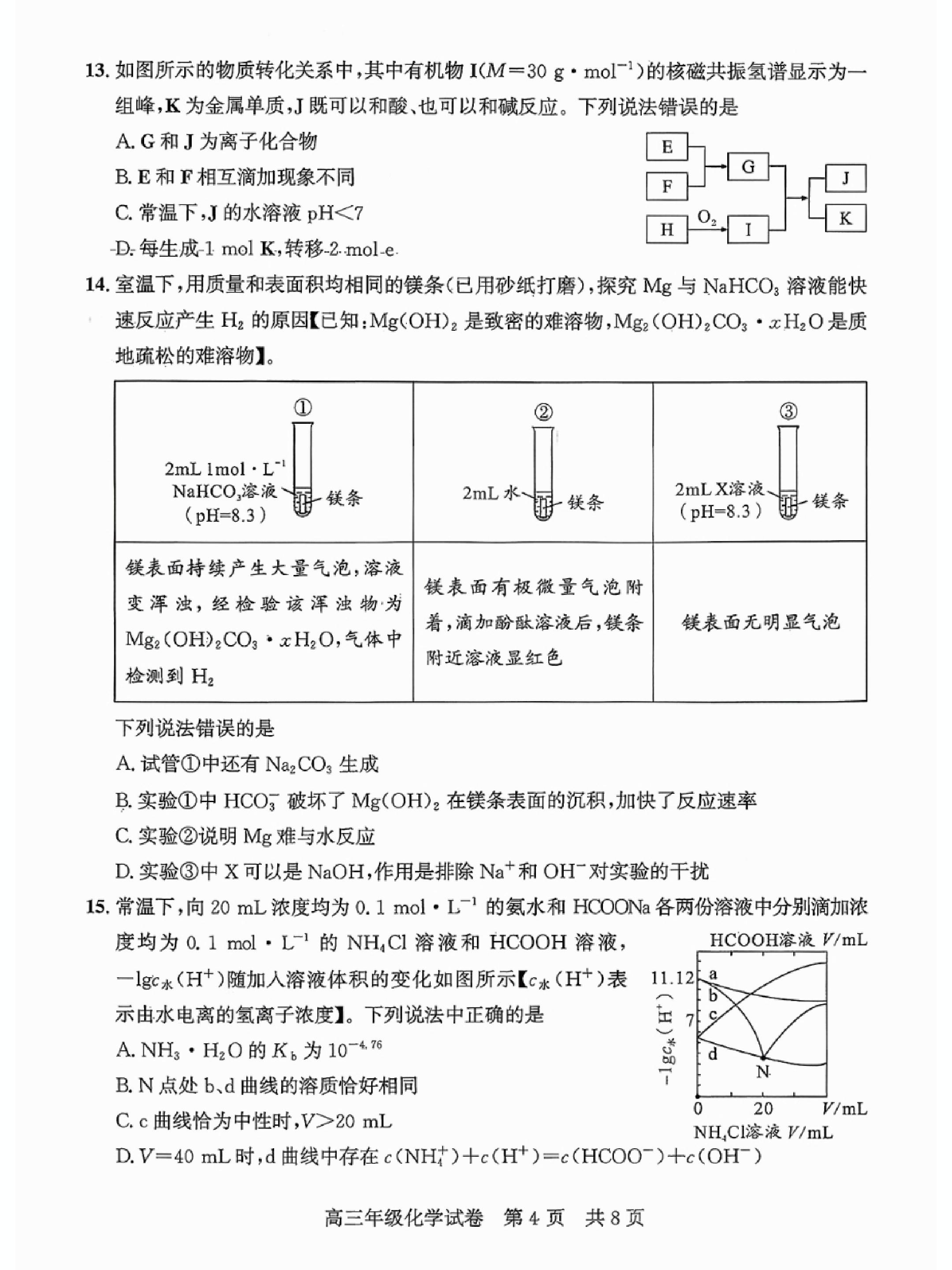
13.如图所示的物质转化关系中,其中有机物I(M=30g·mol一1)的核磁共振氢谱显示为一
组峰,K为金属单质,J既可以和酸、也可以和碱反应。下列说法错误的是
A.G和J为离子化合物
B.E和F相互滴加现象不同
C.常温下,J的水溶液pH<7
D.每生成1molK,转移2mole
14.室温下,用质量和表面积均相同的镁条(已用砂纸打磨),探究Mg与NaHCO,溶液能快
速反应产生H2的原因【已知:Mg(OH)2是致密的难溶物,Mg2(OH)2CO3·xH2O是质
地疏松的难溶物】。
①
②
③
2mL1mol·L-
NaHCO,溶液
匪钱条
2mL水
2mLX溶液
(pH=8.3)
证镁条
(pH=8.3)
厨镁条
镁表面持续产生大量气泡,溶液
镁表面有极微量气泡附
变浑浊,经检验该浑浊物为
着,滴加酚酞溶液后,镁条
镁表面无明显气泡
Mg2(OH)2C03·xH2O,气体中
附近溶液显红色
检测到H2
下列说法错误的是
A.试管①中还有Na2CO3生成
B.实验①中HCO3破坏了Mg(OH)2在镁条表面的沉积,加快了反应速率
C.实验②说明Mg难与水反应
D.实验③中X可以是NaOH,作用是排除Na+和OH对实验的干扰
15.常温下,向20mL浓度均为0.1mol·L-1的氨水和HC0ONa各两份溶液中分别滴加浓
度均为O.1mol·L1的NHCl溶液和HCOOH溶液,
HCOOH溶液V/mL
一lgc水(H+)随加入溶液体积的变化如图所示【c水(H+)表
11.12a
示由水电离的氢离子浓度】。下列说法中正确的是
A.NH·H2O的K6为1046
*8I-
N
B.N点处b、d曲线的溶质恰好相同
0
20
V/mL
C.c曲线恰为中性时,V>20mL
NH,CI溶液V/mL
D.V=40mL时,d曲线中存在c(NHt)+c(H+)=c(HCOO-)+c(OH厂)
高三年级化学试卷第4页共8页
二、非选择题,本题共4小题,共55分。
16.(14分)
钼镍催化剂是石油裂解工业的重要催化剂,其通常使用A山2O3作为催化剂载体。从废弃
钼镍催化剂中回收钼元素与镍元素的工艺流程如下图所示。
①H,SO
②75℃H8(g)
沉相
提纯MoS:
H,SO,、HF、NaOH
H,O,
(pH≈5.5)
NaOH
废液1
废弃细镍
催化剂
焙烧
酸漫
调pH,H
讽pH,
①HCI
②NH,·H,O
滤渣
③Na,S
H,0
洗渣
沉淀转化
Niso,
已知:
废液2
①25℃时,KNi(OH)2]=2×10-15,lg2=0.3;
②pH>6时,钼元素常以MoO形式存在;
③加沉淀剂使一种金属离子浓度小于等于l0-5mol·L1,即认为沉淀完全。
回答下列问题:
(1)“焙烧”的目的是除去固态碳沉积物和
(2)已知F的配位能力极强,滤渣主要成分的晶体结构中阴阳离子之比为1:3,其化学
式为
(3)“调pH”后的过滤操作选用漏斗的材质可为
(填标号)。
①塑料
②铁
③陶瓷
(4)“调pH2”中控制溶液的pH范围为
(5)“沉钼”中②的离子方程式为
(6)“沉淀转化”中发生的化学方程式为
(7)“废液1”与“废液2”可先混合再处理,这样操作比直接分别处理的优势是
17.(13分)
某研究小组探究硫酸铜溶液与硫化钠溶液反应的产物。
实验
实验操作
实验现象
向2mL0.02mol·L-1CuSO4溶液中加入
I
立即产生黑色沉淀
2mL0.02mol·L-1Na2S溶液
向2mL饱和CuSO:溶液中加入2mL饱和
Π
产生棕黑色沉淀
Na2S溶液
Ⅲ
向I的上层清液滴加浓氨水
无明显现象
溶液显浅蓝色,放置一段时间
向Ⅱ的上层清液滴加浓氨水
后溶液蓝色加深
高三年级化学试卷
第5页共8页
已知:CuS、Cu2S均为黑色沉淀;Cu2S可溶于浓氨水形成无色的[Cu(NH3)2]+,在空气
中易被氧化为[Cu(NH3)4]+。
回答下列问题:
(1)实验Ⅲ的现象说明了实验I中发生了
反应(选填“氧化还原”或“复分解”)。
(2)实验V中溶液蓝色加深的离子方程式为
(3)为探究实验Ⅱ棕黑色沉淀的成分,取洗涤后的棕黑色沉淀进行如下实验操作:
上层清液
试剂X,
白色沉淀
稀盐酸
沉淀溶解
稀硝酸
浓NaOH
白色沉淀
棕黑色溶液,加热
沉淀
离心分离
稀硫酸
均分三份
无现象
稀硫酸
H,O,
+有气泡生成,溶液变蓝
仔细观
边缘有红色固体
察颜色
①通过“白色沉淀”判断上层清液中SO号,则试剂X是
②棕黑色沉淀在NaOH溶液中部分溶解的化学方程式为
(4)结合以上实验,得出结论:实验Ⅱ中棕黑色沉淀成分为
(填化学式)。
(5)某小组设计如下原电池装置,研究pH对反应的影响:
⊙
向Na2S溶液中滴加NaOH溶液,测得电压升高,从化
盐桥
学平衡角度解释原因为
石墨
石墨
(6)综合上述实验可知:影响硫酸铜溶液与硫化钠溶液反
应的产物的因素有
20
18.(14分)
饱和CuSO,饱和Na,S
溶液
溶液
一种可用于治疗类风湿性关节炎的药物重要中间体H的合成路线如图。
C
CN
B
Boc-NH,-
+BocN
一OH条件
-Bo
-N
A
B0(
HC
G
高三年级化学试卷第6页共8页
CH
已知:Boc-NH结构式:H,C
NH
H.C
回答下列问题:
(1)B中官能团的名称为
(2)C→D的反应方程式为
(3)G的结构简式为
(4)FG的反应类型为
(5)判断并解释E的αH具有活泼性的原因是
(6)D→F的反应分为两步,第二步反应生成F和另一种产物的结构简式为
(7)A的同分异构体中既含有羧基(一COOH)、又含有氨基(一NH2)的有
种。
19.(14分)
1,4-丁二醇在铜锌复合催化剂上制备Y丁内酯(丫0),存在以下反应:
g-心0g+2H(g△H,>0
g=g+2H,g
△H2>0
皿.80(g+2H,g一凸(g+,0g
)△H
(1)298K,101kPa下部分物质的燃烧热如下表:
0(g
H2(g)
燃烧热(kJ·mol-1)
1868
2325
285.8
已知HO(g)一H2OD△H=一40.7k·mol1,则△H3=
k灯·mol1。
(2)向一密闭容器中充入Y-丁内酯和H2,仅发生反应Ⅲ,改变下列条件,能同时增大反应
速率和Y丁内酯平衡转化率的有
(填标号)。
a.升高温度
b.充入Y丁内酯
c.压缩容器体积
d.更换高效催化剂
(3)已知该催化剂中起实际催化作用的是Cu(O),且Cu越分散,活性催化点位就越多。
实际使用时,将复合催化剂xCuO·yZO在氢气氛围下使用,而不直接使用Cu单
质作为催化剂的原因是
高三年级化学试卷第7页共8页
(4)在一定压强下,将氢气与1,4-丁二醇混合后,以恒定流速通过催化剂,发生反应I、
Ⅱ、Ⅲ。维持体系温度不变,在相同时间,Y丁内酯的产量随氢醇比的变化如下图所
示。随着氢醇比的增大,Y丁内酯的产量先升高后降低的原因是
1.3日
1.2
1.1
划1.0
0.9
0.8
0.7
0.6
234567
n(H):(1,4-乙二醇)
(5)按照氢醇比4:1配制原料气,用Ar作稀释气,充入恒温密闭容器中,发生反应I、
Ⅱ、Ⅲ。体系压强恒为7.3MPa,测得相同时间后各含碳物质的百分含量随n(原料
气):n(稀释气)的变化如图所示。【催化剂消耗H2的量忽略不计,x(y-丁内酯)=
n(y-丁内酯)
n(Y-丁内酯)十n(四氢呋喃)+(1,4-丁二醇X100%】
100
90H
80
70
M(82)
州
60
a.
50
40
30
20
N(16)
10
9(2)
2
45
810
6
n(原料气):(稀释气)
①图中表示四氢呋喃(
百分含量的曲线是
(填a、b或c)。
②M点时,氢气的平衡分压(H2)=
MPa,该温度下,反应I的分压平衡常
数K。=
(MPa)2(列出计算式,用平衡分压代替平衡浓度计算,分压=总
压X物质的量分数)。
高三年级化学试卷第8页共8页化学参考答案
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符
合题目要求的。
2
3
6
8
9
10
11
12
13
14
15
D
A
D
D
B
A
B
B
D
D
B
C
A
二、非选择题,本题共4小题,共55分。
16.(14分)
(1)表面石油(2分》
(2)Na3AlF6(2分)
(3)①(2分)
(4)pH≥9.15(2分)
(5)MoO2+3H2S+2H+=MoS2↓+S+4H20(2分)
(6)NiS+4H202-NiSO4+4H2O (2)
(7)废液1呈酸性,废液2呈碱性,中和后再排放可节省成本:同时生成H2S可以重复利用
(两点答出一点即可得分)。(2分)
17.(13分)
(1)复分解(1分)
(2)4[Cu(NH)z++O2+8NH3+2H20—4[CuNH)A]2++4OH
或4[Cu(NH3)2]+O2+8NH3·H20=4[CuNH34]2++4OH+6H20(2分)
(3)①BaCl2溶液(2分)
②3S+6Na0H△2NaS+NaS03十3H0(2分)
(4)Cu、S、Cu2S(多答CuS给分,2分)
(5)S2十HO一HS-+OH,加碱平衡逆向移动,c(S2)增大,S2还原性增强(2分)
(6)反应物浓度与溶液pH(2分)
试卷第1页,共2页
18.(14分)
(1)碳氯键、醚键(2分)
(2)2 Boc-N.
oH+o会2Bac-◇-0+2H02分)
厂HHC
(3)
NC-
(2分)
(4)水解反应(2分)
(5)-CN与
均为吸电子基团,C一H键的极性较强,H的活泼性高(2分)
6)
(2分)
OH
(7)12(2分)
19.(14分)
(1)-73.9(2分)
(2)c(2分)
(3)氢气还原后的Cu在ZO表面高度分散,比直接使用Cu能提供更多的催化位点,催化活
性更高(2分)
(4)氢醇比较小时,提高氢气占比,有更多CO被还原,催化剂活性增大,反应速率增大,
少丁内酯的产量升高:氢醇比过大时,会稀释1,4丁二醇降低反应速率,同时还会使生成的y丁内
酯还原为四氢呋喃从而降低其产量(2分)
5.642×0.82
(5)①c(2分)
②5.64(2分)
(2分)
0.02
试卷第2页,共2页
资源预览图

1

2

3
4
相关资源
由于学科网是一个信息分享及获取的平台,不确保部分用户上传资料的 来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系学科网,我们核实后将及时进行处理。
