专题4 计算应用题-【众相原创·赋能中考】2026年中考化学分层练习册(河北专用)
2026-03-16
|
2份
|
8页
|
28人阅读
|
2人下载
资源信息
| 学段 | 初中 |
|---|---|
| 学科 | 化学 |
| 教材版本 | - |
| 年级 | 九年级 |
| 章节 | - |
| 类型 | 题集-专项训练 |
| 知识点 | 化学的综合计算(暂存) |
| 使用场景 | 中考复习-一轮复习 |
| 学年 | 2026-2027 |
| 地区(省份) | 河北省 |
| 地区(市) | - |
| 地区(区县) | - |
| 文件格式 | ZIP |
| 文件大小 | 1.19 MB |
| 发布时间 | 2026-03-16 |
| 更新时间 | 2026-03-25 |
| 作者 | 众相原创文化传播(陕西)有限公司 |
| 品牌系列 | 众相原创·赋能中考 |
| 审核时间 | 2025-12-17 |
| 下载链接 | https://m.zxxk.com/soft/55460698.html |
| 价格 | 3.00储值(1储值=1元) |
| 来源 | 学科网 |
内容正文:
13.(1)澄清石灰水变浑浊石灰石分解可以产生二氧化
碳(2)CaC0,高温Ca0+C0,↑(3)在月球基地使用
明火不安全(合理即可)可以使用石灰石和稀盐酸反
应制取二氧化碳(合理即可)(4)钛铁矿(5)温度
(合理即可)
14.任务一:A任务二:(1)Fe03+6HC=2FeCl3+
3H,0(2)无氧温度在35~50℃范围内,相同温度
下,发酵液浓度越高,池容产气率越高(3)g任务
三:【实验验证】产生白色沉淀【交流探讨】减少使用
一次性塑料购物袋(合理即可)
专题四计算应用题
1.(1)检查装置气密性
(2)解:设剩余固体中锰酸钾的质量为x。
2KMn0,△K,Mn0,+Mn0,+0,↑
316
197
6.32g
3166.32g
197x
g=197X632g=3.94g
316
剩余固体中锰酸钾的质量分数为3,945×10%=69.4%
5.68g
答:剩余固体中锰酸钾的质量分数约为69.4%。
2.(1)含碳量不同
(2)解:设100t该赤铁矿石中氧化铁的质量为x。
3C0+Fe,0,商巡2Fe+3C0,
160
112
56t
160x
11256t
x=160x56
=80t
112
该赤铁矿石中氧化铁的质量分数为80
×100%=80%
100t
答:该赤铁矿石中氧化铁的质量分数为80%。
3.(1)锡与铅形成合金后熔点降低
(2)解:151kg含Sn0220%的锡砂中含有氧化锡的质量
为151kg×20%=30.2kg,设理论上可以炼出锡的质量
是x。
C+sn0n商退sn+c0,t
151
119
30.2 kg x
15130.2kg
119x
x-19x30.2s=23.8kg
151
答:151kg含Sn0,20%的锡砂,理论上可以炼出锡的质量
是23.8kg
18
4.(1)不可再生
(2)解:设18g该天然气中甲烷的质量为x。
CH,+20,点燃c0,+2H,0
16
44
x
44g
16x
4444g
x=16x44g=16g
44
该天然气中甲烷的质量分数为18×10%≈8,9%
答:该天然气中甲烷的质量分数约为88.9%。
5.(1)溶液变为红色
(2)解:由图可知,加入稀盐酸50g时二者恰好完全反
应,50g7.3%的稀盐酸中含有HC1的质量为50g×7.3%
=3.65g,设14.0g该抗酸药中碳酸氢钠的质量为x。
HCl+NaHCO,NaCl+H,O+CO,
36.584
3.65gx
36.5_3.65Ξ
84
x
x-84X3.65g=8.4g
36.5
该抗酸药中碳酸氢钠的质量分数为,8.4三×100%=60%
14.0g
答:该抗酸药中碳酸氢钠的质量分数为60%。
6.(1)b
(2)解:参加反应的硫酸的质量为10g×19.6%=1.96g,
设该样品中氧化铜的质量为x。
Cu0+H,S0,=CS0,+H,0
80
98
1.96g
80x
981.96g
x-80x1:968=1.6g
98
该样品中铜的质量分数为4g-1.68×100%=60%
4g
答:该样品中铜的质量分数为60%。
7.(1)不变
(2)解:设产生3.2g的氧气需要过氧化氢的质量为x。
Mn0
2H202¥
=2H,0+0,↑
68
32
x
3.2g
68x
323.2g
x-68×3.28=6.8g
32
装置中过氧化氢溶液的溶质质量分数为68:×1O0%
136.0g
=5%
答:装置中过氧化氢溶液的溶质质量分数为5%。
8.(1)吸收随气体带出的水分
(2)解:设鸡蛋壳中碳酸钙的质量为x。
2HCl+CaCO3=CaCl2+H20+CO2
100
44
820g-810.76g
100
44820g-810.76g
x-100x(820g-810.762=21g
44
鸡蛋壳中碳酸钙的质量分数为2!×1009%=84%
25g
答:鸡蛋壳中碳酸钙的质量分数为84%。
9.(1)18g
(2)解:由第一次实验可知,100g稀硫酸完全反应消耗
氧化铁的质量为20g-4g=16g,设100g稀硫酸中溶质
的质量为x。
Fe203+3H2S04=Fe2(S04)3+3H,0
160294
16g x
160_16g
294x
x-294x16g-=29.4g
160
所用稀硫酸的溶质质量分数为29.4三x100%=29.4%
100g
答:所用稀硫酸的溶质质量分数为29.4%。
10.(1)三
(2)解:设参加反应的Na,C0,的质量为x。
Na CO3+Ca(NO3)2=CaCO3 I+2NaNO3
106
100
x
1g
106-x
1001g
x=106X1g=1.06g
100
该粗盐样品中NaC的质量分数为10g-L.06×1O0%=
10g
89.4%
答:该粗盐样品中NaCl的质量分数为89.4%。
11.(1)NaCl
(2)解:设10g废水样品中氯化镁的质量为x。
MgCl,+2NaOH =2NaCl+Mg(OH)2
95
58
x
0.58g
95
80.58g
x-95×0.58g=0.95g
58
废水样品中氯化镁的质量分数为0×100%=9.5%
答:废水样品中氯化镁的质量分数为9.5%。
12.(1)0.4
(2)解:设参加反应的锌的质量为x。
Zn+H,SO,=ZnSO,+H,1
65
2
x
0.4g
65
20.4g
g=65x0.48=13.0g
黄铜样品中铜的质量分数为40.0g-13.0×100%=
40.0g
67.5%
答:黄铜样品中铜的质量分数为67.5%。
13.(1)氢气
(2)解:根据质量守恒定律,装置减少的质量即为反应中
消耗水的质量。设反应生成氢气的质量为x。
2H,0通电2H,↑+0,↑
36
4
0.9g
x
360.9g
4 x
4×0.98=0.1g
x
36
答:反应生成氢气的质量为0.1g。
14.(1)固体溶解,产生大量气泡
(2)解:反应生成二氧化碳的质量为61.7g+6g-65.5g
=2.2g,设6g样品中NaC03的质量为x。
2HCI+Na2 CO3=2NaCl+H,0+CO,
106
44
2.2g
1063x
442.2g
x=106×22g=5.3g
44
样品中Na,C0,的质量分数为3.38x100%=8.3%
6g
答:样品中Na,C0,的质量分数约为88.3%。
15.(1)引流
(2)解:反应生成碳酸钙的质量为110g+100g-200g=
10g,设所加碳酸钠溶液中溶质的质量为x。
Na,CO3 +CaCl=2NaCl+CaCO3
106
100
x
10g
106x
10010g
106×10g=10.6g
x
100
所加碳酸钠溶液的溶质质量分数是10.6g×10%=
100g
10.6%
答:所加碳酸钠溶液的溶质质量分数是10.6%。
19专题四
计算应用题5年5考)
类型1文字叙述型(2025.18)
3.(2024安徽改编)《天工开物》记载了锡的
1.实验小组同学在老师的指导下进行氧气
冶炼方法:入砂(指锡砂)数百斤,丛架木
的制取实验。加热6.32g高锰酸钾至不
炭亦数百斤,鼓鞴(指鼓入空气)熔化。
再产生气体,剩余固体质量为5.68g。请
…用铅少许勾引,方始(锡)沛然流注。
回答:
其反应原理为C+Sn0,高温5n+C0,↑。
(1)连接好装置后应先进行的操作是
(1)炼锡时加入少许铅形成合金,产物更
易熔化流出,原因是
(2)计算剩余固体中锰酸钾的质量分数。
(要求有必要的化学方程式和计算步骤,
(2)现有151kg含Sn0220%的锡砂,理论
结果保留至0.1%)》
上可以炼出锡的质量是多少(写出计算过
程)?
2.工业上用赤铁矿石冶炼生铁,再锻造成
4.为了保护环境,我国的城市燃气和集中供
钢。用一氧化碳冶炼100t某赤铁矿石理
暖已经广泛使用天然气(主要成分为甲
论上可以得到56t铁,请回答:
烷)。18g某天然气完全燃烧产生二氧化
(1)钢和生铁在性能上有差异,原因
碳44g。请回答:
是
(1)天然气属于
(填“可再
(2)计算该赤铁矿石中氧化铁的质量分
生”或“不可再生”)能源。
数。(要求有必要的化学方程式和计算步
(2)计算该天然气中甲烷的质量分数。
骤)
(要求有必要的化学方程式和计算步骤,
结果保留至0.1%)
57
类型2)坐标曲线型(2024.36)
6.(2025石家庄新华区模拟改编)为测定某
5.(2025兰州改编)为测定某抗酸药(含碳
被部分氧化为氧化铜的铜样品中铜的质
酸氢钠)中碳酸氢钠的质量分数。称取
量分数,取4g该样品于烧杯中,向其中逐
14.0g该药片充分溶解后(假设其他成分
滴加入19.6%的稀硫酸。所得溶液质量
不溶于水,也不与酸反应),向其中逐滴加
与加入稀硫酸的质量关系如图所示。请
入7.3%的稀盐酸,用pH传感器测得实验
回答:
数据如图所示。
溶液质量g
pH
051015稀硫酸的质量/g
05070稀盐酸的质量/g
(1)恰好完全反应的点为
(1)取少量b点溶液,向其中滴入紫色石
(填字母)。
蕊溶液,观察到
(2)该样品中铜的质量分数。(要求有必
(2)请计算该抗酸药中碳酸氢钠的质量分
要的化学方程式和计算步骤)
数。(写出计算过程)
58
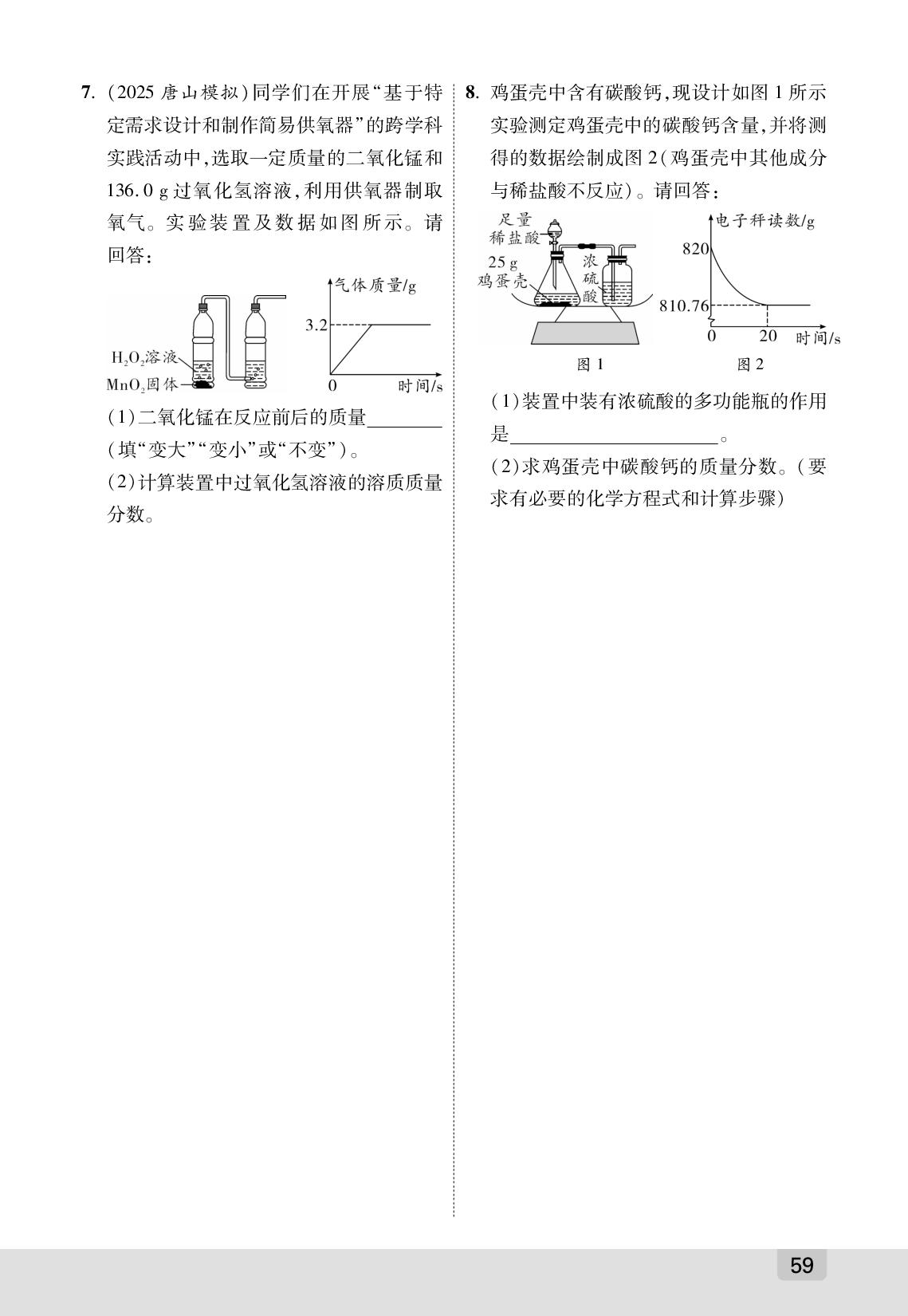
7.(2025唐山模拟)同学们在开展“基于特8.鸡蛋壳中含有碳酸钙,现设计如图1所示
定需求设计和制作简易供氧器”的跨学科
实验测定鸡蛋壳中的碳酸钙含量,并将测
实践活动中,选取一定质量的二氧化锰和
得的数据绘制成图2(鸡蛋壳中其他成分
136.0g过氧化氢溶液,利用供氧器制取
与稀盐酸不反应)。请回答:
氧气。实验装置及数据如图所示。请
足量
↑电子秤读数/g
稀盐酸
回答:
820
25g
浓
↑气体质量/g
鸡蛋壳
硫
南酸目
810.76
3.2
0
20时间/s
H,0,溶液
图1
图2
Mn0,固体
时间/s
(1)装置中装有浓硫酸的多功能瓶的作用
(1)二氧化锰在反应前后的质量
是
(填“变大”“变小”或“不变”)。
(2)求鸡蛋壳中碳酸钙的质量分数。(要
(2)计算装置中过氧化氢溶液的溶质质量
求有必要的化学方程式和计算步骤)
分数。
59
类型3表格数据型(2021.36)
请回答:
9.化学小组同学向盛有20g赤铁矿粉末的
(1)第
次实验时,物质完全
烧杯中,依次加入稀硫酸(赤铁矿中的杂
反应。
质既不溶于水,也不参加反应),充分反应
(2)计算该粗盐样品中NaCl的质量分
后,记录实验数据见表。请计算:
数。(要求有必要的化学方程式和计算
实验次数
第一次
第二次
第三次
步骤)
稀硫酸质量/g
100
100
100
剩余固体质量/g
4
2
2
(1)所用赤铁矿粉末中氧化铁的质量
为
(2)所用稀硫酸的溶质质量分数。(要求
有必要的化学方程式和计算步骤)
11.(2025邯郸模拟)某环保科研小组以含
有氯化镁的工业废水为研究对象,研究
该废水处理方案。实验小组分别进行三
组实验,并详细记录加入氢氧化钠溶液
后的实验数据,具体如下表所示(废水中
其他成分不参与反应):
实验1实验2实验3
废水样品/g
15
10
10
NaOH溶液质量/g
20
20
25
沉淀质量/g
0.58
0.580.58
10.某粗盐样品中含有少量Na2C03杂质,欲
(1)实验2反应后溶液的溶质(不考虑废
测定其中NaCl的质量分数,称取10g粗
水中其他成分)为
(填化学式)。
盐样品放入烧杯中,先加适量水充分溶
(2)计算废水样品中氯化镁的质量分数。
解,再将20g的Ca(NO3)2溶液分四次
(要求有必要的化学方程式和计算步骤)
加入烧杯中,产生沉淀的总质量与加入
Ca(NO3)2溶液的质量关系如表所示。
实验次数
四
所加Ca(N03)2
溶液质量/g
产生沉淀的总质量/g0.450.9
60
类型4)实验操作型(5年2考)
13.(2025武汉改编)项目小组利用如图所
12.(2022河北36题5分)为测定黄铜(铜
示装置电解水并收集干燥的氢气和
锌合金)样品中铜的质量分数,小明取
氧气。
定质量的样品放入烧杯中,分2次加入
质量分数相同的稀硫酸,实验过程和数
据如图所示。
50.0g稀硫酸
60.0g稀硫酸
充分反应
充分反应
样品质量
烧杯内物质
烧杯内物质
40.0g
质量89.8g
质量149.6g
(1)生成氢气的总质量是
(1)接通电源,收集a管逸出的气体,靠
go
(2)黄铜样品中铜的质量分数。
近火焰,观察到气体燃烧,发出淡蓝色火
焰,说明该气体是
(填“氢气”
或“氧气”)。
(2)一段时间后断开电源,实验前后整个
装置的质量减少了0.9g,写出通电过程
中反应的化学方程式并计算生成氢气的
质量(不考虑水的蒸发)。
61
14.(2025江西改编)实践小组为测定某品15.兴趣小组同学用实验室制取二氧化碳气
牌纯碱样品中Na,C03的质量分数,进行
体后的溶液进行如下实验。
了如图实验(杂质不参与反应)。
加入100g
加入61.7g
碳酸钠溶液
滤渣
稀盐酸(过量)
恰好完全
充分反应
盛
110g
反应后过滤
6g纯碱样品
烧杯内物质的
无色溶液
质量为65.5g
无色滤液200g
(1)加入稀盐酸观察到的现象是
(1)过滤操作中玻璃棒的作用是
(2)计算样品中Na2C03的质量分数。
(2)计算所加碳酸钠溶液的溶质质量分
(写出计算过程,结果精确到0.1%)
数。(要求有必要的化学方程式和计算
步骤)
62
资源预览图

1

2
3
相关资源
由于学科网是一个信息分享及获取的平台,不确保部分用户上传资料的 来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系学科网,我们核实后将及时进行处理。

