湖南省长沙市第一中学2025-2026学年高一上学期11月期中化学试题
2025-11-15
|
6页
|
450人阅读
|
60人下载
资源信息
| 学段 | 高中 |
|---|---|
| 学科 | 化学 |
| 教材版本 | - |
| 年级 | 高一 |
| 章节 | - |
| 类型 | 试卷 |
| 知识点 | - |
| 使用场景 | 同步教学-期中 |
| 学年 | 2025-2026 |
| 地区(省份) | 湖南省 |
| 地区(市) | 长沙市 |
| 地区(区县) | - |
| 文件格式 | |
| 文件大小 | 5.90 MB |
| 发布时间 | 2025-11-15 |
| 更新时间 | 2025-11-15 |
| 作者 | 匿名 |
| 品牌系列 | - |
| 审核时间 | 2025-11-15 |
| 下载链接 | https://m.zxxk.com/soft/54922769.html |
| 价格 | 0.00储值(1储值=1元) |
| 来源 | 学科网 |
内容正文:
农沙市第一中学2025-2026学年度高一第一学期期中考试
化学
时量:75分钟满分:100分
得分:」
可能用到的相对原子质量:H~1C~12N~140~16Na23S32Cl35.5
Ca~40Fe~56
一、选择题(本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符
目要求的)
1.下列各组物质分类正确的是
选项
混合物
酸
碱
酸性氧化物
碱性氧化物
A
氢氧化铁胶体
H2S04
NaOH
vO。
MgO
如
B
“84”消毒液
HNO
纯碱
SO;
CaO
氯水
CH COOH
Ba(OH)2
Mn2O2
Na2O
D
盐酸
HCI
NH3·H2O
C02
Na.O2
2.下列对化学概念的理解,正确的是
A.H+十OH一一H2O表示的不一定是酸碱中和反应
斯
B.风化、聚沉和升华都是物理变化
C.物质的溶解过程实质上就是其电离过程
D.漂粉精的主要成分是NaCIO和NaCl
3.性质决定用途,下列物质的性质与用途无关的是
A.氢化钠(NaH)具有还原性,可用作制氢刻
B.高铁酸钠(Na2 FeO4)易溶于水,可饮用水消毒
C.小苏打(NaHCO3)受热易分解,可用作膨松剂
D.维生素C具有还原性,可用作食品抗氧化剂
4.下列过程中,对应的反应方程式错误的是
A.焊接钢轨:2A1十Fe,O,高温Al,Os卡2Fe
B.绿矾(FSO4·7H2O)处理酸性工业废水中的Cr2O号:
6Fe2++Cr2O号-+14H+=6Fe3++2Cr++7H2O
C.漂白粉工作原理:Ca(CIO)2+C2+H2O一CaCO3↓+2HClO
D.《天工开物》记载用炉甘石(ZnCC)火法炼锌:2ZnC0,十C商温2Zn十3C0,个
化学试卷(一中版)第1页(共6页》
5.现有标准状况下四种气体:①8.96LCH②3.01X10s个HCl.③20.4gH2S④0.2mol
NH3,下列关系从小到大表示正确的是
A.体积:④<②<①<③
B.氢原子数:②<④<①<③
C.密度:④<①<②<③
D.质量:④<①<②y③.
6.NA为阿伏加德罗常数的值,下列流法正确的是
A.46g.NO2和N2O4的混合气体含有氧原子的数目为2NA
B.1 mol-Na2(2与足量CO2充分反应,转移的电子数为2NA
C.16.25gFeC固体加人沸水中充分反应形成Fe(OH)3胶体粒子数为91'a
D.3.36LC0和N2的混合气体含有的分子数自为0.15N,
7.下列澄清透明溶液中,能大量共存的离子组是
A.K、HCO3、、OH
B.NO3、C-、Na+、Fe3+
C.Na+、CHCOO、CH、H
D.A13+、Ag+、NO CI
8.下列离子方程式正确的是
A.向硫酸铜溶液中通入少量硫化氢:Cu2+十S2-一CuS↓
B.向饱和碳酸钠溶液中通入过量CO2:2Na++CO3十CO2十H2O一2 NaHCO31
C.强碱性溶液中NaCIO将Mn2+氧化成MnO2:Mn++ClIO-+H2O一MnO2Y+CI-+2H+
D.钠与水反应:Na十H2O—NaOH十H2
9.《本草纲目》中记载:“(火药)乃焰硝(K©、硫黄、杉木炭所合,以为烽燧铳机诸药者。”火药燃烧
爆炸时发生的反应为S十2KND,十3C点燃x,S+N个十3OA。下列有关说法错误的是
A.还原性:C一K2S
B.氧化产物与还原产物的物质的量之比为3∶2
C.反应每转移6mol电子,则能生成标准状况下气体体积44.8工
D.该反应中分别被S和KNO3氧化的碳原子数之比为5:1
I0.已知氧化性:C2>Br2>Fe3+,还原性:Fe+>Br>CI。向FeBr2溶液中通入一定量的Cl2,发
生反应的离子方程式为xFe2++Br十xCl一xFe++B+2eC。其中xz的值不符
合实际反应的是
A.x=4、y=6、x=5
B.x=2、y=10、x=6
C.x=3、y=1、=2
Dx=2、y=2、z=2
化学试卷(一中版)第2页(共6页)
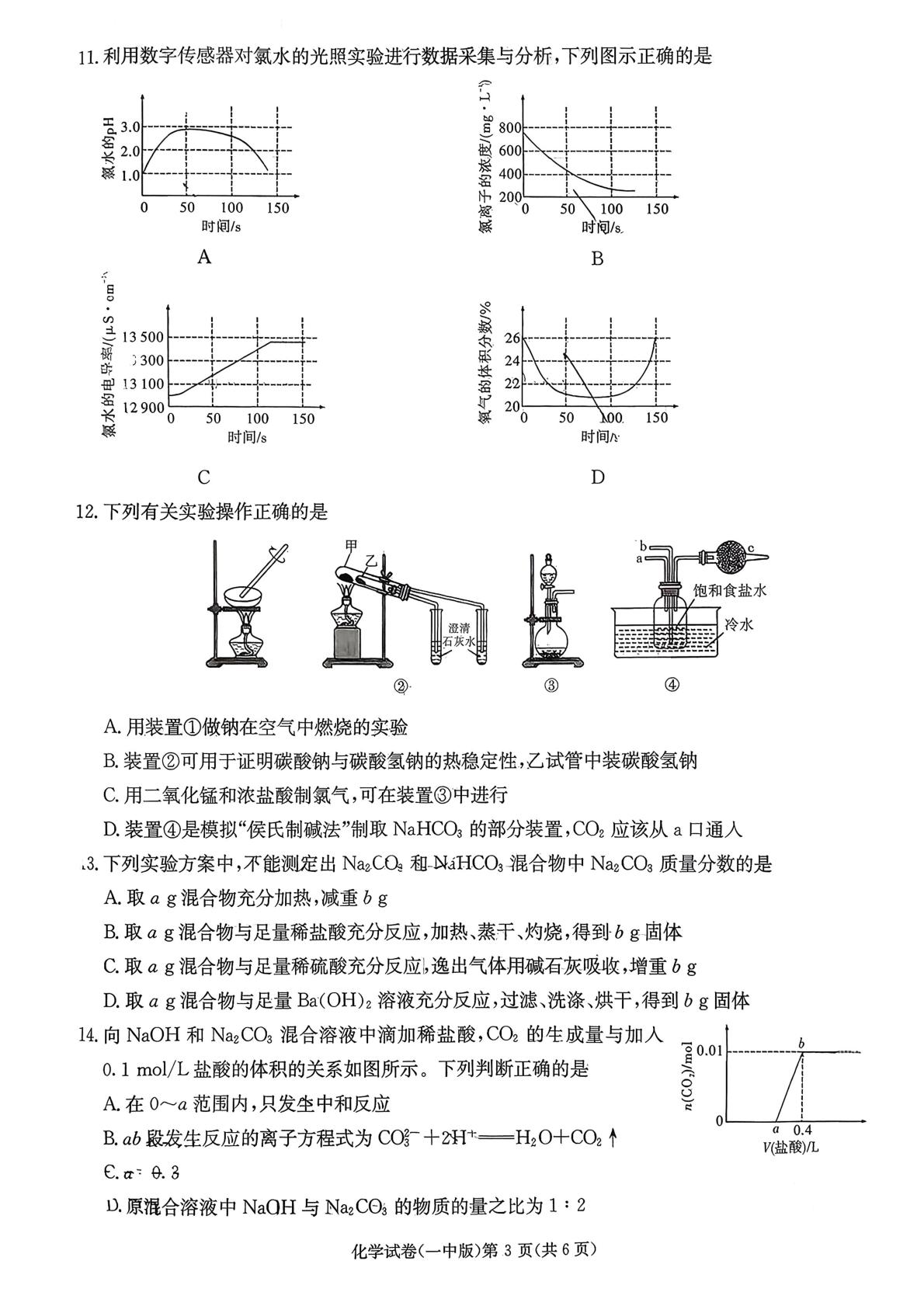
11.利用数字传感器对氯水的光照实验进行数据采集与分析,下列图示正确的是
3.0
800
20
600
1.0
400
200
0
50100
150
50100
150
时间/s
时间/s
A
B
500
)300
13100
26243
12900
20
50100
150
0
50
00
150
时间/s
时间小
C
D
12.下列有关实验操作正确的是
饱和食盐水
冷水
④
A.用装置①做钠在空气中燃烧的实验
B.装置②可用于证明碳酸钠与碳酸氢钠的热稳定性,乙试管中装碳酸氢钠
C.用二氧化锰和浓盐酸制氯气,可在装置③中进行
D.装置④是模拟“侯氏制碱法”制取NaHCO3的部分装置,CO2应该从a口通人
3.下列实验方案中,不能测定出Na2CO和NaHCO3混合物中Na2CO3质量分数的是
A.取ag混合物充分加热,减重bg
B.取αg混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到bg固体
C.取αg混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重bg
D.取ag混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得到bg固体
14.向NaOH和Na2CO3混合溶液中滴加稀盐酸,CO2的生成量与加人
0.1mol/L盐酸的体积的关系如图所示。下列判断正确的是
A.在0a范围内,只发生中和反应
B.ab段发生反应的离子方程式为CO十2H+一H2O+CO2个
a0.4
V(盐酸)L
E.x:0.3
D.原混合溶液中NaOH与Na2CO的物质的量之比为1:2
化学试卷(一中版)第3页(共6页)
选择题答题卡
题号
1
2
4
6
6
7
9
1011
12
1314
得分
答案
二、非选择题(本题共4小题,共58分)
15.(14分)分类和核心元素的化合价是研究物质性质的两个重要角度,通过分类和化合价的分析,
可以解释和预测物质的性质,设计物质间的转化途径。回答下列问题:
I.(1)S02与C02化学性质相似,S0,属于」
(填“酸性”或“碱性”)氧化物,将少量S02
通人澄清石灰水中,可观察到生成白色沉淀,发生反应的离子方程式为
(2)欲制备NaS,O,从氧化还原反应角度分析,下列反应物合理的是
(填标号)。
A.Na2S++S
B.Na2SO3+H2SO
C.Na2SO+S
(3)SO2具有强还原性,可以使酸性高锰酸钾溶液褪色(已知酸性条件下MO被还原成
Mn+),请写出该反应的离子方程式:
Ⅱ.(4)已知次磷酸(HPO2)是一元弱酸,HPO2中P元素的化合价为
,写出HPQ2与
足量NaOH溶液反应的离子方程式:
(5)在工业上HPO2常用手化学镀银,酸性条件下发生的反应如下,配平该离子方程式:
Ag++_H;PO2+Ag+_HgPO+.
16.(16分)侯德榜为我国化工事业的发展作出了卓越贡献,是我国近代化学工业的奠基人之一,他
结合中国国情对氨碱法进行改进,确定亚新的工艺流程一侯氏制碱法:将氨碱法和合成氨法
两种工艺联合起来,方法流程如图所示(s代表固体,g代表气体
C0,
煅烧
NaHCO:(s)
+纯碱
精制盐水
吸氮、
过滤
NH,CI(s)
碳化塔
食盐粉末
母液
母液送回
吸氨、碳化塔
NH
分离液态空气
C0,
H0(g)
c焦炭干馏煤
成
水煤气变换
N
塔
回答下列问题:
化学试卷一中版)第4页(共6页)
(1)向精制盐水中通人NH3、CO2的先后顺序是
(2)写出NaHCO3煅烧时发生反应的化学方程式:
(3)该流程中循环利用的物质为
(填化学式)。
(4)侯氏制碱法除了制取得到纯碱,还生成了一种副产品
(填名称),可以用来
(5)所得纯碱中可能含有少量NaCl杂质,可以通过如下方法测定所得纯碱中碳酸钠的质量
分数:
1.称取ag样品,溶于水中
ⅱ.加入足量氯化钙溶液
ⅲ.过滤、洗涤、干燥、称量,所得沉淀质量为bg
①证明步骤中Na2CO3已经沉淀完全的方法是
②该样品中碳酸钠的质量分数为
(用含a、b的代数式表示)。
17.(12分)某固体可能含有NH、Cu+、Na+、CO、6O?中的几种离子,为确定该固体的离子成
分,课堂上某实验兴趣小组的同学将其分成两等份,进行如下实验(不考虑水的电离和物质与水
发生的反应):
实验一:取一份固体溶于水得无色透明溶液,加入足量BaC2溶液,产生白色沉淀,向沉淀中加入
过量稀盐酸,沉淀部分溶解,过滤、洗涤、干燥,得到沉淀b。
实验二:取另一份固体与过量NaOH固体混合后充分加热,产生使湿润的红色石蕊试纸变蓝的
气体。(已知:氨气能使湿润的红色石蕊试纸变蓝)
回答下列问题:
(1)由以上实验可知,该溶液中一定不含有的离子为
(填离子符号,下同),一定含有的
离子为
(2)检验沉淀b是否洗净的方法为:取最后一次洗涤液,加入
若产生白色沉淀,则
未洗净;反之,则洗净。
(3)过滤时用到的玻璃仪器有烧杯、漏斗和玻璃棒,其中玻璃棒的作用是
(4)实验一中加人稀盐酸时,发生反应的离子方程式为
(5)为进一步确认该固体物质中是否含有Na+,可使用的鉴定方法是
18.(16分)C2O是黄棕色、具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应
生成次氯酸,C2O气体浓度过高易发生爆炸。实验室制取并收集C2O的装置如图所示(夹持及
加热装置已略去)。
浓盐酸
气体
非斑非短
液氨
干燥空气
等Hg0隔热层
水浴18-20℃
⑤
④
化学试卷(一中版)第5页(共6页)
已知:1.Ck0的制备反应:Hg0+2C6820℃-HeC6十C,0,
i.C20的熔点为一120.6℃,沸点为2.0℃。
回答下列问题:
(1)高锰酸钾与浓盐酸反应制氯气的离子方程式为
浓盐酸在该反应中体现了
(填标号)。
A.酸性
B.氧化性
C.还原性
(2)装置②的作用是
,装置③中盛装的试剂是
(3)反应中通入干燥空气的目的是
(4)装置④的加热方式的优点是
()整套装置存在不足之处,应在最后增加一个装置:-琴
一,该装置内的试剂为
使用该装置的目的是
化学试卷(一中版)第6页(共6页)
资源预览图

1

2
3
相关资源
由于学科网是一个信息分享及获取的平台,不确保部分用户上传资料的 来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系学科网,我们核实后将及时进行处理。