湖南省永州市2026届高三上学期第一次模拟考试化学试题
2025-09-19
|
8页
|
191人阅读
|
20人下载
资源信息
| 学段 | 高中 |
|---|---|
| 学科 | 化学 |
| 教材版本 | - |
| 年级 | 高三 |
| 章节 | - |
| 类型 | 试卷 |
| 知识点 | - |
| 使用场景 | 高考复习-一模 |
| 学年 | 2025-2026 |
| 地区(省份) | 湖南省 |
| 地区(市) | 永州市 |
| 地区(区县) | - |
| 文件格式 | |
| 文件大小 | 6.83 MB |
| 发布时间 | 2025-09-19 |
| 更新时间 | 2025-09-20 |
| 作者 | 匿名 |
| 品牌系列 | - |
| 审核时间 | 2025-09-19 |
| 下载链接 | https://m.zxxk.com/soft/53997653.html |
| 价格 | 0.00储值(1储值=1元) |
| 来源 | 学科网 |
内容正文:
永州市2026年高考第一次模拟考试
化学
命题人:张慧坚(祁阳一中)
张秀华(永州一中)
陶爱玲(东安一中)
审题人:胡小峰(永州市教科院)
注意事项:
1.本试卷共18道小题,满分为100分,考试时量75分钟。
2.考生务必将各题的答案填写在答题卡的相应位置,在本试卷上作答无效。考试结束
后只交答题卡。
3.可能用到的相对原子质量H-1C-12N-140-16Na-23Cu-64
一、选择题:本题共14小题,每小题3分,共42分。每小题只有一个选项符合题目要求。
1.2025年九三阅兵展示了我国多种高科技材料。下列材料属于金属材料的是
A.钛合金部件—新型战机发动机关键构件
B.氮化硅陶瓷轴承一地面装备传动系统核心部件
C.碳纤维复合材料一卫星通信车轻量化结构件
D.聚酰亚胺薄膜一电子对抗系统柔性电路基材
2.下列化学用语表述正确的是
A.中子数为12的氖原子:径Ne
2S
2P
B.基态Be原子的价电子排布图:
●
C.PC3分子的空间结构模型:
6120°
H
F
D.反-1,2-二氟乙烯的结构式:
C=C
八H
3.下列气体的提纯方法正确的是
A
B
D
-E
NaOH溶液
饱和NaCI溶液
酸性KMnO,溶液
无水CaCl2
除去C02中的S02
除去C2中的HCl
除去C2H2中的H2S
干燥NH3
4.下列试剂保存与实验操作不规范的是
A.四氯化碳保存在广口塑料瓶中
B.金属钠保存在石蜡油中
C.实验室中可以将未用完的白磷放回原试剂瓶
D.不慎将碱沾到皮肤上,应立即用大量水冲洗,然后涂上1%的硼酸
永州市2026年高考第一次模拟考试·化学第1页(共8页)
5.下列离子方程式与所给事实相符的是
A.过量铁粉与稀硝酸反应:Fe+NO3+4H=Fe3++NO↑+2H20
B.用氯气氧化苦卤得到溴单质:2Br+C2=Br2十2CI
C.用惰性电极电解MgC2溶液:2C+2H,0电解H,↑十20r+C21
D.用Na2CO3溶液处理水垢中的CaSO4:Ca2++CO}CaC03}
6.Na2O2可在呼吸面具中作为氧气的来源,其原理为2Na202十2C02=2Na2C03+O20
设Na为阿伏加德罗常数的值。下列说法正确的是
A.22.4LC02中含o键数目为2NA
B.7.8gNa202固体中含有的离子数为0.4Na
C.1L1molL1的Na2C03溶液中CO3的数目小于Na
D.等物质的量的Na2O2分别与足量的水和CO2反应,转移电子数均为Na
7.下列有关物质性质的解释错误的是
性质
解释
A
熔点:NaCI>CsCl
氯化钠中的离子键强于氯化铯中的离子键
B
稳定性:H2O>H2S
水分子间存在氢键,而硫化氢分子间不存在氢键
键角:NO2>NO3
NO中N原子为sp杂化,NO3中N原子为sp杂化
D
碱性:CH3NH2>NH3
一CH3是推电子基团,CH3NH2中氮原子电子云密度大
8.化合物QXY)(W2Y)5]ZY4可用于离子检测。W、X、Y、Z、Q为前四周期元素,且原
子序数依次增加,W原子的电子只有一种自旋取向,X的简单氢化物水溶液呈碱性,
Y是地壳中含量最高的元素,Z与Y同主族,基态Q原子的M层未成对电子数为4。
下列说法正确的是
A.原子半径:Z>Y>X
B.第一电离能:Y>X>Z
C.Y形成的两种常见单质均为非极性分子
D.化合物中含有离子键、极性键、配位键
9.采用电解和催化相结合的循环方式,以Pt为电极,电解NaBr溶液,可实现高效制H2
和O2,装置如图所示。下列说法正确的是
X
电源
Br
B
催化剂
泵
BrO2
A.电极a连接电源正极
B.电解过程中需不断补充NaBr
C.b电极反应式为Br一6e+3H20=BrO3+6H
D.催化反应生成的n(Z:n(Br)=2:3
永州市2026年高考第一次模拟考试·化学第2页(共8页)
10.布诺芬为解热镇痛药物,其合成路线如下:
(CH,CO),O
H2、C0
→人〔
COOH
HF
催化剂
I
下列说法错误的是
A.I中所有原子不可能共平面
B.Ⅱ转化为Ⅲ的过程中,有手性碳原子形成
C.Ⅱ转化为I的反应,原子利用率为100%
D.1molⅢ最多可与4molH2反应
l1.工业上可用低品位锰矿(主要成分MmO2,含Fe、Al、Ni、Pb等元素的杂质)制备高
纯二氧化锰,工艺流程如图所示。下列说法错误的是
①空气
NH HCO
②FeSO,
NH,H2O
Na,S
NHHO
空气
低品位
锰矿
焙烧
浸取
除铝
除镍铅
沉锰
煅烧
→Mn02
Fe2O3
已知:常温下Kp(PbS)=8.0×10-28、Ksp(NiS)=1.0×10-21
A.“焙烧”前,需对低品位锰矿进行粉碎处理
B.“除铝”时,可用足量的NaOH溶液代替NHH2O
C.“除镍铅”后的滤液中,cPb2:cN2+)=8.0×10-7
D.“沉锰”时,反应的离子方程式为:
HCO3 +NH3H2O+Mn2*=MnCO34+NH+H2O
12.烟酸又称维生素B3,实验室可用3-甲基吡啶为原料来制备。
CH.
COOK
KMnO4
COOH
3-甲基吡啶(沸点:144℃)
烟酸(沸点:293℃)
已知:烟酸微溶于冷水,易溶于热水。
实验步骤:①在3-甲基吡啶和水的混合液中分多次加入KMO4固体,加热搅拌。
②将步骤①所得溶液转移至蒸馏烧瓶中,控制温度在144℃时蒸馏,趁热过滤。
③用浓盐酸酸化滤液,并调节溶液的pH为3.84.0,经一系列操作,获得粗产品。
下列说法错误的是
A.分多次加入高锰酸钾的目的是控制反应速率和提高产率
B.蒸馏的目的是为了除去未反应的3-甲基吡啶
C.步骤③中,可用广泛pH试纸测定溶液的pH
D.可采用重结晶的方法提纯粗产品
永州市2026年高考第一次模拟考试·化学第3页(共8页)
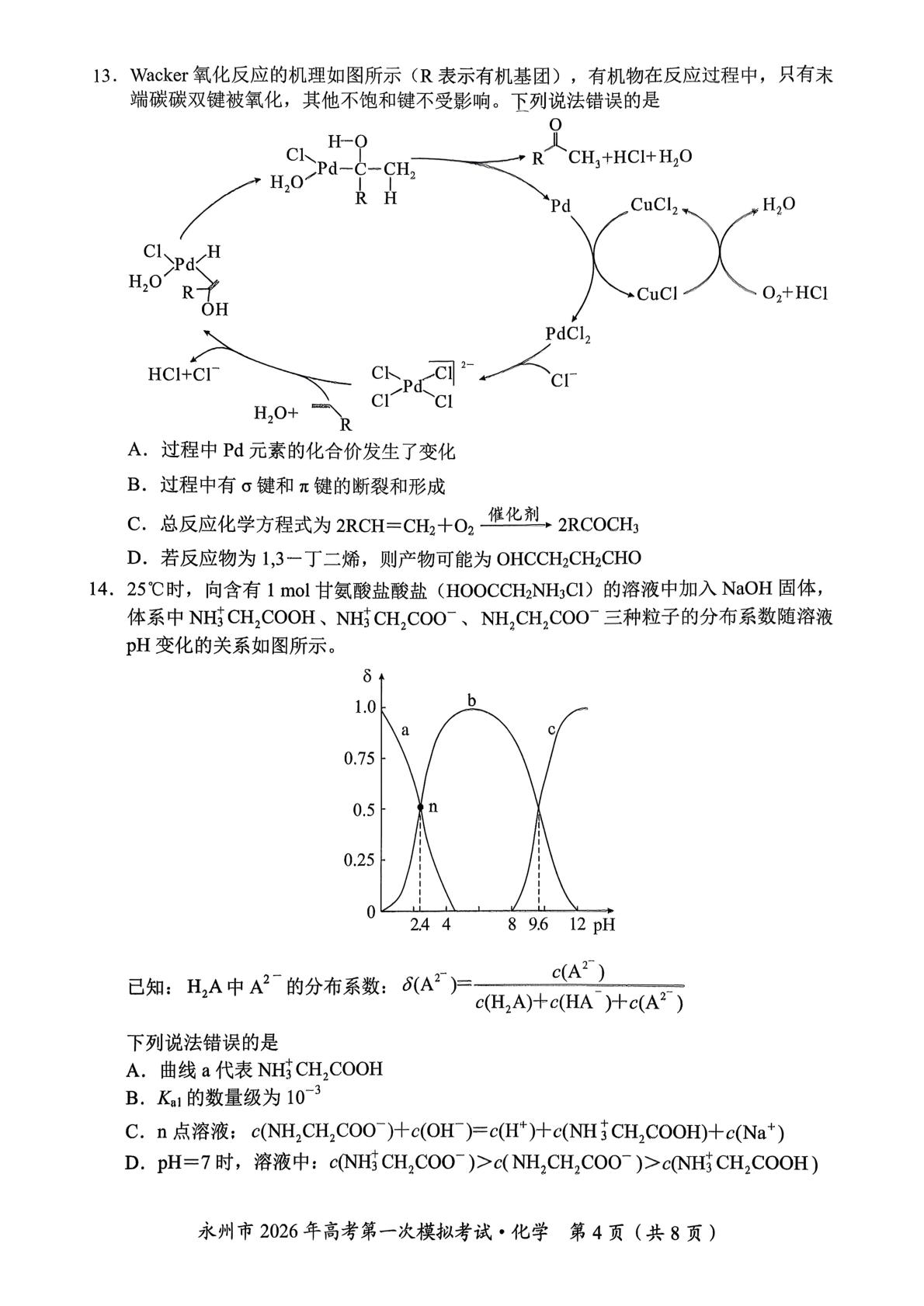
l3.Wacker氧化反应的机理如图所示(R表示有机基团),有机物在反应过程中,只有末
端碳碳双键被氧化,其他不饱和键不受影响。下列说法错误的是
H-O
CPd-C-CH2
R CH,+HCI+H,O
→H0
Pd
CuCl2。
H2O
Pd H
Cl
H201
R
CuC】
O,+HCI
OH
PdCl2
HCI+CI
CK,C2
CI
H20+
A.过程中Pd元素的化合价发生了变化
B.过程中有σ键和π键的断裂和形成
C.总反应化学方程式为2RCH=CH,+O,催化剂,2RC0CH,
D.若反应物为1,3一丁二烯,则产物可能为OHCCH2CH2CHO
14.25℃时,向含有1mol甘氨酸盐酸盐(HO0CCH2NHCI)的溶液中加入NaOH固体,
体系中NHCH2COOH、NHCH,COO、NH,CH,COO三种粒子的分布系数随溶液
pH变化的关系如图所示。
δf
1.0
b
a
0.75
0.5
0.25
0
2.44
89.612pH
已知:H,A中A2的分布系数:6(A2)=
c(A2)
c(HA)+c(HA )+c(A2
下列说法错误的是
A.曲线a代表NHCH,COOH
B.Ka1的数量级为103
C.n点溶液:c(NH,CH,COO)+c(OH)=c(H)+c(NH3CH,COOH)+c(Na)
D.pH=7时,溶液中:c(NH CH,COO)>c(NH,CH,COOˉ)>c(NH CH,COOH)
永州市2026年高考第一次模拟考试·化学第4页(共8页)
二、非选择题:本题共4小题,共58分。
15.(14分)一水硫酸四氨合铜(IⅡ){[CuNH)4]S04H2O}是一种深蓝色晶体,某兴趣小
组利用在CSO4溶液中滴加氨水的方法合成该物质,并测定晶体中铜元素的质量分数。
实验步骤如下:
步骤1制备氨水:向水中通入氨气。
步骤2制备铜氨溶液:向CuSO4溶液中滴加氨水,先产生蓝色沉淀,继续滴加氨水,
沉淀溶解,得到深蓝色的透明溶液。
步骤3析出晶体:向深蓝色溶液中加入适量95%的乙醇,并用玻璃棒摩擦器壁,静置,
有深蓝色晶体析出。
步骤4晶体纯化:减压过滤,用乙醇与浓氨水的混合液洗涤晶体,最后用丙酮洗涤,
低温干燥。
步骤5测定晶体中铜元素的质量分数:称取mg晶体,置于碘量瓶中,用煮沸的稀硫酸充
分溶解后,再加入过量KI溶液,盖好瓶塞,振荡,充分反应,静置5分钟,用c mol-LNa2S2O3
标准溶液滴定至淡黄色时,注入4mL0.2%的淀粉溶液,平行滴定3次,平均消耗mLNa2S2O3
溶液。
已知:[CuNH3)4]2++4H=Cu2++4NH4、2Cu2++4I=2Cul↓+I2、2S203+I2=2I厂+S4O6
请回答下列问题:
(1)[CuNH3)4]+的中心离子是
配位原子杂化方式为
(2)步骤1用氯化铵和熟石灰制备氨气的化学方程式为
(3)步骤3中用玻璃棒摩擦器壁的作用为
(4)步骤4中,用乙醇与浓氨水的混合液洗涤晶体,加入浓氨水的原因是
(5)步骤5中需要用到的仪器有
(填名称)。
A
B
(6)晶体中铜元素的质量分数为
(用含m、c、V的代数式表示)。下列操
作会导致测得的铜元素质量分数偏小的是
(填标号)。
A.稀硫酸未加热煮沸
B.滴定管尖嘴滴定前有气泡,滴定后消失
C.在滴定终点读取滴定管刻度时,俯视标准液液面
D.在配制Na2S2O3标准溶液时,烧杯中的溶液有少量溅出
永州市2026年高考第一次模拟考试·化学第5页(共8页)
16.(14分)一种利用含钉、铋的废料(主要成分为Ru、Bi2O3、SiO2等)为原料,制备
三氯化钉(RuCL3)和疏化铋(Bi2S3)的工艺流程如下:
NaOH+氧化剂
CH,OH
NaClO,
盐酸
废料→
氧化
碱浸
→滤液1→
还原
→Ru(OHD4
氧化
蒸馏
→RuO4(g)→吸收
→RuCl3
滤渣1
盐酸
Na,S
气体X
滤液2→酸化
→BiCl3→
沉铋
→Bi2S3
滤渣2
已知:①滤液1中有RuO、BiO2等离子;
100
②常温下,KpBi2S)=1.0x10-23。
回答下列问题:
60
(1)Bi的原子序数为83,在元素周期表中位于
区。
NaClO,
NaCIo
(2)“氧化碱浸”时,两种氧化剂在不同温度下对
40H
钉浸出率的影响如图所示,则适宜的氧化剂和反应温度分
20111111111111
190200210220230
别为
温度℃
(3)“还原”过程中有碳酸盐生成,写出该过程的离子方程式
(4)滤渣2的主要成分是
(填化学式)。
(5)气体X经NaOH溶液吸收后,可以循环利用,则X为
(填化学式)。
(6)“沉铋”时,若向1L1.5molL1BiCl3溶液中加入1.0LNa2S溶液,反应后混
合溶液中c(S2-)为1.0×10-7molL-1,则B#的沉淀率为(忽略溶液混合引起的体积
变化;保留三位有效数字)。
(7)钉酸铋(B2RuO6)可用于光催化,其晶胞结构(氧原子未画出)如图所示,晶胞
边长分别为anm、anm、cnm,晶胞棱边夹角均为90°。设阿伏加德罗常数的值为Na,Bi2RuO6
的相对分子质量为,则晶体的密度为
gcm3(列计算式)。
永州市2026年高考第一次模拟考试·化学第6页(共8页)
17.(15分)丙烯是一种重要的化工原料,可通过下面两种方法由C02合成。
方法一、CO2氧化丙烷脱氢法制丙烯
CO2在催化剂作用下和丙烷反应可生成丙烯,体系中主要发生如下反应:
反应I:C3H(g)十CO2(g)=C3H6(g)+CO(g)+HO(g)
△H
反应IⅡ:CHs(g十3C02(g)=6C0(g)+4H2(g)
△H2
回答下列问题:
(1)己知:C3H(g)=C3H6(g)+H2(g)
△H=+124kJmo11
C0(g)+H20(g)=C02(g)+H2(g)
△H=-41 kJmol-1
反应I的△H1=kJ.mol,该反应
(填标号)。
A.高温自发
B.低温自发
C.高温低温均自发
D.高温低温均不自发
(2)一定条件下,将1molC3H3和1molC02通入密闭容器中,发生上述反应,平衡
时各产物的物质的量随温度变化如下图所示。图中表示n(CH6)随温度变化的曲线是一,
n(H2O)在图示温度范围内几乎为0的可能原因是
2.0
2.0
L
12
1.5
1.5
s
1.0
1.0
0.5
0.5
父
0.0
H00.0
500
6508239501100
温度/K
(3)在TK、100kPa的恒温恒压密闭容器中,充入1molC3Hg和3 mol CO2,在催化剂
作用下进行上述反应,平衡时,C3H3的转化率为50%,C3H6的选择性S为80%。
n(CH)
己知:S(CH,)=消耗的n(C,Hg)s
×100%
①平衡时,n(CO)=
mol.
②该温度下反应I的分压平衡常数K,=
kPa(保留小数点后一位)。
方法二、CO2电解法制丙烯
装置如图所示:
米
丙烯←
02
C02
膜
H,SO4溶液
H,SO4溶液
(4)电解一段时间后,右室电极附近溶液pH
(填“变大”“变小”或“不
变”);生成丙烯的电极反应式为
永州市2026年高考第一次模拟考试·化学第7页(共8页)
18.(15分)H是一种香料的主要成分,分子结构中含有三个六元环。其一种合成路线如
下(部分反应条件和产物略去):
H
A
C.Hs
CH=C-CH,CI
催化剂
Cl2
NaOH(aq)
500℃
HCL
C1oH12Cl2
催化剂02
CH=CH,
HO-Br
①NaOH(aq)
G
CH,O,Br
催化剂
E
一定条件
②H
△浓H2SO4
H
己知:①RCH=CH2十CH2=CHR'
催化剂
CH,=CH2+RCH-CHR';
②C的核磁共振氢谱有6组吸收峰;
③E和F互为同系物。
回答下列问题:
(1)按系统命名法,A的名称为
(2)B→C的反应类型依次为
(3)C的结构简式为
(4)F中官能团的名称为
(5)D→E的化学方程式为
(6)F有多种同分异构体,同时满足下列条件的同分异构体有
种(不考虑立
体异构)。
①与FeCl3溶液发生显色反应
②能与NaHCO3溶液反应生成CO2
(7)以丙烯为原料,设计H[O一CH一C1OH的合成路线(无机试剂任选)。
CH,
永州市2026年高考第一次模拟考试·化学第8页(共8页)
资源预览图

1

2

3
4
相关资源
由于学科网是一个信息分享及获取的平台,不确保部分用户上传资料的 来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系学科网,我们核实后将及时进行处理。