天津市南仓中学2024-2025学年高一下学期第一次月考化学试卷
2025-04-02
|
8页
|
160人阅读
|
8人下载
资源信息
| 学段 | 高中 |
|---|---|
| 学科 | 化学 |
| 教材版本 | - |
| 年级 | 高一 |
| 章节 | - |
| 类型 | 试卷 |
| 知识点 | - |
| 使用场景 | 同步教学-阶段检测 |
| 学年 | 2025-2026 |
| 地区(省份) | 天津市 |
| 地区(市) | - |
| 地区(区县) | - |
| 文件格式 | |
| 文件大小 | 4.98 MB |
| 发布时间 | 2025-04-02 |
| 更新时间 | 2025-04-02 |
| 作者 | 匿名 |
| 品牌系列 | - |
| 审核时间 | 2025-04-02 |
| 下载链接 | https://m.zxxk.com/soft/51407688.html |
| 价格 | 0.00储值(1储值=1元) |
| 来源 | 学科网 |
内容正文:
天津市南仓中学2024至2025学年度第二学期
高一年级 过程性检测
(化学学科)
本试卷分为第I卷(选择题)和第II卷两部分,共100分,考试用时60分钟。第1
卷1至2页,第II卷3至4页
答卷前,考生务必将自己的姓名、考生号填写在答题纸上。答卷时,考生务必将答
案涂写在答题纸上,答在试卷上的无效
祝各位考生考试顺利
第1卷
注意事项:
1.每小题选出答案后,用铅笔将机读卡上对应题目的答案标号涂黑。如需改动,用
橡皮擦干净后,再选涂其他答案标号。
2.本卷共12小题,共36分
一、选择题(每小题3分,共36分)
1. 化学与人类生活、社会可持续发展密切相关。下列说法正确的是
A. 光化学烟雾、臭氧层空洞、温室效应的形成都与氮氧化合物有关
B. 明矶溶于水可形成氢氧化错胶体,常用于水体杀菌消毒
C. 漂粉精既可作棉、麻、纸张的漂白剂,又可用作环境的消毒齐
D. 石英甘涡耐高温,可用来加热熔化烧碱、纯碱等固体
2. 25C,下列离子或分子在指定条件下的同一水溶液中能大量共存的是
A. pH=2的溶液中:Fe”、K'、MnO:、C1'
B. 加入铭粉能产生H的溶液中:NHt、Fe*、sO、NO;
C. 滴加紫色石试液呈红色,一会儿变成无色的溶液中:Na'、A1”、Cl、so
D. c(Fe)-0.10mol.L'的溶液中:scN、KI'、H.o'
3. 已知N,表示阿伏加德罗常数,以下说法正确的是
A. 1mOlMg与足量0.或N反应生成MgO或MgN.均失去2N.个电子
B. 1.8g的NH4*离子中含有的电子数为1.1N
C. 标准状况下22.4LS0,中含原子数为4N
D. 在铜与疏的反应中,1mo1铜失去的电子数为2N
4.下列离子方程式正确的是
. 碳酸氢安与过量烧碱溶液:HCO+OH=II.O+CO-
B. 用铜与稀硝酸反应制备一氧化氮:Cu+4H+2NO:=Cu*+2NO个+2H.C
C. 实验室用疏酸错溶液和氛水制备氢氧化铅:Al*+3OH=Al(OH)。
D. 用氢氧化钢溶液吸收少量二氧化梳气体:sO。+2OH-SO?+H.O
CO.+N,其相对能量如图所
CO+N.O
示。下列反应的能量变化与该反应不相同的是
A. 疏酸和氢氧化纳反应
D. 氮气和氢气合成氛气
CO.+N.
. 氢气在氛气中燃烧
D. 盐酸和碳酸氢纳的反应
6. 2022年俄乌冲突升级引发能源短缺危机,新能源技术突显重要性。下列关于能源问
题的叙述正确的是
心氢能、天然气、风能、太阳能都是新能源
8. 天然气燃料电池工作时,天然气通入的一极是正极
C. 反应中能量变化的大小与可燃物的性质有关,与质量无关
D. 推广开发使用清洁能源,有利于实现人与自然的和谐共生
7. 下列有关应用的叙述错误的是
A. 二氧化疏具有漂白性,防腐和抗氧化等作用,可以作为食品添加剂
B. 硅具有半导体性能,高纯硅可用于制作光感电池
C. 氮化硅陶瓷属于传统无机非金属材料,可用于制造陶瓷发动机的受热面
1. 闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成
过性检嵩
第1页共4页
8. 下列说法不正确的是
》. HNO。→NO→NO,以上各步变化均能通过一步实现
B. 某气体能使湿润的红色石蕴试纸变蓝,该气体的水溶液一定显碱性
C. 铜与稀硝酸反应的离子方程式为3Cu十8H +2NO。=3Cu*+2N0++4H(
D. 在稀疏酸中加入铜粉,铜粉不溶解,再加入Cu(NO。).固体,铜粉仍不溶解
9. 一定条件下硝酸按受热分解的化学方程式为:5NH.NO.=2HNO.十4N。+9H,0,在反应中
被氧化与被还原的氮原子数之比头
B.5:4
A.5:3
1:1
D.3:5
10. 下列装置不能完成相应实验的是
-浓水
饱和NayCO;
溶液
乙
丙
A. 甲装置可用于制备氛气
B. 乙装置可除去C0.中少量的S0杂质
G. 丙装置可用于粗盐提纯
D. 丁装置可分离植物油和水的混合溶液
11.如图所示,是疏及其部分化合物的“价一一类”二维图
疏元素化合价
6
.w
,
.
..........................
,2
单质 氧化物 酸 盐 物质类别
f
下列说法正确的是
A. X点对应的物质只有一种
B 7点对应物质的化学式为H.sO
C. W点对应的物质在空气中易被氧化
D. X点对应的物质与足量O,在点燃条件下经一步反应可以转化为)
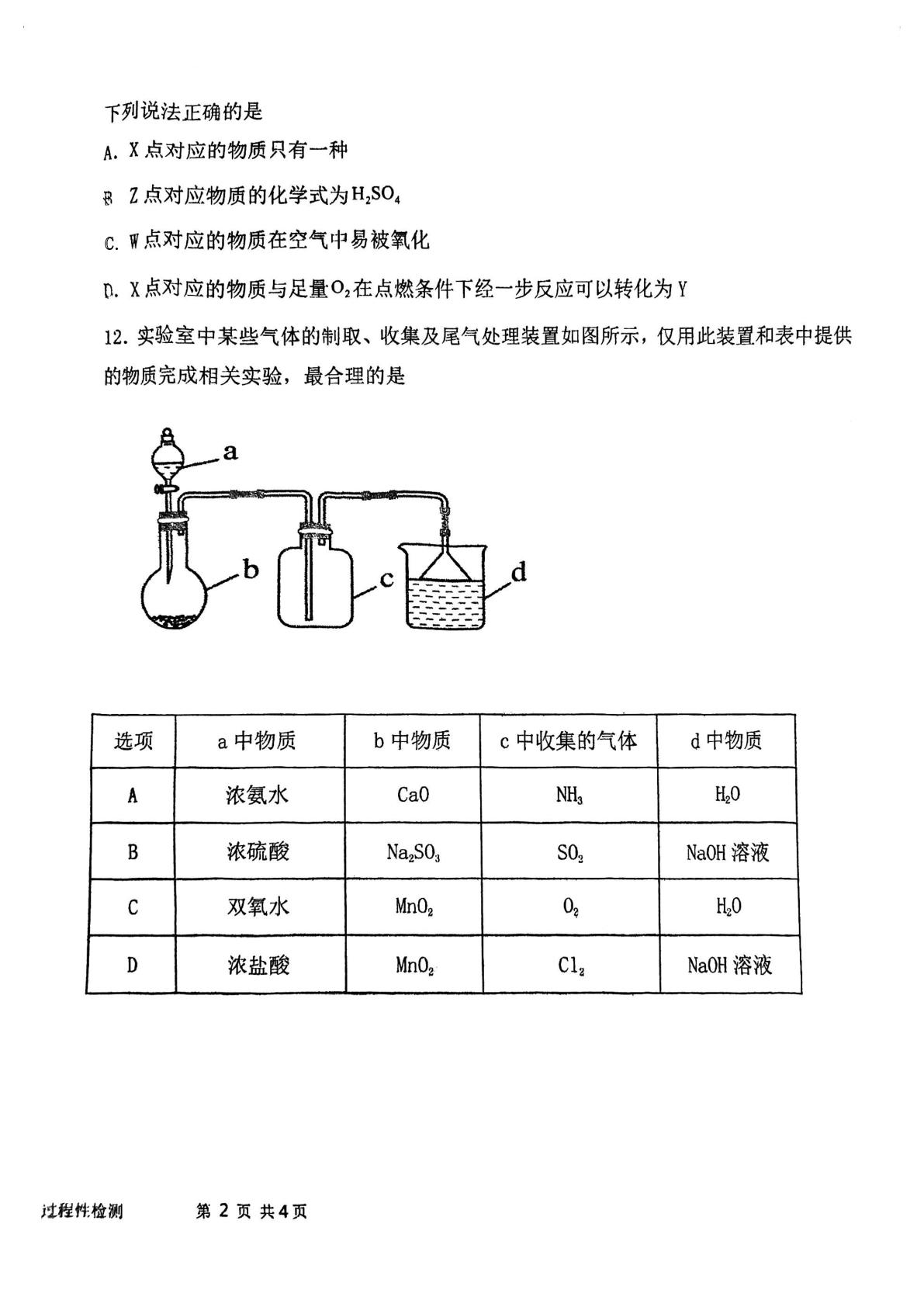
12. 实验室中某些气体的制取、收集及尾气处理装置如图所示,仅用此装置和表中提供
的物质完成相关实验,最合理的是
##
a中物质
b中物质
选项
c中收集的气体
d中物质
浓氛水
CaO
NH.
A
H0
浓疏酸
NaSO.
sO.
NaOH溶液
乙
双氧水
MnO
0.
H0
MnO2
浓盐酸
Cl.
_
NaOH浴液
过程性检测
第2页共4页
天津市南仓中学2024至2025学年度第二学期
高一年级过程性检测(化学学科)
第11卷
注意事项:
1.用黑色墨水的钢笔或签字笔将答案写在答题纸上
2.本卷共4小题,共64分。
二、填空题(每小题16分,共64分)
13.(每小题2分,共16分)阅读信息,回答以下问题
I.孩、氮元素是高中化学学习的两种重要非金属元素,其价类二维图分别如图所示
t化合价
一6 ..........1..
。
NO:
O:
,
②
o-.......
N
①
NH_
-NHC
氢化物单质 氧化物 酸 盐物类别
氢化物Y氧化物酸 盐
(1)c物质的浓溶液与金属铜发生反应的化学方程式为:
(2)a与HS发生反应的化学方程式:
(3)氛气是工业制硝酸的重要原料,写出①反应的化学方程式
(4)关于氮及其化合物的说法错误的是
A. 氮气分子结构稳定,常做保护气,不支持任何物质燃烧
B. NO、NO。均为大气污染气体,在大气中均可稳定存在
C. 可用浓盐酸检测输送NH.的管道是否发生泄漏
D HNO。具有强氧化性,可溶解铜、银等不活泼金属
II.根据图示回答问题
+O催化剂
B*^{2C
A
_Cu
H2O
#
(5)B的分子式为
高一年级(化学
(6)C物质颜色为
(7)D→B的化学方程式为:
(8)A→B的化学方程式为:
14.(每小题2分,共16分)图I,是实验室制备某种气体或验证某种气体性质的装置
#10
图I
图III
品红溶液
石灰水
I. 利用图I装置,可以制备纯净、干燥的氢气;
(1)仪器a的名称是
(2)装置A内发生的离子反应为
(3)装置B中的溶液为___溶液
II.利用图I装置,还可证明S0。漂白性、还原性及生成气体中含有C0。其中仪器b内
加入碳,a中加入浓疏酸,B、D中均为少量品红溶液,C中为足量酸性高酸钾溶液
E中为澄清石灰水
(4)证明S0.有漂白性的装置是
(填装置图对应大写字母)
(5)证明S0.具有还原性的现象是
(6)证明生成气体中含有C0的现象是
(7)D装置的作用是
III. 向如图III所示装置中缓慢地通入气体X,若关闭活塞,则品红溶液无变化,澄清石
灰水变浑浊:若打开活塞,则品红溶液褪色。
(8)下表符合X和Y的组合可能是
B
t→2
选项
A
D
s0.
HC1
NO.
x
Cl2
水
饱和NaHCO.溶液
NaSO.溶液
Na.SO.溶液
性检测
第3页共4页
15. I.近年来我国储氢碳纳米管研究获得重大进展,电狐法合成碳纳米管常伴有大量
物质一一碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式头
C+K.Cr,O,HSO(稀)=CO个+KsO.+C (sO)+8H,O
(1)完成并配平上述反应的化学方程式
(2)此反应的氧化剂是
(③此反应的氧化产物是
(4)疏酸在上述反应中表现出的性质是
(填字母序号)
A. 酸性
吸水性
B.氧化性
D. 还原性
(5)该反应中转移的电子数为
II. 化学电池的发明,改变了人们的生活
(6)将用导线相连的两个钻电极插入KOH溶液中,向两极分别通入H.和0,发生了原电池
反应,该原电池中正极的电极反应式为
(7))如图是银铛原电池装置的示意图。回答下列问题
7n_
_Ag
CuSO:溶液
银电极上的电极反应式为
(8) 上述银辞电池中的能证明化学能转化为电能的实验现象是
16.回答下列问题:
I. 硅是太阳能电池的重要材料,工业治炼纯硅的原理是
①Si0:+2C
1800~2000C
粗硅治炼:
-Si+2C0
300C
精炼硅:
②Si+3HC1
-SiHCl+H.
1100C
③SiHCl+H.
__-Si+3HC1
化学反应与能量变化如图所示,回答下列问题
高
年级
&能情
能量
Si+3HC1
Si+3HC1
Si-2C0
SiHCl,+H:
SiO-+2C
反应过程
反应过程
(1①是
_反应(填“吸热”或“放热”)
(2)0.5molSiHC1.发生反应③时,有 mol极性键断裂
(3)反应③破坏反应物的化学键所吸收的能量(填“大于”或“小于”或“等
于”)形成生成物中化学键所放出的能量
II. 能源是现代文明的原动力,化学电池在生产生活中有着广泛的应用
(4)如图,是常见的辞干电池构造示意图
己知:电池总反应Zn+2MnO+2NH:=Zn”+MnO+2NHg+H0说法正确的是__(填字母)。
a. 铲筒作负极
b. MnO:作正极
c. MnO发生还原反应
d. NHC1发生氧化反应
(5)根据构成原电池的本质判断,下列可以设计成
原电池的是__(填序号)
-石
A. Ca0(s)+Ho(1)=Ca(oH)。(aq)
-MnO
B. NaOH(aq)+HC1(aq)=NaC1(aq)+Hgo(1)
-NHCI糊
一简
C. 2C0(g)+0(g)=2C0(g)
D. Fe(s)+2FeCl.(aq)=3FeCl(aq)
III. 高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定
的放电电压。高铁电池的总反应为:3Zn+2K.Fe0.+8H.0→3乙n(0H).+2Fe(0H)+4K0H。
(6)放电时,负电极是
(7)放电时,正极附近溶液的碱性(填“增强”或“减弱”或“不变”)
(8)放电时,每转移__mo1电子,正极有1molKFe0.被还原
性检测
第4页共4页
资源预览图

1

2

3
4
相关资源
由于学科网是一个信息分享及获取的平台,不确保部分用户上传资料的 来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系学科网,我们核实后将及时进行处理。