辽宁省沈阳市郊联体2024-2025学年高一上学期期末考试化学试卷
2025-01-23
|
2份
|
7页
|
1614人阅读
|
76人下载
资源信息
| 学段 | 高中 |
|---|---|
| 学科 | 化学 |
| 教材版本 | - |
| 年级 | 高一 |
| 章节 | - |
| 类型 | 试卷 |
| 知识点 | - |
| 使用场景 | 同步教学-期末 |
| 学年 | 2025-2026 |
| 地区(省份) | 辽宁省 |
| 地区(市) | 沈阳市 |
| 地区(区县) | - |
| 文件格式 | ZIP |
| 文件大小 | 4.87 MB |
| 发布时间 | 2025-01-23 |
| 更新时间 | 2025-03-12 |
| 作者 | 匿名 |
| 品牌系列 | - |
| 审核时间 | 2025-01-23 |
| 下载链接 | https://m.zxxk.com/soft/50156665.html |
| 价格 | 1.00储值(1储值=1元) |
| 来源 | 学科网 |
内容正文:
辽宁省重点高中沈阳市郊联体
2024一2025学年度上学期高一年级期末考试试题
化学
命题人:沈阳市辽中一高中苏士杰审题人:沈阳市第八十三中学李峰
时间:75分钟满分:100分
可能需要用到的相对原子质量:H-1C-120-16Na-23A1-27Fe-56Ca-40C1-35.5
Ag-108
第I卷
一、选择题:本大题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只
有一项符合题目要求。
1.据东北新闻网报道,2024年11月12日,辽宁沈阳城市上空出现万米“丁达尔效应”,
阳光透过晨雾照射到大街小巷,现场蔚为壮观。产生该效应的分散系是()
A.水蒸气
B.溶液
C.胶体
D.浊液
2.劳动开创未来。下列劳动项目与所述的化学知识对应关系错误的是(
选项
劳动项目
化学知识
A
课外活动小组模拟侯氏制碱法制碱侯氏制碱法的“碱”指的是NaHCO3
B
环保工作者用漂粉精作泳池消毒剂
漂粉精的有效成分具有强氧化性
C
工人必须将模具干燥后再注入熔融钢水
铁与HO高温下会反应
D
工程师用钠钾合金作核反应堆传热介质
钠钾合金室温下呈液态便于传热
3.下列关于物质微粒间的作用说法正确的是(
A.CO2分子内存在着非极性共价键
B.含有共价键的化合物一定是共价化合物
C.化学键既可存在于分子内的原子间,又可存在于分子之间
D.水结冰时体积膨胀是由于水分子之间存在氢键
4.下列有关化学用语的表示方法错误的是()
A.C02的电子式::0:C:0:
B.Li的结构示意图:
432
C.含10个中子的氧原子:O
D.N2分子的结构式:N=N
5.设N为阿伏加德罗常数的值。下列说法正确的是()
A.7.8g过氧化钠中含阴离子数为0.2NA
B.1.6gO2和O3混合物中含氧原子数为0.1NA
C.1L0.1 mol-LNa2SO4溶液中含氧原子数日为0.4W
D.标准状况下22.4LC12与足量的铁充分反应,转移的电子数为3N
高一化学第1页(共6页)
6.在加入铝粉能放出氢气的无色溶液中,下列各组离子可能大量共存的是()
A.Na、K、CH:COO、CO3
B.Na、Cu2、SO?、C1
C.Mg2+、AI3+、SO、HC03
D.Ba2、K、SO3、Br
7.下列有关高中教材《化学必修第一册》中的示意图,表述错误的是(
B
C
D
电子层模型
合金内原子层间结构
NaCI溶液中的水合离子
H2与C12反应的过成
子核
88
88P
00+00-→09
00
A.A
B.B
C.C
D.D
8,下列离子方程式正确的是(
A.工业上用CuSO:溶液除HS气体:Cu2+S2—CuS到
B.将过量的CO2通入石灰水中:CO2十OH -HCO3
C.过氧化钠转化为氢氧化钠:203+2H0一4OH+021
D.Fe,O4和HC1的反应:FeO4十8H=Fe3++2Fe2++4HO
9.几种短周期元素的原子半径及主要化合价如下表:
元素代号
W
X
Y
Z
Q
原子半径/nm
0.160
0.143
0.102
0.089
0.074
主要化合价
+2
+3
+6、-2
+2
-2
其中Z和W、Q和Y分别属于同主族元素,下列叙述正确的是(
A.W、X的单质与稀硫酸反应速率:X>W
B.最高价氧化物对应水化物的碱性:W>Z
C.Q、Y的氢化物常温常压下均为无色气体
D.X、Y形成的简单离子核外电子层数相等
10.下列选项描述与对应图像相符的是(
导电能力
NalICO.
50
-50
-50
-250
2545
V(NaHSO
时问/s
核电荷数
时间/s
①
③
④
A.图①为向Ba(OH用2溶液中滴加等浓度的NaHSO4溶液时,溶液导电能力的变化
B.图②为新制饱和氯水在受到阳光直射时,溶液中c(H)的变化
C.图③为卤族元素单质的熔点随核电荷数递增的变化
D.图④为向盛有等物质的量的NaCO3和NaHCO3溶液的密闭容器中分别滴入等浓
度盐酸时气压的变化
高一化学第2页(共6页)
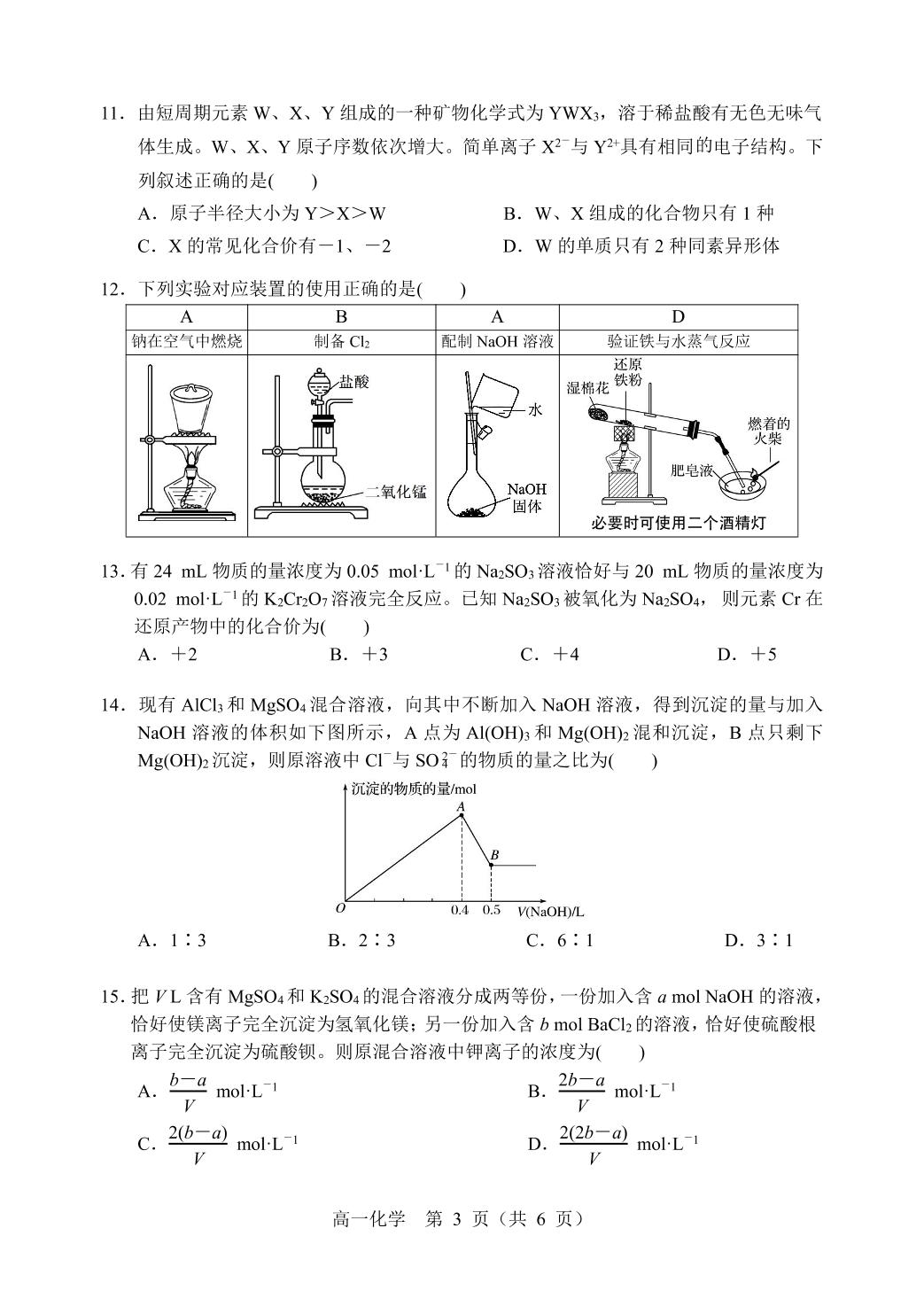
11.由短周期元素W、X、Y组成的一种矿物化学式为YWX3,溶于稀盐酸有无色无味气
体生成。W、X、Y原子序数依次增大。简单离子X2与Y2+具有相同的电子结构。下
列叙述正确的是()
A.原子半径大小为Y>X>W
B.W、X组成的化合物只有1种
C.X的常见化合价有一1、一2
D.W的单质只有2种同素异形体
12.下列实验对应装置的使用正确的是(
A
B
A
D
钠在空气中燃烧
制备C2
配制NaOH溶液
验证铁与水蒸气反应
还原
盐酸
湿棉花铁粉
水
燃着的
火柴
把皂液
二氧化锰
NaOH
固休
必要时可使用二个酒精灯
13.有24mL物质的量浓度为0.05molL1的Na2SO3溶液恰好与20mL物质的量浓度为
0.02molL1的KCrO7溶液完全反应。已知Na2SO3被氧化为NaSO4,则元素Cr在
还原产物中的化合价为()
A.+2
B.+3
C.+4
D.+5
14.现有A1Cl3和MgSO4混合溶液,向其中不断加入NaOH溶液,得到沉淀的量与加入
NaOH溶液的体积如下图所示,A点为AI(OH)3和Mg(OH2混和沉淀,B点只剩下
Mg(OHD2沉淀,则原溶液中CI与SO的物质的量之比为()
沉淀的物质的量mol
0.40.5Na0H)L
A.1:3
B.2:3
C.6:1
D.3:1
15.把VL含有MgSO4和KSO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,
恰好使镁离子完全沉淀为氢氧化镁:另一份加入含b mol BaCl2的溶液,恰好使硫酸根
离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为(
)
A.
b-a
mol-L
B.
2b-a mol-L
C.2(b-a)
2 mol-LI
D.2(26-a)mol-L-
高一化学第3页(共6页)
第Ⅱ卷
二、非选择题:本大题共4题,共55分。
16.(14分)下图中A、D、G、I是常见的单质,其它为化合物,有些反应中的部分物质被
略去。C具有两性,反应①常被应用于野外焊接钢轨。F是海水中含有盐的主要成分,
J为D、G反应产物形成的水溶液。
A
高温「
H溶液E
B
D
B
回DK
M-
空气中
N
电解
F溶液
④
(红褐色
固体)
(1)单质G呈
色,B的化学式为
(2)写出反应③的化学方程式:
(3)写出J与D反应生成K的离子方程式
写出反应②的离子方程式:
(4)在空气中,絮状沉淀物M由■
色迅速变成
色,过一段时间后才最终变为
红褐色。写出反应④的化学方程式:
(⑤)在一次野外焊接钢轨作业中,工作人员测得某处钢轨裂缝容积为28mL,已知单质
D的密度是8g©m3,根据反应①计算这次焊接中需要消耗单质A的质量是g。
17.(14分)近年来,辽宁省在环境保护、自然资源综合应用等方面取得显著成果。辽宁省
沙地研究所彰武县章古台镇建成省第一片“碳中和林”,具有吸收二氧化碳、净化空气
等重要生态功能。辽宁有充足的水、天然气(CH)资源,辽宁海域食盐资源丰富。
(1)通过现代实验手段(如X射线衍射法等)可以测定某些分子的空间结构,例如:
CO2是形,H20呈
形,CH4呈
形。
(2)请用电子式表示NaCI的形成过程:
(3)据中国质量新闻网报道,目前8家氟化工产业链上企业与辽宁工程技术大学联合制
定《辽宁省氟化工产业链供应链质量联动提升试点工作方案(2024一2025年)》。已知
HF气体的水溶液称氢氟酸,氢氟酸为弱酸。
①氟位于元素周期表的第二周期第族:氢化物的沸点:HFHO(填“>”或“<):
气态氢化物的稳定性:HF(g)HO(g)(填>”或“<")。
②写出氢氟酸和NaOH溶液反应的离子方程式:
(4)辽宁丹东硼矿贮量达3亿吨,硼的最高价氧化物对应的水化物为硼酸(HBO)。
①非金属性:硼
碳(填“>”或“<):判断酸性:硼酸
碳酸(填“>”或“<)。
②硼有两种天然同位素B和;B,硼元素的近似相对原子质量为10.80,则B和;B
的原子个数之比为
高一化学第4页(共6页)
18.(14分)探究实验(特别是对比探究)对于研究中学化学规律有重要作用。
「,某化学小组用如图所示装置进行实验。
浸有NaBr溶
浸有淀粉-K1
液的棉花球
溶液的棉花球
干燥的。湿润的
浓硫酸有色布条有色布条
NaOH溶液
(I)f装置中NaOH溶液与Cl2反应的离子方程式为:
(2)下列说法不正确的是
(填字母,第Ⅱ卷的选择题不一定是单选,以下同)。
A.b处干燥的有色布条不褪色,c处湿润的有色布条能褪色
B.d处发生反应的离子方程式为C2+2Br—-2C1厂十Br2
C.e处棉花球变成蓝色,说明Br2的氧化性比2强
D.实验结束后,利用a→f处余下溶液相互反应不可能再生成C2
Ⅱ,H2O2是难电离的物质,遇催化剂或受热易分解。铜与过量HO2作用的实验如下:
+NaS0.溶液
①)
无明显现象
过量30%I,0,
→铜片溶解,溶液变蓝,
钢片配
+稀H2SO,
少吊无色气体生
(3)实验②中Cu溶解使溶液变蓝的离子方程式为:
(4)之后片刻,溶液中产生少量无色气体(可使带火星木条复燃)的化学方程式为:
(⑤)比较实验①和②,判断下列说法正确的是
A.H的氧化性强于Na
B.H既不是氧化剂,又不是还原剂
C.实验②中,从溶液变蓝到产生少量无色气体的过程中,HO2只作氧化剂
D.物质的氧化性的强弱可能与溶液的酸碱性有关
Ⅲ,某同学利用如图装置(夹持仪器已略去)对比探究纯碱和小苏打的性质:
NalICO.
Na CO
Ca(OH)
溶液
h
(6)观察到有白色沉淀生成的烧杯是
(填字母“a”或“b")
比较热稳定性:碳酸钠
碳酸氢钠(填“>”或“<”。
(7)如果将16.8 g NaHCO3加热一段时间。将加热产生的气体全部通入足量的Ca(OD2
溶液,最终得到白色沉淀5.0g。如果将加热产生的气体全部通入400mL0.2mol/LNaOH
溶液中充分吸收,不考虑CO3的水解以及HCO;的水解和电离,求所得溶液中CO
和HCO;的物质的量之比为
高一化学第5页(共6页)
19.(13分)混合物的分离、检验是化学知识的重要应用。
(1)铜铝合金被称为“铝青铜”,原因是这种合金的颜色与青铜(铜锡合金)相似。现收集
切割铝青铜时留下的粉末进行如下探究:
铝青铜粉末
足量NaOH溶液
FeCl3溶液
剩余固体
黄绿色溶液
反应①
反应②
反应①的离子方程式为:
反应②的化学方程式为:
(2)为检验黄绿色溶液是否含Fe+,取少许,滴入
(填试剂名称,用汉宇
填写)溶液,若溶液呈
色即可证明。
(3)上述“黄绿色溶液”便是制造印刷电路板时残留废液的主要成分,工程师欲从中回收
铜,并获得FeC13溶液,设计如下方案:
滤液B
合并
废液
过量金属A
FeCl溶液
加入F
过滤
滤液
加入过量D
滤渣C
过滤
铜
①滤渣C的化学式为
②试剂F宜选用
(填选项序号),通入F的目的是
A.酸性KMnO4溶液
B.氯水
C.溴水
(4)取30.0mL待测废液,加入足量的AgNO3溶液,过滤、洗涤、干燥后得25.83g白
色沉淀。则废液中c(C1)=
高一化学第6页(共6页)高一化学 第 1 页(共 1 页)
2024-2025上学期郊联体期末考试高一化学答案与评分标准
一、选择题:1~15 题,每小题 3 分,共 45 分。每小题只有一个选项符合题目要求。
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 C A D A B A C B B D C D B C D
二、非选择题:16~19 题,共 55 分。
16.(14分)(1)黄绿(1分,答黄或绿不给分) Fe2O3(1分)
(2)Al2O3+2NaOH+3H2O===2Na[Al(OH)4](或:Al2O3+2NaOH===2NaAlO2+H2O,2分,
配平有错扣 1分,将“Na[Al(OH)4]”写成“NaAl(OH)4”不扣分)
(3)2Fe3++Fe===3Fe2+(2分,配平错不给分) 2Cl-+2H2O=====
电解
2OH-+H2↑+Cl2↑(2分,不
写“电解”或“通电”条件扣 1分,配平有错扣 1分)
(4)白(1分) 灰绿(1分) 4Fe(OH)2+2H2O+O2===4Fe(OH)3(2分,配平错不给分,生成物
写↓了不扣分)
(5)108(2分,将单位“g”抄到答题纸上不扣分)
17.(14分)(1)直线(1分) V(1分,答“角”形也可) 正四面体(1分,写成“四面体”也可)
(2) (2分,可以都用“点”表示,没写弯键号扣 1分,没写弯键号但电子
式写对给 1分;箭号写等号的扣 1分;但是只写电子式不给分,因为强调的是形成过程....)
(3)①ⅦA(1分,“第七主”等不给分) <(1分) >(1分) ②HF+OH-===F-+H2O(2分)
(4)①<(1分) <(1分) ②1:4(或1
4
,或 0.25,2分)
18.(14分)(1)2OH-+Cl2===ClO-+Cl-+H2O(2分,配平有错扣 1分)
(2)CD(2分,对一个给 1分,有错不给分)
(3)Cu+H2O2+2H+=== Cu2++2H2O(2分,配平有错扣 1分)
(4)2H2O2Cu
2+或 CuSO4或催化剂或△2H2O+O2↑(2分,没写条件扣 1分,配平有错扣 1分)
(5)BD(2分,对一个给 1分,有错不给分)
(6)b(1分) >(1分)
(7)3:2(或3
2
,或 1.5,2分)
19.(13分)(1)2Al+2OH-+6H2O===2[Al(OH)4]-+3H2↑(或 2Al+2OH-+2H2O===2AlO-2+
3H2↑,2分,配平有错扣 1分,将“[Al(OH)4]-”写成“Al(OH)-4”不扣分)
2FeCl3+Cu===2FeCl2+CuCl2 (2分,配平有错扣 1分)
(2)硫氰化钾(或其他硫氰化物,1分,“氰”字错不给分) 红(或血红,1分)
(3)①Fe、Cu (2分,只答 Fe 或 Cu给 1分)
②B(1分) 将溶液中的 Fe2+转化(或氧化)为 Fe3+(或写离子反应,合理即可,2分)
(4)6.0 mol·L-1 (或 6.00mol·L-1或 6 mol/L,2分,没写单位扣 1分)
资源预览图

1

2
3
相关资源
由于学科网是一个信息分享及获取的平台,不确保部分用户上传资料的 来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系学科网,我们核实后将及时进行处理。