湖南省长沙市雅礼中学2026届高三上学期月考(一)化学试题
2025-08-18
|
2份
|
12页
|
649人阅读
|
29人下载
资源信息
| 学段 | 高中 |
|---|---|
| 学科 | 化学 |
| 教材版本 | - |
| 年级 | 高三 |
| 章节 | - |
| 类型 | 试卷 |
| 知识点 | - |
| 使用场景 | 同步教学-阶段检测 |
| 学年 | 2025-2026 |
| 地区(省份) | 湖南省 |
| 地区(市) | 长沙市 |
| 地区(区县) | - |
| 文件格式 | ZIP |
| 文件大小 | 5.15 MB |
| 发布时间 | 2025-08-18 |
| 更新时间 | 2025-08-29 |
| 作者 | 匿名 |
| 品牌系列 | - |
| 审核时间 | 2025-08-18 |
| 下载链接 | https://m.zxxk.com/soft/53506839.html |
| 价格 | 1.50储值(1储值=1元) |
| 来源 | 学科网 |
内容正文:
雅礼中学2026届高三月考试卷(一)》
化学参考答案
一、选择题(本题共14小题,每小题3分,共42分,每小题只有一个选项符合题意)
题号
123
4
56
789
10
111213
14
答案
A
BD
B
0
B
D
1.A【解析】聚氯乙烯(PVC)薄膜中有氯乙烯单体残留,危害人体健康,A项错误。线型酚醛树脂具有热塑性,
受热易软化,B项正确:天然橡胶的主要成分是顺式聚异戊二烯,含有碳碳双键,能使溴水褪色,D项正确。
2.B【解析】100g30%的HCHO溶液中含甲醛30g,即1mol,但是溶剂水中也有氧原子,A项错误:
1mol[Cu(NH3):]2中N与Cu2+形成配位键,所以g键数目为16NA,B项正确;Cu与硫粉反应生成Cu2S,
1 mol Cu完全反应转移1mol电子,C项错误:不能确定其准确的物质的量,D项错误。
3.D【解析】B.浓硫酸的密度比水的密度大,浓硫酸溶于水放热,故稀释浓硫酸时应将浓硫酸沿烧杯内壁缓慢倒
入盛水的烧杯中,并用玻璃棒不断搅拌,B项合理:C.NaCl的溶解度随温度的升高变化不明显,从NC溶液中
获得NaCl晶体采用蒸发结晶的方法,C项合理:D.定容阶段,当液面在刻度线以下约1cm时,应改用胶头滴管
滴加蒸馏水,D项不合理。
4.D【解析】碳酸锰、碳酸铜难溶于水,离子方程式应为MnCO,+2H+一Mn2+十H2O+CO2↑、CuCO3十2H
-一Cu++H2O十CO2↑,A错误:加入MnO2将Fe2+转化为Fe3+的离子方程式应为MnO2十2Fe2++AH
一2e3++M2+十2H2O,B错误:除去Cu+不能通入过量的氨气,氨气过量时反应的离子方程式应为
Cu++6NH+2HO一[Cu(NH)4](OH)2十2NHt,C错误;若向溶液中加入MnS除去Cu2+,转化为更难
溶的CuS:Cu+(aq)+MnS(s)一Mn2+(aq)+CuS(s),D正确。
5.D【解析】A.同一主族从上到下,碱金属元素原子的半径逐渐增大,金属键逐渐减弱,金属键越弱,熔、沸点越
低,A正确:B.王水是浓硝酸和浓盐酸按体积比1:3混合而成,能溶解金和铂,是因为浓盐酸提供的大量CI
与金属离子形成稳定的配离子,增强了金属的还原性,从而使反应能够进行,B正确:C,晶体的自范性是指在适
宜条件下,晶体能够自发地呈现多面体外形,缺角的NaCI晶体在饱和NaCI溶液中变为完美的立方体,体现了
晶体的自范性,C正确:D.(C2HNH)NO和NH,NO处于固态时都属于离子晶体,(CHNH)NO3的熔点
低于NHNO3是因为引入的乙基使离子间作用力减弱,而不是改变了晶体类型,D错误。
6.B【解析】乙醚的结构简式为CH,CH,OCH,CH,B项错误;H,0中0的价电子对数为3+6-)一3-=4,所
2
以VSPR模型为四面体,C项正确:CO中碳原子为sp杂化,CH COOH的甲基中碳原子为sp杂化,
CHCOOH的羧基中碳原子为sp杂化,D项正确。
7.C【解析】A.由PM的结构简式可知,PM中含有酯基、醚键和羟基三种官能团,A项正确:B.M中含有甲基和
亚甲基等,故M分子中不可能所有原子共面,B项正确:C.由PM的结构简式可知,理论上,合成1 mol PM需
要消耗n mol M和1mol苯甲醇,C项错误;D.1molM含有的酯基与足量NaOH溶液反应,消耗1mol
NaOH,D项正确。
8.C【解析】A.装置甲采用固液不加热制备氯气,二氧化锰固体和浓盐酸制备Cl2需加热,故A错误:B.装置乙
的作用是除去氯气中的HCI,同时可作安全瓶,以监测装置丙中是否发生堵塞,故B错误:C.装置丁中碘和氯
气反应生成1C3,三氯化碘的熔点为33℃,沸点为77℃,可采用水浴加热,故C正确:D.IC13易与水发生反应,
同时可能还有C2未反应完,所以装置戊的作用是吸收多余的C2、防止外界水蒸气进入装置丁,换成氯化钙无
法吸收多余的C2,故D错误。
9.B【解析】砷化镓废料“溶解”过程中,H2O2受热易分解,A正确:实验室“结晶”时主要用到的仪器有酒精灯、
烧杯、蒸发皿、玻璃棒,B错误;“滤渣2”的主要成分为Fe(OH)a、Ca(AsO:)2、CaSO4,C正确;电解
NaGa(OH)1]溶液时,阴极发生还原反应生成金属镓,电极反应式为[Ga(OH),]-十3c一Ga十4OH,
D正确」
10.B【解析】由图可知,与H距离最近且等距离的Mg2+的个数是3,则H的配位数为3,A项错误;Mg2位于
品胞的顶点和体心,该晶胞中Mg的个数为8×日+1=2,B项正确:该晶胞的体积为cX10cm,Mg
化学试题参考答案(雅礼版)一1
的个数为2,H的个数为4区2十2=4,一个品胞中含有2个MgH,故品体密度为V。×10g/am,C项
错误:Mg(1)和Mg(1)之间的距离等于晶胞体对角线长度的一半,为2@+已m,D项错误。
2
11.D【解析】加热促进水解,铁离子水解生成氢氧化铁,则实验①中,Fe2(S),)3溶液显浅黄色的原因是Fe3+水
解产生了少量的Fc(OH)3,A项正确:由Fe3+十3H2O一Fe(OH)3十3H可知,酸化后加热,溶液颜色无明
显变化,而氢离子抑制水解,则实验②中酸化对Fe3+水解的抑制程度大于升温对F3+水解的促进程度,B项
正确:加入NaCI后,溶液立即变为黄色,发生反应:Fe3++4CI十2HO一[FcCl,(HO)2],
[FeCL,(H,O)2]丁为黄色,加热时平衡正向移动,溶液颜色变深,C项正确:实验④中存在Fe+十ACI+2HO
[FcCl,(H2O)2],升高温度平衡正向移动,溶液颜色变深,因此不能证明升温一定是因为Fe3+水解平衡
正向移动,D项错误。
12.B【解析】电极b上的电极反应式为Br一6e十3H2O一一BrO方+6H,澳元素的化合价上升,失去电子发
生氧化反应,为阳极,连接电源正极,A项正确:电极a上的电极反应式为2H2O十2e一H2↑十2OH,结合
选项A可知,电解过程中消耗H2O和Br,而催化阶段BO被还原成Br循环使用,故加入Y的目的是补
充H,0,维持NaBr溶液为一定浓度,B项错误;电解总反应式为Br十3H,0也:BrO5十3H,↑,C项正确:
催化阶段,澳元素的化合价由十5价降至一1价,生成1 mol Br得到6mol电子,氧元素的化合价由一2价升
至0价,生成1molO2失去4mol电子,根据得失电子守恒,反应产物的物质的量之比n(O2):n(Br)=6:4
=3:2,D项正确。
13.C【解析】反应①吸热,反应②放热,升高温度,反应①平衡正向移动,反应②平衡逆向移动,两者均有利于异
丁烯的制备,A正确:平衡常数反映了反应进行的程度,由于K1远大于K2,主要进行反应①,因此高于190℃
时温度对异丁烯的平衡产率影响不大,B正确;若只有异丁烯、水和二聚异丁烯生成,由于可逆反应还有剩余
的异丁醇没有反应完,根据元素守恒可知,C。(异丁醇)=c(异丁烯)十2c(二聚异丁烯)十c(异丁醇),C错误:
190℃时,恒压条件下增大水和异丁醇的比例,相当于减压,由图可知异丁烯产率增加,反应①平衡右移,反应
②平衡左移,不利于反应②的进行,D正确。
14.D【解析】溶液pH增大时,H2B的浓度减小、HB的浓度先增大后减小,B-的浓度增大,则曲线Ⅱ表示
pc(HB)与pH的关系、曲线I表示pc(HB)与pH的关系、曲线Ⅲ表示pc(B)与pH的关系,A正确;由图
可知,pH=6时,溶液中微粒的浓度大小顺序为c(HB)>c(B)>c(H2B),B正确:由图中X点可知,溶液
中c(H,B与c(HB)相等时,溶液pH为1.9,则K(H,B》=HBcH=c(H)=101,同理由
c(H2B)
c2(HB)
2(HB)·c(H)=K=109
Y点可知,K.(H,B》=10,溶液中B,BB,Bㄧ术-10=10,
C正确:调节溶液pH的过程中,由元素守恒可知,溶液中HB、HB、B的物质的量之和不变,故在不同的
pH条件下,三者浓度之和不变,D错误。
二、非选择题(本题共4小题,每空2分,共58分)
15.(16分)(1)无水CaC
(2)分液漏斗
(3)促进
OMgBr水解产生三苯甲醇
(4)A
(5)趁热过滤,(滤液)冷却结晶
(6)2PhMgBr+PhCOOC.H;THEPh,COMgBr+C.H.OMgBr
(7)38.5%偏低
【解析】(I)仪器C为球形千燥管,格氏试剂(RMgBr)性质活泼,可与水、酯等物质反应。为了防止格氏试剂与
水反应,球形千燥管可装无水CaCl2。
化学试题参考答案(雅礼版)一2
(2)在分液漏斗中将有机相和水相分离:洗涤有机相时也在分液漏斗中进行洗涤分离;分离有机相和洗涤有机
相时均需使用分液漏斗。
(3)滴加饱和NH,CI水溶液促进
OMgBr水解产生三苯甲醇。
(4)格氏试剂(RMgBr)性质活泼,可与水等物质反应。
(5)粗产品用80%乙醇水溶液热溶解,再经活性炭脱色,需将活性炭趁热过滤除去后,滤液冷却结晶,抽滤后
得白色固体产品。
(7)加入PhMgBr20mmol,苯甲酸乙酯6.3mmol,根据反应的化学方程式可知PhMgBr过量,生成的三苯甲
0.63g
醇理论上为6.3mmol,实际为0.63g,三苯甲醇的产率为6.3×10m01X260gmaX100%≈38.5%:若水
相未用乙酸乙酯萃取且合并有机相,实际得到的三苯甲醇减少,则导致测定结果偏低。
16.(14分)(1)2s22p
(2)增大矿石和空气的接触面积,提高反应速率,使反应更充分
(3)BaSO
(4)H与F结合生成HF,而HF是挥发性弱酸,随着c(H)增大,HF挥发性增强,使c(F)减小,CeF+的
浸出率下降
(5)还原6HC05+2Ce3+一Ce2(CO)3↓+3CO2↑+3H2O
(6)加入NaOH溶液,使难溶于强酸的固体B发生如下沉淀转化反应:Ce(SO,)3·Na:SO,·nH2O(s)+
6OH-(aq)一2Cc(OH)3(s)+4SO(aq)+2Na(aq)+nHO(I),转化为可溶于强酸的Ce(OH)3,便于后
续用盐酸溶解得到含Ce3+的溶液[或Ce2(SO,)3·NaSO4·nH2O(s)一2Ce3+(aq)+4SO(aq)+
2Na(aq)+HzO(I),加入NaOH溶液,Ce3+与OH结合,c(Ce3+)下降,平衡正移,固体B转化成可溶于强
酸的Ce(OH)a,便于后续用盐酸溶解得到含Ce3+的溶液]
【解析】(2)利用高压空气将矿石粉吹起并悬浮,形成类似液体沸腾的状态可以增大矿石和空气的接触面积,提
高反应速率,使反应更充分。
(4)硫酸浸出过程中,H与F结合生成HF,而HF是挥发性弱酸,随着c(H)增大,HF的挥发性使c(F)
减小,CeF3+的浸出率下降。
(5)加入硫脲将溶液中的Ce(Ⅳ)还原为Ce3+,即硫脲作还原剂。
(6)根据已知信息可知Ce2(SO,)3·NaSO·nH2O难溶于水也难溶于强酸,加入NaOH,使其发生如下沉淀
转化反应:Cc(SO,)3·Na2SO,·nH2O(s)+6OH(aq)一2Ce(OH)3(s)+4SO(aq)+2Na(aq)+
nHOI),转化为可溶于强酸的CC(OH)3,便于后续用盐酸溶解得到含CC3+的溶液。或:CC2(SO1)3·
Nae SO,·nH2O(s)=2Ce3+(aq)+4SO(aq)+2Na(aq)十nH2O(I),加入NaOH溶液,Ce3+与OH结
合,c(Ce3+)下降,平衡正移,固体B转化成可溶于强酸的Ce(OH)3,便于后续用盐酸溶解得到含Ce3+的溶液。
17.(14分)(1)对氯苯胺或4-氣苯胺
(2)保护氨基取代反应
(3)F30
(4)bG
化学试题参考答案(雅礼版)一3
OH
(6)2
一定条件
+2H2O
H
【解析】(1)由合成路线中A的结构简式,可知有机物A的名称为对氯苯胺或4一氯苯胺。
(2)由F→G又生成氨基可知过程A→B的作用是保护氨基。G→H属于取代反应。
(4)a.E含有苯环、碳碳三键、甲基,故分子中碳原子的杂化方式有3种,正确:b.消去反应会产生不饱和结
构,E→F的反应没有产生不饱和结构,故不是消去反应,b错误;C.由结构可知,化合物H的分子式是C4
H.F CINO2,难溶于水,c错误。
(5)满足①含有苯环:②H-NMR谱显示有6种不同化学环境的氢原子:③能发生水解反应,产物之一是甘氨
酸的化合物N的同分异构体有)
OH
(6)根据已知信息,可知J的结构简式为
,将其在一定条件下催化氧化可生成物质K:
H
OH
一定条件
十02
2
+2H2O。
H
18.(14分)(1)BaC2+2H2O→Ba(OH)2+HC=CH↑
(2)①106②105B
(3)①BaO②速率不变至BaC2产率接近100%
(4)2CO2+10H*+10e-C2H2+4H2O
【解析】(1)Ba、Ca元素同主族,所以BC2与水的反应和CaC2与水的反应相似,其反应的化学方程式为
BaC2+2HO→Ba(OH)2+HC=CH↑.
(2)①反应I+反应Ⅱ得BaCO(s)十4C(s)=BaC(s)+3CO(g),所以其平衡常数K=K(I)XK(Ⅱ)=
(部八,由图1可知,1585K时K(1)-102,K()-105,即(部-10×1015-10,所以
p=10×(105Pa)3=1016Pa3,则K。=po=106Pa3。
②由图1可知,1320K时反应I的K()=10=1,即K(I)=(部=1,所以%,=(10P,即w
10Pa:若将容器容积压缩到原来的,由于温度不变,平衡常数不变,重新建立平衡后p应不变,即p0=
105Pa。
(3)①由图2可知,1400K时,BaC2的产率为0,即没有BaC2,又实验表明BaB)已全部消耗,所以此时反应
体系中含Ba物种为BaO。
②图像显示,1823K时BaC2的产率随时间t~2由0开始呈直线上升到接近100%,说明该反应速率为一
个定值,即速率保持不变。
化学试题参考答案(雅礼版)一4雅礼中学2026届高三月考试卷(一)
化
学
命题人:朱鹏飞
审题人:姚相仁
得分:
本试题卷分选择题和非选择题两部分,共8页。时量75分钟,满分100分。
可能用到的相对原子质量:H~1C~12N140~16Na23Mg24C~35.5Fe~56Br~80
第I卷选择题(共42分)
一、选择题(本题共14小题,每小题3分,共42分,每小题只有一个选项符合题意)
1.高分子材料在各个领域应用广泛。下列说法不正确的是
A聚氯乙烯薄膜的透明性好,具有防潮、防水等性能,广泛用作食品包装袋
却
B.线型酚醛树脂可由苯酚和甲醛在浓盐酸催化下合成,受热易软化
C.聚对苯二甲酰对苯二胺纤维(芳纶1414)具有强度高、密度小、热稳定性高等性能,可制成消防服、防切
割耐热手套
D.天然橡胶的主要成分顺式聚异戊二烯能使溴水褪色
召
2.HCHO还原[Cu(NH)4]+的离子方程式为HCHO+2[Cu(NH)4]++2H2O一2Cu↓+6NHt+
2NH十CO?,NA为阿伏加德罗常数的值。下列说法正确的是
A100g30%的HCH0溶液中含氧原子数目为NA
都
B.1mol[Cu(NH)4]+中g键数目为16Na
C.1 mol Cu与足量的硫粉反应转移电子的数目为2NA
图
D.等物质的量的H2O与NH所含电子数均为10NA
3.下列实验的对应操作中,不合理的是
浓硫酸
蒸馏水
眼晴注视锥形瓶中溶液
A用HC标准溶液滴定NaOH溶液
R稀释浓硫酸
蒸馏水
液面离刻度
线约1cm
C,从提纯后的NaCl溶液获得NaCl晶体
D.配制一定物质的量浓度的H,C,O,溶液
化学试题(雅礼版)第1页(共8页)
4.以碳酸锰铜矿(主要成分为MnCO、CuCO,还含有FezO,、Fe0等杂质)为原料制备硫酸锰的主要过程
第一步溶于稀硫酸、第二步氧化F+、第三步除去Cu+等,有关离子方程式书写正确的是
A.第一步溶于稀硫酸主要发生反应:CO+2H+一H20十CO2个
B.加人MnO2将Fe2+转化为Fe+:MnO2iFe2++4HtFe++Mn2++2H2O
C.可以向溶液中通人过量氨气除去Cu+:Cu2++2NH·H2O一Cu(OH)2+2NHW
D.若采用向溶液中加人MnS除去Cu+:Cu2+(aq)+MnS(s)一Mn2+(aq)十CuS(s)
5.结构决定性质,性质决定用途。下列相关事实对应的解释不正确的是
选项
事实
解释
随着核电荷数的增加,碱金属元素的单质熔、沸
同一主族从上到下,碱金属元素原子的半径逐渐增大,
A
点逐渐降低
金属键逐渐减弱
浓盐酸提供的大量C与金属离子形成稳定的配离子,
B
王水能溶解金和铂
增强了金属的还原性
缺角的NaCl晶体在饱和NaCl溶液中变为完美
C
晶体具有自范性
的立方体
D
C2H,NH,NO的熔点低于NH,NO
C2H,NH,NO,引人的乙基改变了晶体的类型
6.利用格氏试剂制备羧酸的原理为CH:MgBr
HO+
无水乙醚
CH,COOH。下列化学用语表述错误的是
AC02的电子式为0:C:d
B乙醚的结构简式为CH;OCH
C,HO+的VSEPR模型为四面体
D.题涉物质中碳原子的杂化方式有sp、sp、sp
.合成聚醚酯(PMD新型材料,可实现“单体一聚合物一单体”的闭合循环,推动塑料经济的可持续发展。合
成方法如下。下列说法不正确的是
0
苯甲醇
催化剂
单体00
聚醚酯(PM)
APM中含有酯基、醚键和羟基三种官能团
B.1molM与足量NaOH溶液反应,消耗1 mol NaOH
C.合成1 mol PM,理论上需要n mol M和nmol苯甲醇
D.M分子中不可能所有原子共面
&.三氯化碘(IC,)被广泛应用于药物合成,其熔点33℃、沸点77℃,易水解。氯气与单质碘需在温度稍低
于70℃下反应制备IC。实验室制备ICl的实验装置如图所示。
下列说法正确的是
化学试题(雅礼版)第2页(共8页)
浓盐酸
碱石灰
饱和食盐水
氯化钙碘单质
乙
丙
丁
戊
A.甲(无加热装置),烧瓶中的固体为二氧化锰
B.装置乙仅起到除杂的作用
C.装置丁可以采用水浴加热
丑将戊换成丙可以达到相同的效果
9.傢被称为“电子工业脊梁”,与铝性质相似。以砷化像废料(主要成分为GAs,含少量Fe2O2、SiO2等杂
质)为原料生产Ga,工艺流程如图。
蔬酸H,0,Ca(OH)2疏酸、(NH)S0
调pH
化馋一藩解一除豹
废
结晶
NH,Gn(SO)2
滤渣1
滤流2
NaOH溶液
加热
Ga-+一转溶一Ga(OH,
已知:砷化镓废料“溶解”后砷以H3AsO,形式存在。下列说法错误的是
A砷化镓废料“溶解”过程不宜采用“高温”条件
B.实验室“结晶”时主要用到的仪器有酒精灯、烧杯、坩埚、玻璃棒
C.“滤渣2”的主要成分为Fe(OH)1、Ca(AsO)2、CaSO,
D.电解Na[Ga(OHD,]溶液的阴极电极反应式为[Ga(OHD4]-+3e-Ga+4OH
10.储氢材料MgH2的晶胞结构如图所示,已知MgH2的摩尔质量
为Mg/mol,阿伏加德罗常数的值为NA。下列说法正确的是
A.H的配位数为2
B.晶胞中含有2个Mg2+
2M
Mg"
C.晶体密度的计算式为NAa。g/m
O
anm
D.Mg+(1)和Mg+(i)之间的距离为@+
-nm
2
11.已知:[FeCl,(H2O)2]为黄色,溶液中存在可逆反应:Fe++4CI十2H20→[FeCl4(H2O)2]-,下列
实验所得结论不正确的是
①
②
③
④
目
[目
固体
围
0.1mol…L
酸化的0.1mol·L
0.1 mol.L
Fe,(S0,溶藏
FeS0,落液
酸化的0.1mol·L
FeS0,溶箴
FeCl溶被
加热前溶液为浅黄色,加
加热前溶液接近无色,加
加人NaCl后,溶液立即变为
加热前溶液为黄色,加热
热后颜色变深
热后溶液颜色无明显变化
黄色,加热后溶液颜色变深
后溶液颜色变深
注:加热为微热,忽略体积变化。
A.实验①中,Fez(SO)3溶液显浅黄色的原因可能是Fe+水解产生了少量Fe(OH):
B.实验②中,加酸对Fe+水解的抑制程度大于升高温度对Fe+水解的促进程度
C.根据实验③现象得到:Fe3++4CI-+2H20[FeCL,(H2O)2]△H>0
D.实验④可证明升高温度,溶液颜色变深一定是因为F+水解平衡正向移动
化学试题(雅礼版)第3页(共8页)
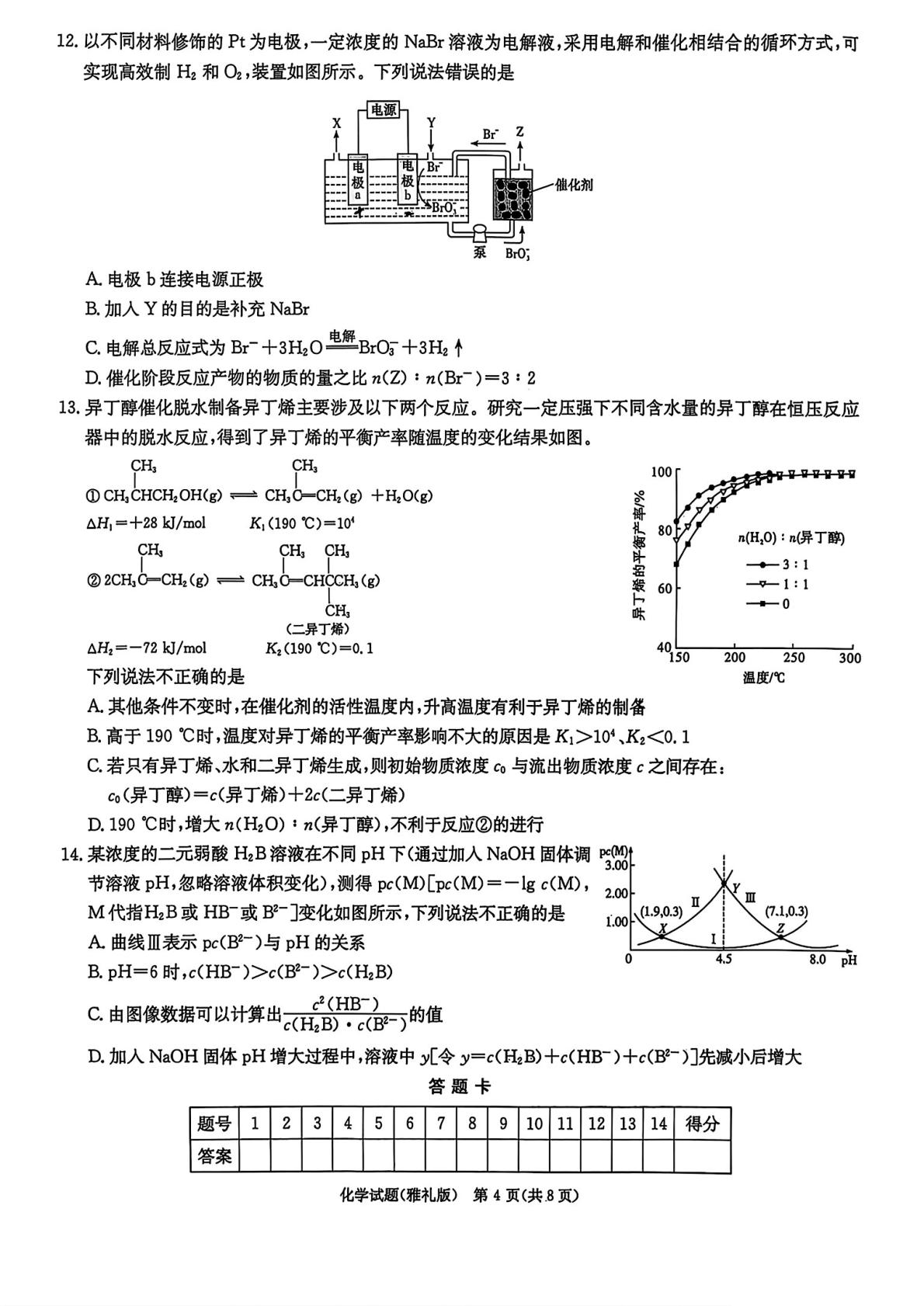
12.以不同材料修饰的Pt为电极,一定浓度的NaBr溶液为电解液,采用电解和催化相结合的循环方式,可
实现高效制H2和O2,装置如图所示。下列说法错误的是
电源
维化剂
BrO,
A.电极b连接电源正极
B.加人Y的目的是补充NaBr
C.电解总反应式为Br十3H,0电邂B0+3H2个
D.催化阶段反应产物的物质的量之比n(Z)n(Br)=3:2
13.异丁醇催化脱水制备异丁烯主要涉及以下两个反应。研究一定压强下不同含水量的异丁醇在恒压反应
器中的脱水反应,得到了异丁烯的平衡产率随温度的变化结果如图。
CH,
CH,
100
特特湘?双
D CH,CHCH,OH(g)CH,O-CH (g)+H:O(g)
△H1=+28k/mol
K1(190℃)=10
80
n(H,O):n屏丁胸
CH,
CH,CH,
◆一3:1
2CH,O-CH2 (g)CHO-CHCCH,(g)
名缘
60
g一1:1
CH,
。一0
味
(二异丁烯)
△H2=-72k/mol
K2(190℃)=0.1
150
200
250
300
下列说法不正确的是
温度/℃
A其他条件不变时,在催化剂的活性温度内,升高温度有利于异丁烯的制备
B.高于190℃时,温度对异丁烯的平衡产率影响不大的原因是K1>10、K2<0.1
C.若只有异丁烯、水和二异丁烯生成,则初始物质浓度c与流出物质浓度c之间存在:
c(异丁醇)=c(异丁烯)十2c(二异丁烯)
D.190℃时,增大n(H2O):n(异丁醇),不利于反应②的进行
14.某浓度的二元弱酸HzB溶液在不同pH下(通过加入NaOH固体调ps0
3.00
节溶液pH,忽略溶液体积变化),测得pc(MD[pc(M)=一lgc(MD,
2.00
M代指HB或HB或B-]变化如图所示,下列说法不正确的是
(1.9.0.3)
71.0.3)
L.00
A曲线Ⅲ表示pc(B-)与pH的关系
8.0
B.pH=6时,c(HB)>c(B2-)>c(H2B)
c2(HB-)
C由图像数据可以计算出,(B),B的值
D.加入NaOH固体pH增大过程中,溶液中y[令y=c(H2B)十c(HB)十c(B-)]先减小后增大
答题卡
题号
12
3
4
5
6
7
8
9
1011121314
得分
答案
化学试题(雅礼版)第4页(共8页)
第Ⅱ卷非选择题(共58分)
二、非选择题(本题共4小题,共58分)
15.(16分)三苯甲醇(相对分子质量为260)是一种有机合成中间体,利用格氏试剂制备三苯甲醇的原理
如下:
OC H
OMgBr
饱和NHC溶液
格氏试剂
已知:①THF(四氢呋喃)为常见的有机溶剂,能溶于水,沸点66℃。
②格氏试剂(RMgB)性质活泼,可与水、酯等物质反应。
③三苯甲醇为白色晶体,不溶于水,易溶于乙醇,在80%乙醇水溶液中溶解度随温度升高显著增大。
实验步骤:
I,制备:按如图所示装置安装相关仪器。向三颈烧瓶内加人格氏试剂
PhMgBr(3.62g,20mmol,Ph代表苯基),并置于冰水浴中,在搅拌下,由恒
压滴液漏斗A缓慢滴加苯甲酸乙酯(0.95g,6.3mmol)和THF(5mL)的混
合液。滴加完毕后,将冰水浴改为水浴加热,于70℃下继续回流1h,此时溶
液变为淡黄色。再次在冰水浴和搅拌下,由恒压滴液漏斗B缓慢滴加饱和
NHCl水溶液(15mL)。
Ⅱ.提纯:收集三颈烧瓶中的有机相,水相用乙酸乙酯(每次10L,2次)萃取,合并有机相并洗涤,有机
相用无水硫酸镁干燥,过滤后蒸馏除去溶剂,得粗产品。粗产品用80%乙醇水溶液热溶解,再经活性炭
脱色,
,抽滤后得白色固体产品0.63g。
回答下列问题:
(1)仪器C中盛放的物质为
(中性物质)。
(2)如图仪器中,分离有机相和洗涤有机相时均需使用的是
(填仪器名称)。
50 mL
(3)滴加饱和NHCl水溶液的作用是
(4)下列说法不正确的是
(填标号)。
A.保存格氏试剂(RMgBr)不需要密封
B.滴加饱和NH,C水溶液需在冰水浴下进行,是因为反应放热剧烈
C.步骤Ⅱ中水相用乙酸乙酯萃取时,有机层位于上层
D,固体产品可以通过X射线衍射测定物质结构
(5)步骤Ⅱ:“再经活性炭脱色,
,”(补充完整)。
(6)制备原理第一步反应的化学方得式为
(苯基用Ph表示)。
(7)三苯甲醇的产率为
(保留三位有效数字)。若水相未用乙酸乙酯萃取且合并有机相,则
导致测定结果
(填“偏高”“偏低或“无影响”)。
化学试题(雅礼版)第5页(共8页)
6.(14分)稀土是重要的战略资源。氧化铈(CO2)是应用广泛的稀土氧化物。由氟碳铈矿为原料制备
CeO2的工艺流程如下:
①NaOH溶液
②过滤
①硫脲
③盐酸
含Ce·NH,HCO.
Ce(CO,)
围体B
培烧
含CeF
②硫酸钠
步骤Ⅱ
的溶液
步骤Ⅲ
餐
的溶液
滤液D
步骤I
浸出
含氟溶液
固体A
资料:I,氟碳铈矿的主要成分为CeFCO.,主要杂质有BaO和SiO2:
.氢氟酸水溶液具有较强的挥发性;K.(HF)=6.6X10-;
M.Ce(OH)3难溶于水,可溶于强酸;固体B为Cez(SO,)3·Na2 SO,·nH2O,难溶于水也难溶于强酸。
(1)基态氟原子的价层电子排布式为
(2)“焙烧”在沸腾炉中进行。利用高压空气将矿石粉吹起并悬浮,形成类似液体沸腾的状态。这样操作
的目的是
(3)固体A的主要成分是SiO2和
(4)用硫酸浸出过程中,控制浸出时间40min、浸出温度55℃,Ce元素和CeF+的浸出率随起始硫酸浓度
的变化如图所示。c(H2SO)>3mol·L后,CeF+的浸出率下降,原因是
100
100
80
80
601
60
40
40
20
0.511522.533.54
c(Hs0(mol·L
(5)步骤I中硫脲作
剂。写出步骤Ⅲ反应的离子方程式:
(6)从化学平衡的角度,解释步骤Ⅱ中NaOH的作用是
化学试题(雅札版)第6页(共8页)
7.(14分)化合物H是一种抗艾滋病药物,某课题组设计的合成路线如下:
YH.
CF,COOC,H,
C,H,CI
CH,COCI
C.H.NO,F,CL乙l
H,0
NH
NHz
0
OH
已知:①
易被氧化;②RBr乙醚
MsR MgBr-H.O/H
R
回答下列问题:
(1)写出有机物A的名称:
(2)在合成过程中,A→B的目的是
,G→H的反应类型为
(3)化合物D的结构简式是
(4)下列说法错误的是
(填标号)。
aE分子中碳原子的杂化方式有3种
b.E→F的反应类型是消去反应
c.化合物H的分子式是C,HFCN2,易溶于水
HO
(5)化合物N(
)是另一合成路线的中间体,化合物N有符合下列条件的同分异构体,
H
写出其中的一种:
①含有苯环;
②H-NMR谱显示有6种不同化学环境的氢原子;
③能发生水解反应,产物之一是甘氨酸(HN一CH2一COOH)。
(6)以
和CH,CHO为原料,制备
的合成路线如下:
H
MgBr
Mg
H:O/
CH,CHO
醚
NH
H
K
写出J→K的化学反应方程式:
化学试题(雅礼版)第7页(共8页)
18.(14分)某制备乙炔的绿色环保新路线:BaCO和焦炭为原料,经反应I、Ⅱ得到BaC2,再由BaC2与水
反应。
反应I:BaCO2(s)+C(s)一BaO(s)+2CO(g)
反应Ⅱ:BaO(s)+3C(s)=BaC2(s)+C0(g)
回答下列问题:
(1)写出BaC2与水反应的化学方程式:
(2)已知:K=(器。)(是C0的化学计量系数)且反应I,Ⅱ的1gK与温度的关系曲线见图1,K,=
(pco)"。
2
反应1(1585,2.5)
(1320.00
-2
反应Ⅱ(1585,-1)
1200
1600
2000
T/K
图1gK与T的关系曲线
①反应BaCO(s)+4C(s)BaCz(s)+3C0(g)在1585K的Kp=
Pa
②保持1320K不变,假定恒容容器中只发生反应I,达到平衡时∞=
Pa;若将容器容积
压缩到原来的,重新建立平衡后p0」
(填标号)。
A.变大
B.不变
C.变小
(3)恒压容器中,焦炭与BaCO3的物质的量之比为4:1,Ar为载气。1400K和1823K下,BaC2产率
与时间的关系曲线依实验数据拟合得到图2(不考虑接触面积的影响)。
100
80
60
-1823K
20
=---1400K
4
时间
图2BaC,产率与时间的关系曲线
①初始温度为900K,缓慢加热至1400K时,实验表明BaCO已全部消耗,此时反应体系中含Ba物
种为
②1823K下~2时,反应速率的变化特点为
(4)科学家开发催化电极,在酸性介质中电解CO2制备乙炔,其阴极的电极反应式为
化学试题(雅礼版)第8页(共8页)
资源预览图

1

2

3
4
相关资源
由于学科网是一个信息分享及获取的平台,不确保部分用户上传资料的 来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系学科网,我们核实后将及时进行处理。