6.2024年北京市初中学业水平考试-【木牍中考】2025年安徽中考化学全解全析专题汇编
2024-10-12
|
2份
|
10页
|
135人阅读
|
9人下载
资源信息
| 学段 | 初中 |
|---|---|
| 学科 | 化学 |
| 教材版本 | - |
| 年级 | 九年级 |
| 章节 | - |
| 类型 | 试卷 |
| 知识点 | - |
| 使用场景 | 中考复习-学业考试 |
| 学年 | 2024-2025 |
| 地区(省份) | 北京市 |
| 地区(市) | - |
| 地区(区县) | - |
| 文件格式 | ZIP |
| 文件大小 | 3.00 MB |
| 发布时间 | 2024-10-12 |
| 更新时间 | 2024-10-12 |
| 作者 | 安徽木牍教育图书有限公司 |
| 品牌系列 | 中考试题精编·全解全析专题汇编 |
| 审核时间 | 2024-10-12 |
| 下载链接 | https://m.zxxk.com/soft/47882549.html |
| 价格 | 4.00储值(1储值=1元) |
| 来源 | 学科网 |
内容正文:
6.2024年北京市初中学业水平考试
木中考
18+5
化学
注意事项:
1.本试卷满分70分,考试时间70分钟。
2.可能用到的相对原子质量:H-1C-12N-14(O一16Ti-一48Fe-56
第一部分
本部分共25题,每题1分,共25分。在每题列出的四个选项中,选出最符合题目要求的一项。
1.下列变化属于化学变化的是
A.冰雪融化
B.酒精挥发
C.镁条燃烧
D.矿石粉碎
2.如表列出了某食品的营养成分,其中含量最高的是
项目
每100g
蛋白质
35.0g
脂肪
5.6g
碳水化合物
4.5g
钠
180mg
A.蛋白质
B.脂肪
C.碳水化合物
D.钠
3.下列物质属于纯净物的是
A.大理石
B.氯化钾
C.汽水
D.蔗糖溶液
深入打好蓝天、碧水、净土保卫战,持续优化生态环境。回答4一6题。
4.垃圾分类对保护土壤具有重要意义。下列属于厨余垃圾的是
A.空易拉罐
B.空矿泉水瓶
C.土豆皮
D.废旧报纸
5.为系统治理水资源、水环境、水生态,提倡的做法是
A.任意排放生活污水
B.防治海洋垃圾污染
C.农业上过量使用农药
D.景观用水大量使用自来水
6.为防治大气污染,下列做法不可行的是
A.加强扬尘管控
B.使用清洁能源
C.直接排放工业废气
D.加强大气质量监测
7.粗盐中难溶性杂质的去除实验中,蒸发滤液不需要用到的仪器是
A.蒸发皿
B.酒精灯
C.玻璃棒
D.量筒
8.下列标志表示“禁止烟火”的是
B
9.下列物质混合后产生白色沉淀的是
(
A.Na,CO,溶液和Ca(OH)2溶液
B.HO2溶液和Mn(O。
C.NaOH溶液和稀硫酸
D.NaHCO.溶液和稀盐酸
2024年6月,嫦娥六号完成世界首次月背采样,五星红旗在月背成功展开。回答10、11题。
10.嫦娥六号探测器钻杆主体采用铝基碳化硅材料。铝、碳、硅是三种不同的元素,决定元素种类的是(
A.质子数
B.中子数
C.核外电子数
D.相对原子质量
11.制作嫦娥六号月背展示国旗的原材料是玄武岩。玄武岩的组成元素有硅、铝、铁、钙等,其中属于非金属元
素的是
(
A.硅
B.铝
C.铁
D.钙
12.下列操作正确的是
不断搅拌
-TG
浓硫酸
水
A.倾倒液体
B.加热液体
C.读取液体体积
D.稀释浓硫酸
13.下列关于物质用途的描述不正确的是
A.O2用于食品防腐
B.NaCl用作调味品
C.干冰用于人工降雨
D.N2用作保护气
二十四节气蕴含丰富的文化内涵,反映了我国劳动人民的智慧。回答14~16题。
14.春分“竖蛋”。蛋壳的主要成分是碳酸钙,其化学式为
A.CaCl
B.Ca()
C.CaCO,
D.Ca(OH)2
15.请明放风筝。下列与风筝制作、放飞相关的部件中,用到金属材料的是
A.竹质骨架
B.纸质风筝面
C.棉质捆扎线
D.不锈钢手握轮
16.秋分吃桂花糕。桂花中含甜菜碱(CH,NO2),下列关于C,H,NO2的说法正确的是
A,由三种元素组成
B.氢、氮元素质量比为11:14
C.氢元素的质量分数最大
D.碳、氧原子个数比为2:5
为实现“双碳”目标,我国积极推动能源绿色低碳安全高效转型。回答17一20题。
17.下列燃料在O,中充分燃烧时,不会产生CO,的是
(
A.CH
B.CO
C.C.H:OH
D.H2
18.为实现高效光催化分解水制氢,科研人员开展Nb,N,纳米复合光催化材料的研究。铌(Nb)在元素周期表
中的原子序数是41,下列关于Nb的说法不正确的是
A.质子数是41
B.核电荷数是41
C.原子质量是41
D.核外电子数是41
19.CH,与CO2在一定条件下反应生成H2和CO,该制氢反应的微观示意图如图所示:
。一氢原子
p+⑦○0
一定条件
氧原子
甲
丙
碳原子
图中丁的微观图示为
02
B
0
20.甲烷水蒸气重整制氢的反应为CH,十HO
能化剂CO+3H,下列说法不正确的是
高温
A.反应涉及两种氧化物
B.反应前后氢原子个数不变
C.生成的CO、H2的分子个数比为1:1
D.参加反应的CH,、HO的质量比为8:9
卿酸在生产生活中有广泛应用。20℃时,进行如下实验。完成下面小题。回答21~23题。
加入2g
加入2g
加入2g
加入2g
100g水
硼酸
硼酸
硼酸
硼酸
①
3
资料:20℃时,硼酸的溶解度为5.0g:40℃时,硼酸的溶解度为8.7g。
21.①~④所得溶液中,溶质与溶剂的质量比为1:50的是
A.①
B.②
C.③
D.④
22.③所得溶液的质量为
A.104g
B.105g
C.106g
D.108g
23.下列关于①~④的说法不正确的是
A.①所得溶液为不饱和溶液
B.若②升温至40℃,溶质质量变大
C.若向③中加水,溶液质量变大
D.若④升温至40℃,得到不饱和溶液
24.下列关于Fe在O2中燃烧的反应叙述不正确的是
A.放出热量
B.生成黑色固体FeO
C.反应前后固体质量相等
D.参加反应的Fe与生成物中铁元素质量相等
25,用如图所示装置进行实验,测定出空气中O,约占号(按体积计算)。下列叙述不正确的是
100mL水
铁丝
打开胶塞
取出200mL水,
白磷(着火点为40℃)
连接装置
水
©
A.②中瓶内空气的体积约为200mL
B.可加热铁丝引燃铜匙中的白磷
C.白磷的作用是消耗②中瓶内的O
D.最终注射器活塞移至约40mL刻度线处
第二部分
本部分共14题,共45分。
【生活现象解释】
26.(2分)“九门走九车”说的是老北京内城九座城门的昔日景象。
(1)西直门走水车。水的组成元素是
(2)卓成门走煤车。除煤外,化石燃料还有天然气和
27.(2分)大豆既能通过根系吸收肥料氨,又能利用根瘤菌固定空气中的氨。
(1)下列物质中,属于氮肥的是
(填序号)。
A.K2CO
B.CO(NH2)2
C.Ca(H2 PO)2
(2)空气中含氨元素的物质主要是
28.(3分)化学与生活息息相关
发酵粉
八
(1)捞饺子对应的分离固液混合物的实验操作是
(2)发酵粉(含NaHCO)可用于制作面包。NaHCO,的俗称是
(3)盐酸可用于除铁锈(主要成分为FeO,),原理为
(用化学方程式表示)。
【科普阅读理解】
29.(6分)阅读下面科普短文。
生活中有时需要用到高浓度O2,供氧方式主要有氧气瓶、氧气袋和制氧机。
氧气瓶和氧气袋中的O2一般用深冷法制得,该方法利用物质的沸点差异,从空气中分离出O2。
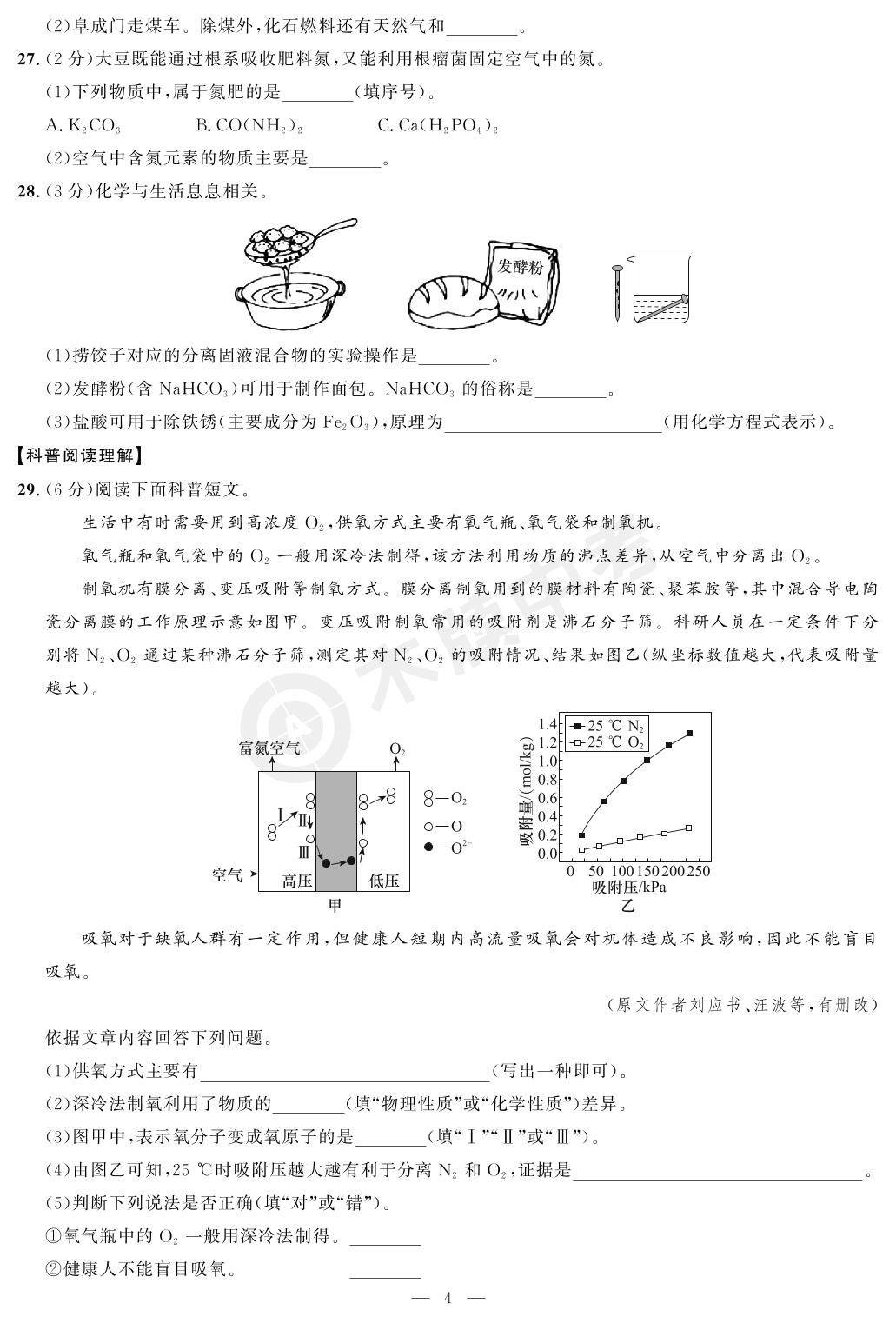
制氧机有膜分离、变压吸附等制氧方式。膜分离制氧用到的膜材料有陶瓷、聚苯胺等,其中混合导电陶
瓷分离膜的工作原理示意如图甲。变压吸附制氧常用的吸附剂是沸石分子筛。科研人员在一定条件下分
别将N2、O2通过某种沸石分子筛,测定其对N2、O:的吸附情况、结果如图乙(纵坐标数值越大,代表吸附量
越大)。
1.4
■25CN2
富氮空气
0
12。
1.0
◆
0.8
88
8-0
0.61
0.4
8
0-0
●一0子
蓄0d
Ⅲ
0.0t
00000
空气
高压
低压
050100150200250
吸附压kPa
甲
乙
吸氧对于缺氧人群有一定作用,但健康人短期内高流量吸氧会对机体造成不良影响,因此不能盲目
吸氧
(原文作者刘应书、汪波等,有删改)》
依据文章内容回答下列问题。
(1)供氧方式主要有
(写出一种即可)。
(2)深冷法制氧利用了物质的
(填“物理性质”或“化学性质”)差异。
(3)图甲中,表示氧分子变成氧原子的是
(填“1”“Ⅱ”或“Ⅲ”)。
(4)由图乙可知,25℃时吸附压越大越有利于分离N和O2,证据是
(5)判断下列说法是否正确(填“对”或“错”)。
①氧气瓶中的O2一般用深冷法制得。
②健康人不能盲目吸氧。
【生产实际分析】
30.(2分)电石渣[主要成分为C:(OH)2]是电石法生产乙炔的副产物,可资源化利用。
(1)处理工业废水。用电石渣可处理
(填“酸性”或“碱性”)废水。
(2)制备工业产品。用电石渣生产CaO的主要反应为Ca(OH):△CaO+H,O,该反应属于基本反应类型
中的
31.(4分)硫化钠(NaS)广泛应用于染料、造纸等工业、以NaSO,为原料制备Na,S的部分流程如图所示。
H
H.
NaOH溶液
HS、H
Na2SO
+Na,S溶液
NaS固体
设备1
设备2
已知:H2S为副产物,直接排放会造成环境污染
E平化学方程式:回Na,S0,+口H,口Na,S+口H0
(2)Na,S中S的化合价为
(3)图中标示出的物质中,属于单质的是
(4)设备2中,加入NaOH溶液的目的是
【基本实验及其原理分析】
32.(1分)补齐仪器与名称的连线。从A或B中任选一题作答,若均作答,按A计分。
A
B
烧杯
漏斗
锥形瓶
集气瓶
胶头滴管
试管夹
33.(4分)选用如图装置进行O2的制取实验。
(1)用KMnO,制取O2的化学方程式为
,发生装置是
(填序
号)。
(2)用向上排空气法收集O2的原因是
(3)用带火星的木条检验O2已收集满,现象是
34.(3分)用如图所示装置和干燥紫色石蕊纸花进行实验,验证C(O2的性质。
玻璃片
CO,
干燥紫色
澄清
石蕊纸花
石灰水
(1)观察到澄清石灰水变浑浊,反应的化学方程式为
:由该实验还可以
得出分子具有的性质是
(2)为验证CO,能与水反应,需进行的操作及现象是
35.(3分)用如图所示实验验证金属的性质。
铁丝
电池
铜丝
铁丝
稀硫酸
CuSO,溶液
铁
实验1
实验2
实验3
(1)实验1,观察到灯泡发光,说明铁具有的性质是
(2)实验2中反应的化学方程式为
(3)实验3能证明铁的金属活动性比铜的强,现象是
36.(2分)用如图所示实验验证可燃物燃烧的条件。
气球
0
80℃水
已知:白磷的着火点为40℃,红磷的着火点为240℃
(1)若a、b均为白磷,可观察到的现象是
(2)若a、b均为红磷,判断该实验能否证明可燃物燃烧需要与O,接触,并说明理由:
37.(3分)完成实验报告。
实验
1
2
3
目的
验证CO2不支持燃烧
鉴别NaOH溶液和盐酸
配制
NaCI溶液
试剂a
3gNaC47mL水
CO,
操作
燃着的
蜡烛
溶液①
溶液②
已知:Pk=1gcm
现象
①变红,②不变色
固体全部溶解
(1)实验1中,现象是
(2)实验2中,试剂a为
(3)补全实验3的目的:配制
NaCI溶液。
【科学探究】
38.(7分)同学们把盛有自上而下依次呈现多种颜色溶液的试管称为“彩虹管”。小组同学看到某个“彩虹管”的
制作过程(如图)后,对影响“彩虹管”效果的因素进行探究。
—6
黑枸杞
NaOH溶液
浸取液
振荡
红色
團盐酸
蓝色
黄色
已知:“彩虹管”呈现出的颜色越多、保持时间越长,效果越好。
【进行实验】
实验1:用蒸馏水浸泡黑枸杞得到浸取液,分别滴入H不同的无色溶液中,记录现象。
pH
≤3
45
6~8
9-11
12
≥13
溶液颜色
红色
粉色
紫色
蓝色
绿色
黄色
实验2:向试管中加入6mL一定质量分数的盐酸,滴入5滴黑枸杞浸取液、振荡,再逐滴滴入约3mL一定
质量分数的NaOH溶液,之后记录溶液颜色。
盐酸中溶质的质量
NaOH溶液中溶质
实验
溶液颜色
分数/%
的质量分数/%
①
5
红色
自上而下依次为红色、蓝色、黄色,静置约6分钟只
②
5
10
剩红色、黄色
自上而下依次为红色、蓝色、黄色,静置约20分钟仍
③
5
15
无明显变化
④
10
自上而下为无色、红色
⑤
10
10
红色
自上而下依次为红色、蓝色,黄色,静置约6分钟只
⑥
10
15
剩红色、黄色
【解释与结论】
(1)向pH=7的无色溶液中滴加黑枸杞浸取液,溶液颜色变为
(2)盐酸与NaOH反应的化学方程式为
(3)实验2中,①②③的目的是
(4)实验2中,“彩虹管”效果最佳的是③,理由是
【进一步探究】
查阅资料发现,在NaOH溶液中加入一定量NaCO,可使“彩虹管”效果更好。小组同学设计实验3进行验
证,并与实验2中③对照。
实验3:向100mL质量分数为15%的NaOH溶液中加入1 g NazCO,固体,搅拌后得到溶液a,进行如下实
验并记录。
操作
现象
再逐滴滴
立即出现气泡:滴加完成后溶液颜色自上而下依次为红色、粉色、紫色、蓝色、绿
入约3mL溶液a
色、黄色,静置约1小时仍无明显变化
【解释与结论】
(5)补全实验3的操作:
(6)实验3中观察到气泡,推测有气体生成,该气体是
(7)由实验2、3可知:制作“彩虹管”过程中,影响其效果的因素一定有
【实际应用定量计算】
39.(3分)氢化钛(TiH,)作为储氢材料备受关注。用铁粉(T)生产TH的反应为Ti十H,一定条件TH。若
制得100kgTH:,计算参加反应的H,的质量(写出计算过程及结果)。
木牍中者
—8-6.2024年北京市初中学业水平考试
参考答案
1.C2.A3.B4.C5.B6.C7.D8.B9.A10.A11.A12.D13.A14.C15.D16.B
17.D18.C19.D20.C21.A22.B23.B24.C25.D
26.(1)氢、氧元素(2)石油
27.(1)B(2)氮气(或N:)
28.(1)过滤(2)小苏打(3)FeO3+6HC1=2FeCl+3HO
29.(1)氧气瓶(或氧气袋或制氧机)
(2)物理性质(3)Ⅱ
(4)25℃时,吸附压越大,氨气的吸附量越大,而氧气的吸附量变化不大
(5)①对②对
30.(1)酸性(2)分解反应
31.(1)414(2)-2
(3)氢气(或H)(4)分离出H2,吸收H,S得到Na:S产品
32.A
B
烧杯
漏斗
锥形瓶
集气瓶
胶头滴管
试管夹
33.(1)2KMn0,△K,MnO,+Mn02+0,↑A
(2)氧气密度大于空气
(3)置于集气瓶口的带火星的木条复燃
34.(1)CO2+Ca(OH)2CaCO3¥+HO分子在不断运动
(2)先将干燥紫色石蕊纸花放入盛有二氧化碳的集气瓶中,纸花不变色,将纸花取出喷水后再放入盛有二氧
化碳的集气瓶中,纸花变红
35.(1)导电性
(2)Fe+H2 SO,=FeSO,+H2
(3)铁丝表面覆盖一层红色物质,溶液由蓝色逐渐变为浅绿色
36.(1)a处白磷不燃烧,b处白磷燃烧
(2)不能,因为温度未达到红磷的着火点,a、b处的红磷均不燃烧
37.(1)燃着的蜡烛熄灭(2)酚酞溶液(3)6%
38.(1)紫色(2)HC1+NaOH-NaC1+HO
(3)探究盐酸和氢氧化钠反应的质量关系对“彩虹管”效果的影响
(4)呈现出的颜色最多、保持时间最长
(5)向试管中加入6mL一定质量分数的盐酸、滴入5滴黑枸杞浸取液、振荡
(6)二氧化碳(7)溶液pH的变化情况等(合理即可)
39.解:设参加反应的H2的质量为x。
9
Ti十H,一定条件TH。
2
50
100kg
2
x
50100kg
x=4 kg
答:参加反应的H2的质量为4kg。
木膜中者
-10-
资源预览图

1

2

3
4
相关资源
由于学科网是一个信息分享及获取的平台,不确保部分用户上传资料的 来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系学科网,我们核实后将及时进行处理。

